既治療の切除不能進行・再発胃癌/食道胃接合部癌に対するPembrolizumabとPaclitaxelの無作為化比較第III相試験(KEYNOTE-061試験)
Pembrolizumab vs paclitaxel for previously treated advanced gastric or gastroesophageal junction cancer: phase 3 KEYNOTE-061 trial
Charles S. Fuchs, et al.
監修コメント

山﨑 健太郎先生
静岡県立静岡がんセンター 消化器内科 医長
本試験ではあらかじめ設定された統計学的設定を満たすことができず、残念ながら主要評価項目を達成することができなかった。しかし発表では、PD-L1発現別の解析やMSI-High(マイクロサテライト不安定性が高いもの)における解析などもあわせて報告され、抗PD-1抗体薬が有効な患者集団を絞り込める可能性を示した点ではポジティブな発表であり、今後の開発や解析へ大きなインパクトを与える結果であったと考える。また、本結果は発表同日にLancet1)に掲載されており、是非一読していただきたい。
(コメント・監修:静岡県立静岡がんセンター 消化器内科 医長 山﨑 健太郎)
切除不能進行・再発胃癌/食道胃接合部癌に対する二次化学療法におけるPembrolizumabとPaclitaxelを比較
第III相比較試験であるATTRACTION-2試験の結果、既治療の切除不能進行・再発胃癌/食道胃接合部癌に対し、抗PD-1抗体薬であるNivolumabは、プラセボに比べ全生存(OS)期間を延長したことから、本邦でもNivolumabは標準治療薬の1つとなっている。一方、同様の抗PD-1抗体薬であるPembrolizumabは、KEYNOTE-059試験の結果を受け、2レジメン以上の化学療法に不応または不耐となった切除不能進行・再発胃癌/食道胃接合部癌に対し、米国FDAでは承認を受けている。
2017年のASCOとESMOではPembrolizumabの有効性を検証する第II相試験であるKEYNOTE-059試験の結果が報告され、切除不能進行・再発胃癌/食道胃接合部癌に対し三次化学療法でのPembrolizumab単剤(コホート1)、未治療患者におけるフッ化ピリミジン系薬剤(5-FUまたはCapecitabine)+CDDPとの併用療法(コホート2)、Pembrolizumab単剤(コホート3)の結果が報告され、良好な抗腫瘍効果が示唆された2-4)。
本試験は、切除不能進行・再発胃癌/食道胃接合部癌に対する二次化学療法において、Pembrolizumab単剤と標準治療薬の1つであるPaclitaxel(週1回投与)とを比較した第III相試験である。
主要評価項目はPD-L1 陽性(CPS≧1)における全生存(OS)期間と無増悪生存(PFS)期間
本試験は、フッ化ピリミジン系薬剤+プラチナ製剤の併用療法後に病勢進行(PD)した切除不能進行・再発胃癌/食道胃接合部癌患者が対象で、Pembrolizumab療法群(200mg、3週毎)とPaclitaxel療法群(80mg/m2、day 1,8,15、4週毎)に無作為に割り付けられた。HER2陽性患者はTrastuzumabを投与された症例に限られ、扁平上皮癌や未分化癌の患者は対象に含まれていない。
PD-L1発現率は22C3抗体を用いた免疫組織染色のCPS[combined positive score、PD-L1で染色された細胞数(腫瘍細胞、リンパ球、マクロファージ)/全生存細胞数×100]で評価され、本試験では1%以上(CPS≧1)の場合が陽性とされた。総登録数592例のうち最初の489例はPD-L1の陽性/陰性にかかわらず登録されたが、最後の103例はPD-L1陽性(CPS≧1)のみが登録対象となった。層別因子は、地域、CPS(<1 vs. ≧1)、一次化学療法の無増悪期間(TTP)(6ヵ月未満 vs. 6ヵ月以上)などであった。最終的にはPD-L1陽性(CPS≧1)395例のうち、196例がPembrolizumab療法群に、199例がPaclitaxel療法群に割り付けられた。
主要評価項目は、PD-L1陽性(CPS≧1)例における全生存(OS)期間と無増悪生存(PFS)期間で、試験全体では片側α=0.025と設定され、OSが統計学的有意を示すにはp<0.0135を達成する必要があった。副次評価項目は、PD-L1陽性(CPS≧1)例における奏効率(ORR)と奏効期間(DR)、全症例における安全性などであった。Pembrolizumab療法群とPaclitaxel療法群における患者背景に大きな隔たりは認めなかった。
Pembrolizumabは奏効症例では効果が長く持続したが、OSにおいて統計学的有意差は示せなかった
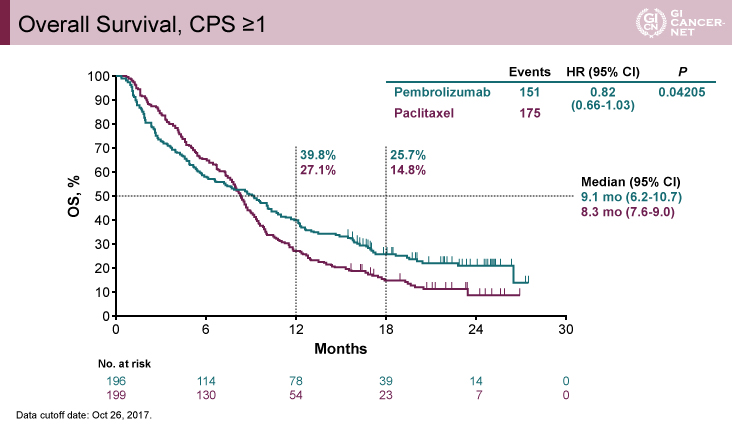
PD-L1陽性(CPS≧1)例におけるOS期間の中央値(MST)は、Pembrolizumab療法群9.1ヵ月、Paclitaxel療法群8.3ヵ月[ハザード比(HR)=0.82、片側p=0.042]で、Pembrolizumab療法群において良好であったが、統計学的な有意差は示せなかった。Pembrolizumab療法群とPaclitaxel療法群のOS率は、治療開始後12ヵ月では39.8% vs. 27.1%、18ヵ月では25.7% vs. 14.8%であり、長期生存症例はPembrolizumab療法群で多かった(図1)。
図1 Overall Survival, CPS≧1(発表者の許可を得て掲載)
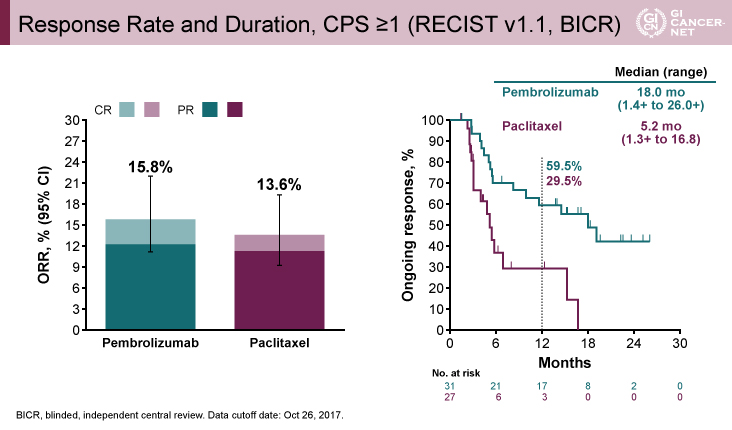
PD-L1陽性(CPS≧1)例におけるPFSおよびORRでは、両群に差は認められなかった(図2、図3)。しかし、奏効例[部分奏効(PR)以上を達成]のDR中央値は、Pembrolizumab療法群18ヵ月 vs. Paclitaxel療法群5.2ヵ月、12ヵ月以上の持続的奏効率(DRR)は59.5% vs. 29.5%で、Pembrolizumab療法群では奏効が持続することが示された(図3右)。
図2 Progression-Free Survival, CPS≧1(発表者の許可を得て掲載)
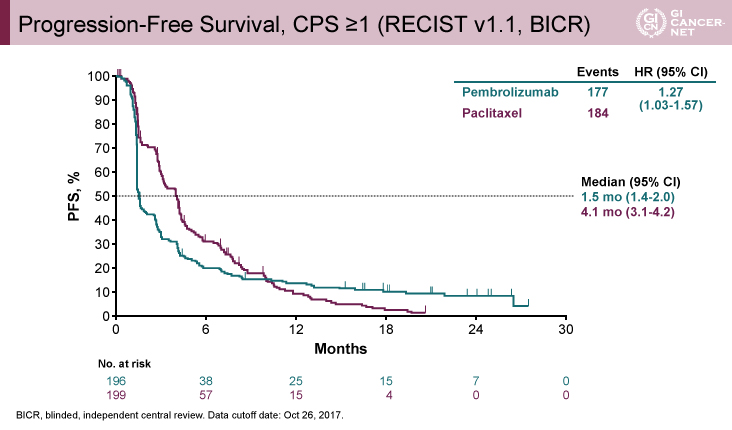
図3 Response Rate and Duration, CPS≧1(発表者の許可を得て掲載)
PD-L1がCPS 1未満の症例ではPembrolizumab療法の効果が乏しく、CPSが高くなるに伴い効果が高まることが示された。また、MSI-High例におけるサブグループ解析(Pembrolizumab療法群15例、Paclitaxel療法群12例)では、Pembrolizumab療法群におけるOS期間、ORRが良好であった(OSは未達、ORR 46.7%)。
全症例における安全性については、Grade 3-5の有害事象発現率が、Pembrolizumab療法群14.3%、Paclitaxel療法群34.8%で、Pembrolizumab群でより安全に治療が行われた。
まとめ
本試験では、切除不能進行・再発胃癌/食道胃接合部癌のPD-L1陽性(CPS≧1)例に対する二次化学療法におけるPembrolizumab療法は、Paclitaxel療法に対するOS期間延長効果を示せなかった。しかし、ECOG PS(performance status)0、PD-L1 CPS≧10、MSI-Highといったサブグループ解析においてはPembrolizumab療法群のOS期間延長効果は良好で、Pembrolizumab療法奏効例でのDRは非常に良好であったことから、Pembrolizumab単剤での化学療法における治療効果予測因子のさらなる探索が重要であると考えられた。
(レポート:香川大学医学部 腫瘍内科 大北 仁裕)
References
1) Shitara K, et al.: Lancet. June 4, 2018 [Epub ahead of print][PubMed]
2) Fuchs CS, et al.: ASCO 2017 #4003
3) Bang YJ, et al.: ASCO 2017 #4012
4) Wainberg ZA, et al.: ESMO 2017 #LBA28
関連リンク
・Kang YK, et al.: Lancet. 390(10111): 2461-2471, 2017[PubMed]
・2レジメン以上の化学療法に対して不応・不耐であった進行胃癌・食道胃接合部癌に対するNivolumab療法:無作為化二重盲検Placebo対照第III相試験(ATTRACTION-2試験)[論文紹介]
・KEYNOTE-059試験:ASCO 2017 #4003+4012[学会レポート]
・KEYNOTE-059試験:ESMO 2017 #LBA28[学会レポート]

監修
谷口 浩也先生
愛知県がんセンター中央病院
薬物療法部 医長
加藤 健先生
国立がん研究センター中央病院
消化管内科 医長
山﨑 健太郎先生
静岡県立静岡がんセンター
消化器内科 医長
上野 誠先生
神奈川県立がんセンター
消化器内科 医長
レポーター (50音順)
伊澤 直樹先生
聖マリアンナ医科大学
臨床腫瘍学
大北 仁裕先生
香川大学医学部
腫瘍内科
小林 智先生
神奈川県立がんセンター
消化器内科
佐藤 雄哉先生
国立がん研究センター中央病院
臨床研究支援部門
高橋 直樹先生
埼玉県立がんセンター
消化器内科
寺島 健志先生
金沢大学
先進予防医学研究センター
古田 光寛先生
静岡がんセンター
消化器内科
堀田 洋介先生
埼玉医科大学国際医療センター
消化器腫瘍科