RAS野生型切除不能進行・再発大腸癌(mCRC)に対する一次療法としてのmodified FOLFOXIRI+Panitumumab併用療法vs. FOLFOXIRI療法:AIO-KRK-0109/VOLFI試験(無作為化第II相試験)における有効性とQOL
Efficacy and quality of life in VOLFI trial: mFOLFOXIRI + Panitumumab versus FOLFOXIRI as first-line treatment in patients with RAS wild-type metastatic colorectal cancer (mCRC): a randomized phase II trial of the AIO (AIO-KRK-0109).
Michael Geissler, et al.
監修コメント
FOLFOXIRI[Fluorouracil(5-FU)+Leucovorin(LV)+Oxaliplatin(OX)+Irinotecan(IRI)]療法は、TRIBE試験においてBevacizumab(Bmab)との併用という形で、FOLFIRI(5-FU+LV+IRI)療法との比較においてポジティブな結果を出してきた1)。しかし、Bmab併用ということもあり、TRIBE試験ではRAS/BRAF変異症例が多かった。予後不良であるBRAF変異型に対する有効性を示した重要な結果であったが、一方でRAS野生型に対する有効性、特に抗EGFR抗体の効果がそれほど期待できない右側原発の結腸癌での効果がどうなのかというところがQuestionであった。
本VOLFI試験は、RAS野生型に対して、FOLFOXIRI療法と、FOLFOXIRI療法にPanitumumab(Pmab)を上乗した少数例で比較した無作為化第II相試験である。主要評価項目は奏効割合(objective response rate: ORR)で、すでにESMO 2017において、ORR、無増悪生存(PFS)期間について報告がなされていたが、ORRはPmab併用群で上回り、腫瘍縮小後の切除割合も上昇するものの、PFS期間では有意差を認めないというものであった。今回の発表は、長期観察に伴い腫瘍切除割合の向上が全生存(OS)期間に対してどのようにインパクトを与えるのかが注目されたが、今回の発表はサブグループ解析とQOL解析についての発表であった。
主要評価項目であるORRはFOLFOXIRI+Pmab療法群87.3%と2017年の発表より1.6%増加していたが、FOLFOXIRI療法群では60.6%と2017年と同様であった。注目すべきは、抗EGFR抗体をもってしても治療効果不十分と思われる右側結腸に対する効果である。左側に比べると劣るが、右側であってもFOLFOXIRI+Pmab療法群で70.0%のORRを示し、Pmabの上乗せがないFOLFOXIRI療法群の37.5%に比べて良好であった。同様に、RAS陽性BRAF変異型に対してもORR 85.7%と良好な結果であった。少数例の検討であることに注意は必要であるが、治療効果不良な対象に対する選択肢の1つとなり得る。またQOLについては、額面上の毒性増加のわりに両群であまり差を認めなかった。
やはり、PFS期間やOS期間がどうなのかということが注目される。今後の発表に期待したい。
(コメント・監修:国立がん研究センター中央病院 消化管内科 医長 加藤 健)
modified FOLFIXIRI+抗EGFR抗体併用療法における初の非盲検無作為化比較試験
FOLFOXIRI[Fluorouracil(5-FU)+Leucovorin(LV)+Oxaliplatin(OX)+Irinotecan(IRI)]療法は、大腸癌の一次治療として奏効割合(objective response rate: ORR)や生存延長について良好な成績を残している1)。本試験(VOLFI trial)は、modified FOLFOXIRI(mFOLFOXIRI)+抗EGFR抗体(Panitumumab: Pmab)併用療法における初の無作為化比較試験である。試験デザインは非盲検の無作為化第II相試験であり、mFOLFOXIRI+Pmab療法群とFOLFOXIRI療法群に2:1で割り付けされた。また、切除の可能性がない群(コホート1)と切除の可能性を有する群(コホート2)に層別化された。
主要評価項目は、RECIST 1.1に基づくORR、副次評価項目は、無増悪生存(PFS)期間、全生存(OS)期間、病勢コントロール割合(DCR)、奏効期間(DR)、QOL(EORTC QLQ-C30)、二次的切除割合、毒性などであった。
ORRはmFOLFOXIRI+Pmab療法群で有意に高かった
mFOLFOXIRI+Pmab療法群に63例、FOLFOXIRI療法群に33例が割り付けられた。治療期間中央値、治療サイクルは両群で同じであり、それぞれ5.4ヵ月、11サイクルであった。
主要評価項目であるORRは、mFOLFOXIRI+Pmab療法群87.3%、FOLFOXIRI療法群60.6%であり、mFOLFOXIRI+Pmab療法群において有意に高かった(p=0.004)。原発部位(tumor sidedness)別では、左側結腸でmFOLFOXIRI+Pmab療法群90.6% vs. FOLFOXIRI療法群68.0%、右側結腸で同様に70.0% vs. 37.5%であった。遺伝子変異型別では、RAS/BRAF野生型でmFOLFOXIRI+Pmab療法群86.0% vs. FOLFOXIRI療法群64.7%、BRAF変異型で同様に85.7% vs. 22.2%で、いずれのサブセットにおいてもmFOLFOXIRI+Pmab療法群で高いORRであった(図1)。
しかしながら、ORRの高さがPFS期間の延長へと必ずしも反映されていなかった(図2)。
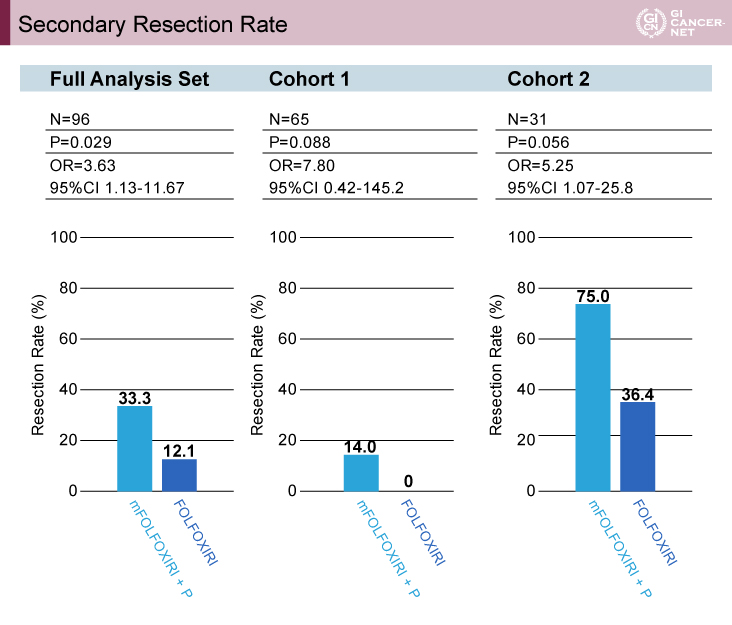
二次的切除割合はmFOLFOXIRI+Pmab療法群33.3% vs. FOLFOXIRI療法群12.1%で、コホート別にみても同様に、コホート1では14.0% vs. 0%、コホート2では75.0% vs. 36.4%で、いずれにおいてもmFOLFOXIRI+Pmab療法群で高い切除割合を認めた(図3)。
図1 Object response rate(発表者の許可を得て掲載)
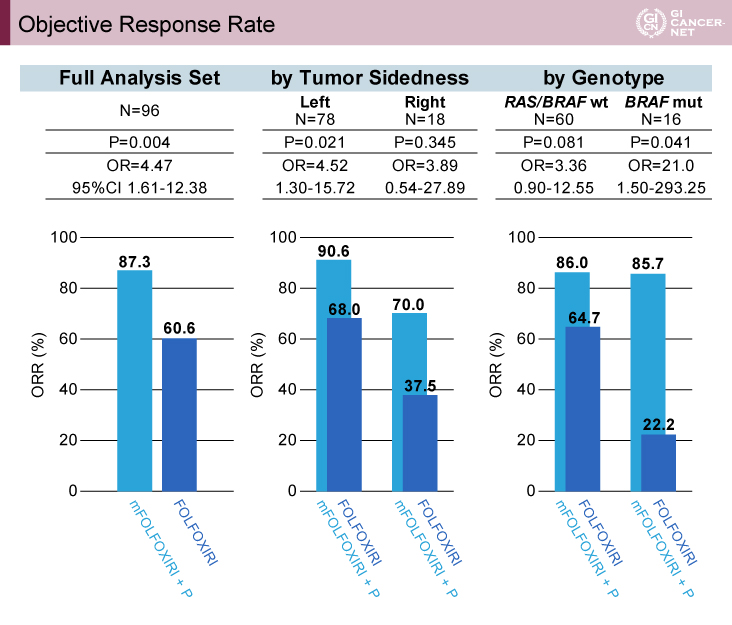
図2 Progression-free survival(発表者の許可を得て掲載)
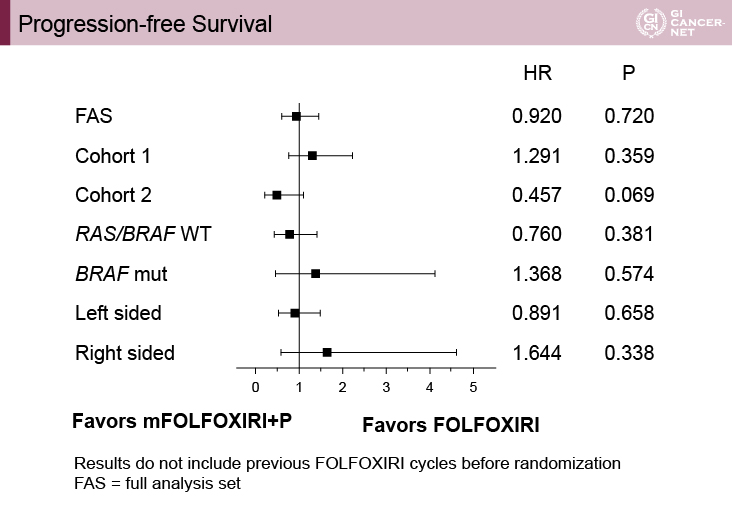
図3 Secondary resection rate(発表者の許可を得て掲載)
QLQ-C30スコアでは両群に有意差が認められなかった
各薬剤で10%超の減量を要した割合は、IRIではmFOLFOXIRI+Pmab療法群68.3% vs. FOLFOXIRI療法群54.5%、以下同様に、OXでは61.9% vs. 54.5%、5-FUでは69.8% vs. 48.5%であり、いずれもmFOLFOXIRI+Pmab療法群で高い割合であった。また、Pmabの10%超の減量を要した割合は30.2%であった。
血液毒性についてはgrade 3以上の好中球減少が、mFOLFOXIRI+Pmab療法群15.6%、FOLFOXIRI療法群21.2%で、FOLFOXIRI療法群で発現率が高かった。全gradeにおけるG-CSFによるサポートは、mFOLFOXIRI+Pmab療法群30.2%、FOLFOXIRI療法群18.2%であり、mFOLFOXIRI+Pmab療法群においてより多くの割合で行われた。非血液毒性においてはgrade 3以上の下痢が、mFOLFOXIRI+Pmab療法群25.0%、FOLFOXIRI療法群12.1%であり、mFOLFOXIRI+Pmab療法群でより多く認められた。
QOLは毒性(CTC 3.0による)を強く認めた群(grade 3/4)と認めなかった群(grade 1/2)でQLQ-C30スコアで有意差が認められず、コホート1とコホート2の間においても有意差は認められなかった。ECOG PS(performance status)0では1の群に比して有意にQLQ-C30スコアが高かったが(p=0.049)、開始時の腫瘍による症状(initial tumor symptoms)の有無では有意差が認められなかった。Global health status、physical functioning、social functioningの各推移においても両群間で経時的な有意差は認められなかった。
まとめ
mFOLFOXIRI+Pmab療法群はFOLFOXIRI療法群に比べて高いORRを認め、その割合は左側結腸群やBRAF変異群において顕著であった。ただし、ORRの高さがPFS期間の延長へと必ずしも反映されていなかった。切除の可能性がないコホート1においても、mFOLFOXIRI+Pmab療法群においては高い切除割合が達成された。腫瘍症状を有する、もしくは切除を念頭においた症例においては、原発部位やBRAF statusにかかわらずmFOLFOXIRI+Pmab療法群の高いORRが注目される。また、本試験においては有害事象の増強が必ずしもQOLの低下へとつながらなかった。
(レポート:がん研有明病院 消化器化学療法科 医員 鈴木 健)
References
関連サイト
- ・AIO-KRK-0109試験[ClinicalTrials.gov]
- ・RAS野生型切除不能進行・再発大腸癌に対するmodified FOLFOXIRI+Panitumumab併用療法の無作為化第II相試験(AIO-KRK-0109/VOLFI試験):ESMO 2017 #475O[学会レポート]
- ・TRIBE試験[ClinicalTrials.gov]
- ・切除不能転移・再発大腸癌へのfirst line治療としての静注LV/5-FU/L-OHP/CPT-11療法(FOLFOXIRI)と静注LV/5-FU/CPT-11療法(FOLFIRI)の比較第III相試験:The Gruppo Oncologico Nord Ovest(GONO)[論文紹介]

加藤 健 先生
国立がん研究センター中央病院 消化管内科 医長