2017年1月19日~21日に米国サンフランシスコにて開催された2017年 消化器癌シンポジウム(2017 Gastrointestinal Cancers Symposium)より、大腸癌や胃癌などの注目演題のレポートをお届けします。演題レポートの冒頭には“Expert's view”として、臨床研究の第一線で活躍する監修ドクターのコメントを掲載しています。
胃癌
切除不能進行・再発胃・食道胃接合部癌における年齢別によるRamucirumabの有効性・安全性の解析(REGARD試験とRAINBOW試験)
Efficacy and safety of ramucirumab …
Kei Muro, et al.
Expert’s view

山﨑 健太郎先生
静岡県立静岡がんセンター 消化器内科 医長
REGARD試験1)、RAINBOW試験2)の結果より、切除不能進行・再発胃・食道胃接合部癌に対して、Ramucirumabは広く日常臨床で用いられている。今回、両試験における年齢別の有効性、安全性について、サブグループ解析の結果が報告された。
有効性に関しては、いずれの試験でも年齢にかかわらず、Ramucirumab投与群でPFS、OSともに良好であり、本体試験と同様の傾向が得られていることから、Ramucirumabは年齢にかかわらず有効と判断して良いであろう。RAINBOW試験の75歳以上の解析においてOSの生存曲線がほぼ重なっているが(中央値11.0 vs. 11.0ヵ月, HR=0.97)、発表者が指摘しているように、75歳以上の集団ではPaclitaxel単独群で原発切除歴有、アジアの症例、ECOG PSが良好な症例など、予後良好な症例が多かったことが影響しているものと考える。
また、安全性に関しては、Ramucirumab投与群において、REGARD試験では高齢になるにつれてGrade 3以上の高血圧の頻度は高い傾向であったが、RAINBOW試験ではそのような傾向は認めなかった。高齢者が必ずしも高血圧の頻度が高くなるわけではないのかもしれないが、高血圧はRamucirumab投与における頻度の高い有害事象であり、これまでと同様に定期的なモニタリングを行い、血圧上昇時は降圧剤の処方など適切な対応が必要である。
以上より、Ramucirumabの適応は年齢によって変わらないと考える。Ramucirumabに限った話ではないが、実臨床では全身状態、年齢、臓器機能、合併症といった様々な患者背景因子を総合的に考慮し、治療適応を判断することが重要であろう。
(コメント・監修:静岡県立静岡がんセンター 消化器内科 医長 山﨑 健太郎)
REGARD試験とRAINBOW試験
Ramucirumabの有効性と安全性を年齢別に検討
本研究は、REGARD試験とRAINBOW試験における、45歳以下、45歳超70歳未満、70歳以上、75歳以上の年齢別サブグループの有効性と安全性に関して報告された。OSとPFSは、Kaplan-Meier法とCox比例ハザード回帰解析が用いられ、症例数が少ないサブグループの解析をより正確に行うために、STEPP(subpopulation treatment effect pattern plot)解析によって、年齢別の有効性を評価した。
年齢分布は、SEER Cancer Statisticsでは、44歳以下6.1%、45~64歳33.1%、65~74歳25.7%、75~84歳35.1%である。一方、REGARD試験とRAINBOW試験のコホートでは、45歳以下11.2%、45~65歳未満51.9%、65~75歳未満30.1%、75歳以上6.9%であり、本研究の対象は、SEER Cancer Statisticsのデータベースと比較して45~65歳未満の分布が多かった。なお、年齢別の患者背景は、いずれの試験においても大きな偏りは認めなかった。
年齢別におけるRamucirumabの有効性
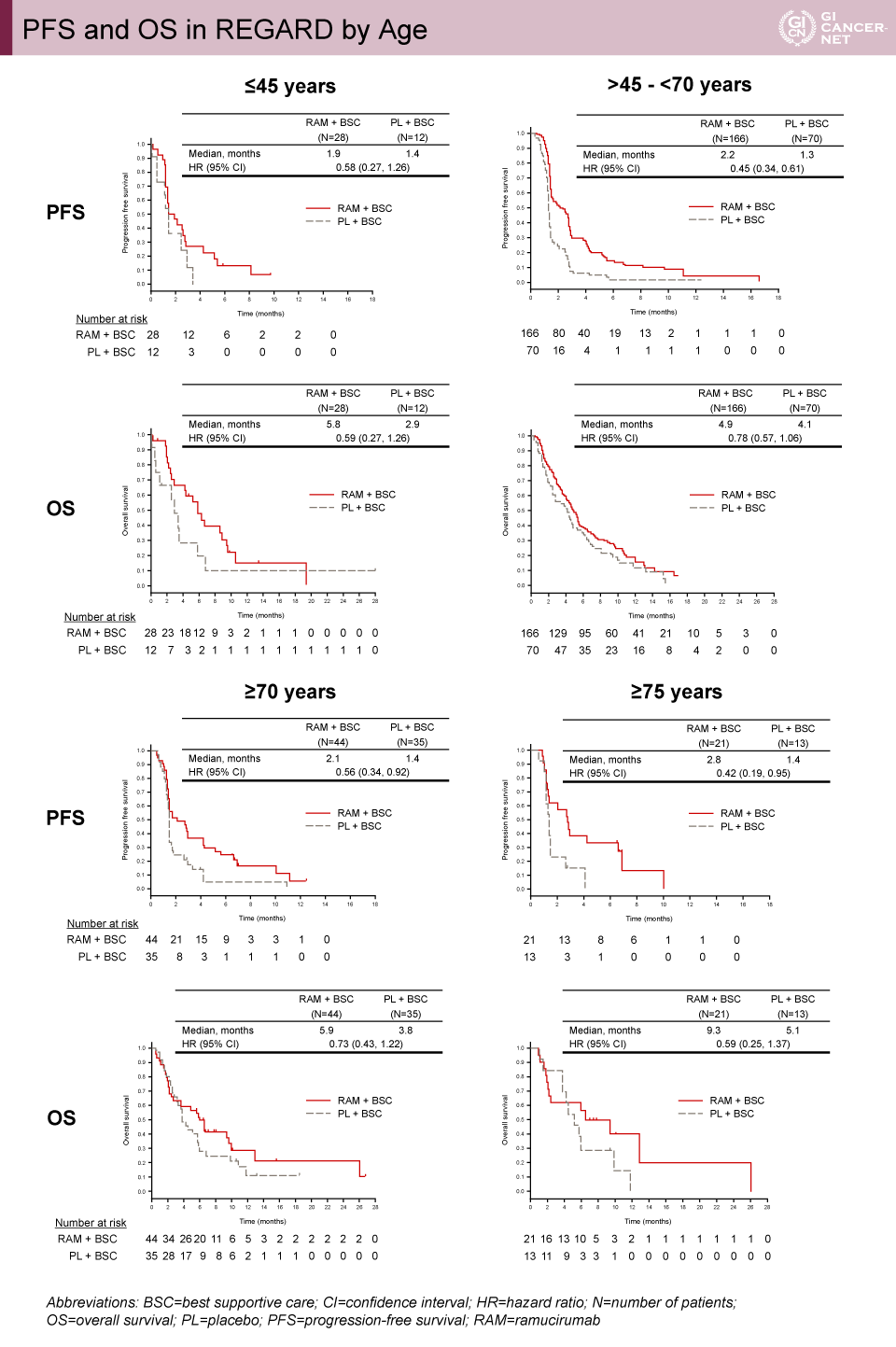
REGARD試験では、45歳以下(40例)、45歳超70歳未満(236例)、70歳以上(79例)、75歳以上(34例)が解析対象となった。Ramucirumab単剤群とプラセボ群のPFS中央値は、45歳以下1.9 vs. 1.4ヵ月(HR=0.58, 95% CI: 0.27-1.26)、45歳超70歳未満2.2 vs. 1.3ヵ月(HR=0.45, 95% CI: 0.34-0.61)、70歳以上2.1 vs. 1.4ヵ月(HR=0.56, 95% CI: 0.34-0.92)、75歳以上2.8 vs. 1.4ヵ月(HR=0.42, 95% CI: 0.19-0.95)であった(図1)。また、OS中央値は、45歳以下5.8 vs. 2.9ヵ月(HR=0.59, 95% CI: 0.27-1.26)、45歳超70歳未満4.9 vs. 4.1ヵ月(HR=0.78, 95% CI: 0.57-1.06)、70歳以上5.9 vs. 3.8ヵ月(HR=0.73, 95% CI: 0.43-1.22)、75歳以上9.3 vs. 5.1ヵ月(HR=0.59, 95% CI: 0.25-1.37)であった。
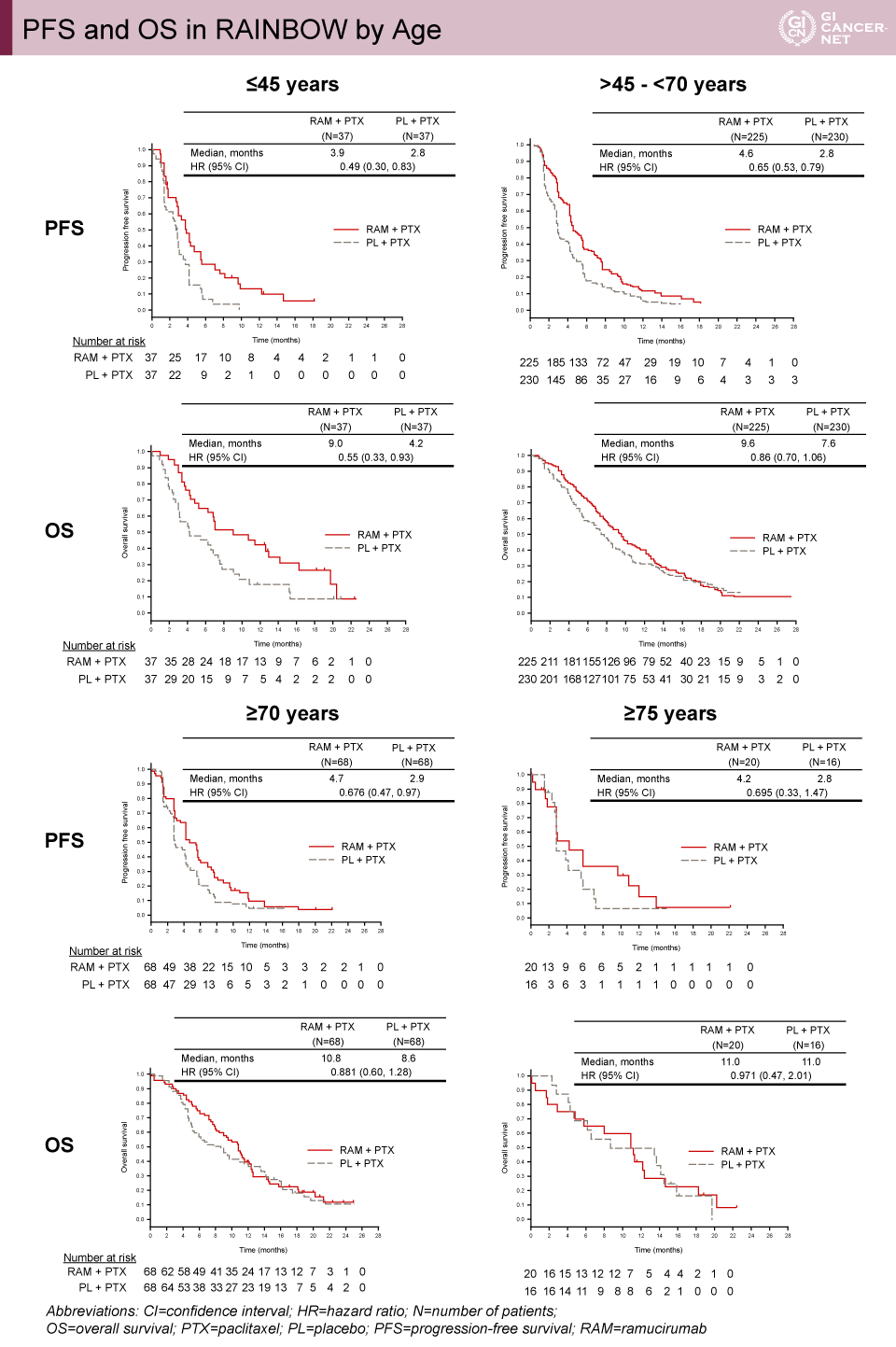
RAINBOW試験では、45歳以下(74例)、45歳超70歳未満(455例)、70歳以上(136例)、75歳以上(36例)が解析対象となった。Paclitaxel+Ramucirumab併用群とPaclitaxel単剤群のPFS中央値は、45歳以下3.9 vs. 2.8ヵ月(HR=0.49, 95% CI: 0.30-0.83)、45歳超70歳未満4.6 vs. 2.8ヵ月(HR=0.65, 95% CI: 0.53-0.79)、70歳以上4.7 vs. 2.9ヵ月(HR=0.68, 95% CI: 0.47-0.97)、75歳以上4.2 vs. 2.8ヵ月(HR=0.70, 95% CI: 0.33-1.47)であった(図2)。OS中央値は、45歳以下9.0 vs. 4.2ヵ月(HR=0.55, 95% CI: 0.33-0.93)、45歳超70歳未満9.6 vs. 7.6ヵ月(HR=0.86, 95% CI: 0.70-1.06)、70歳以上10.8 vs. 8.6ヵ月(HR=0.88, 95% CI: 0.60-1.28)、75歳以上11.0 vs. 11.0ヵ月(HR=0.97, 95% CI: 0.47-2.01)であった。
RAINBOW試験における75歳以上では、OSのハザード比が0.97とほぼ1に近い値であったが、Paclitaxel単独群において原発切除歴有、アジアの症例、ECOG PSが良好な症例など、予後良好な症例が多い傾向であった。
STEPP解析では、REGARD試験とRAINBOW試験のいずれにおいても、年齢別によるPFSとOSのハザード比に違いは認められなかった。
発表者の許可を得て掲載(approved by Kei Muro)
発表者の許可を得て掲載(approved by Kei Muro)
年齢別におけるRamucirumabの安全性とQOL
両試験ともにRamucirumab投与群では、若年者から高齢者になるにつれてgrade 3以上の有害事象の頻度が高くなる傾向があったが、有害事象は年齢にかかわらず十分に管理可能であった。Ramucirumabに関連する有害事象について、REGARD試験では、Ramucirumab投与群でgrade 3以上の高血圧の頻度が高く、若年者よりも高齢者の方がgrade 3以上の高血圧の発現頻度が高かった。一方、RAINBOW試験では、高血圧の頻度は年齢にかかわらずRamucirumab併用群で高かった。Grade 3以上の好中球減少は、Ramucirumab併用群、高齢者で頻度が高かったが、発熱性好中球減少症の頻度は70歳未満(約3%)と70歳以上(約6%)で差は認めなかった。なお、両試験ともに、年齢にかかわらず相対用量強度、投与延期、減量に差は認めず、Ramucirumab投与群では治療が長期間行われていた。
EORTC QLQ-C30(European Organization for Research and Treatment of Cancer Quality of Life [QOL] questionnaire)を用いたGlobal Health StatusによるQOL評価では、6週時点、12週時点いずれにおいても、年齢にかかわらずRamucirumab投与群でQOLが改善していた。

監修・レポーター
監修
加藤 健先生
国立がん研究センター中央病院 消化管内科 医長
レポーター
川上 武志先生
静岡県立静岡がんセンター 消化器内科 レジデント
監修
山﨑 健太郎先生
静岡県立静岡がんセンター 消化器内科 医長
レポーター
成田 有季哉先生
愛知県がんセンター中央病院 薬物療法部 専門員
監修
谷口 浩也先生
愛知県がんセンター中央病院 薬物療法部 医長
レポーター
山口 敏史先生
国立がん研究センター中央病院 消化管内科 レジデント