2017年1月19日~21日に米国サンフランシスコにて開催された2017年 消化器癌シンポジウム(2017 Gastrointestinal Cancers Symposium)より、大腸癌や胃癌などの注目演題のレポートをお届けします。演題レポートの冒頭には“Expert's view”として、臨床研究の第一線で活躍する監修ドクターのコメントを掲載しています。
大腸癌
KRAS野生型切除不能進行・再発大腸癌に対するCPT-11+Panitumumab vs. CPT-11+Cetuximab(WJOG6510G試験)
Randomized phase II study of panitumumab …
Naotoshi Sugimoto, et al.
Expert’s view

谷口 浩也先生
愛知県がんセンター中央病院 薬物療法部 医長
本結果には大変驚いた。Cetuximab(Cmab)とPanitumumab(Pmab)の単剤同士の直接比較試験(ASPECCT試験)では、両者は同等の有効性であった1)。また、切除不能進行・再発大腸癌1st-lineとしてのFOLFOX/FOLFIRI±抗EGFR抗体薬の比較試験を見ても、CmabとPmabの有効性に大きな違いがあるようには見えない。しかしながら、ASPECCT試験におけるサブグループ解析において、Bevacizumabの前治療歴のある患者集団ではPmab群がCmab群よりも良好な結果が報告されている。
本WJOG6510G試験も約97%がBevacizumab投与歴ありの患者集団であり、そう考えると、本試験はASPECCT試験のサブグループ解析の結果を再現しているとも言える。本試験は第II相試験であり、解釈は慎重にされるべきである。あくまで「Irinotecan(CPT-11)+Cmabに対するCPT-11+Pmabの非劣性が示唆された」のが主解析の結果であり、CPT-11+Cmab/Pmab両治療ともに現行どおり本対象患者の治療選択肢として考えて良いだろう。Bevacizumabの前治療が抗EGFR抗体薬の効果に与える影響については、そのメカニズムも含め、さらなる検討が必要である。
(コメント・監修:愛知県がんセンター中央病院 薬物療法部 医長 谷口 浩也)
CmabとPmabとの相違点は?
CmabおよびPmabはともにEGFRを標的とした抗体薬である。フッ化ピリミジン系製剤、Oxaliplatin(L-OHP)、CPT-11の投与歴のあるKRAS野生型の切除不能進行・再発大腸癌患者を対象にCmab単剤療法とPmab単剤療法とを比較した第III相試験(ASPECCT試験)では、両者の治療効果は同等であることが示されている1)。しかしながら、CPT-11併用時のCmabとPmabを直接比較した試験は報告されていない。
CPT-11+CmabとCPT-11+Pmabとの無作為化比較第II相試験
対象は、組織学的に腺癌と診断されておりKRAS変異を有さない(野生型)切除不能・進行再発大腸癌で、ECOG PS 0-2、前治療でフッ化ピリミジン系製剤、L-OHP、CPT-11に不応または不耐となった患者であった。対象患者は、Cmab群(Cmab: 初回投与量400mg/m², 2回目以降は250mg/m², 毎週、CPT-11: 100-150mg/m², 2週毎)とPmab群(Pmab: 6mg/kg, 2週毎、CPT-11: 100-150mg/m², 2週毎)とに1:1で無作為に割り付けられた。
主要評価項目はPFS、副次評価項目はOS、奏効率、病勢コントロール率(DCR)、安全性であった。本試験はPmab群のCmab群に対するPFSの非劣性を検証するためにデザインされ、両群の期待PFS中央値を6ヵ月とし、非劣性マージン1.3、片側α=0.2、検出力70%で、必要症例数は120例であった。
CPT-11+PmabはCPT-11+Cmabに対して非劣性を示した
2011年12月~2014年11月の間に国内31施設から121例が登録され、Cmab群60例、Pmab群61例に割り付けられた。なお、不適格だったCmab群の1例を除いた120例がFAS(Full Analysis Set)集団となった。患者背景は、Cmab群/Pmab群でそれぞれ、年齢中央値64.0歳/64.0歳、ECOG PS 0-1が98.3%/98.4%、前治療Bevacizumab使用率96.6%/96.7%であった。
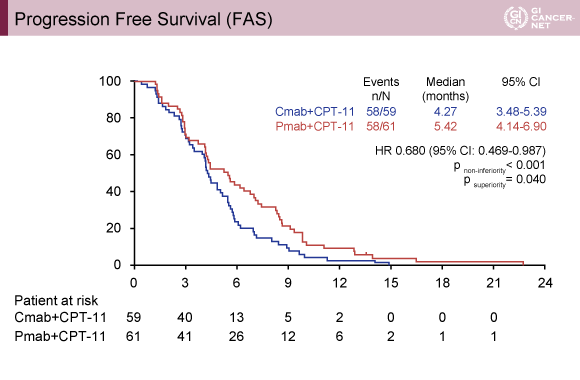
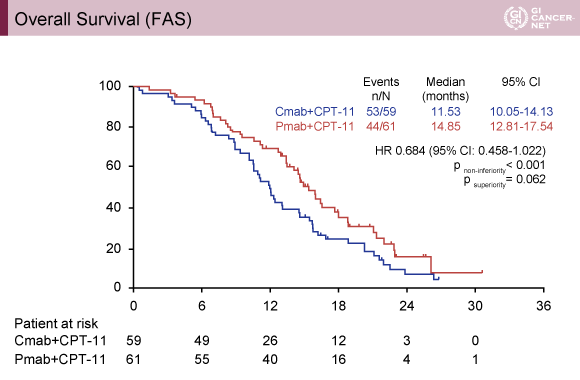
主要評価項目であるPFS中央値は、Cmab群4.27ヵ月(95% CI: 3.48-5.39)、Pmab群5.42ヵ月(95% CI: 4.14-6.90)、ハザード比は0.680(95% CI: 0.469-0.987)であり、非劣性p<0.001、優越性p=0.040とPmab群で有意に良好であった(図1)。OS中央値はCmab群11.53ヵ月(95% CI: 10.05-14.13)、Pmab群14.85ヵ月(95% CI:12.81-17.54)であり、ハザード比は0.684(95% CI: 0.458-1.022)、非劣性p<0.001、優越性p=0.062であった(図2)。また、奏効率はCmab群22.0%、Pmab群26.2%であり、有意差はみられなかった(p=0.671)。
注意すべき有害事象として、grade 3以上の白血球減少(p=0.007)、好中球減少(p=0.007)がCmab群で多く認められた。
発表者の許可を得て掲載(approved by Naotoshi Sugimoto)
発表者の許可を得て掲載(approved by Naotoshi Sugimoto)
まとめ
フッ化ピリミジン系製剤、L-OHP、CPT-11に不応または不耐のKRAS野生型切除不能・進行再発大腸癌において、CPT-11+Pmab併用療法はCPT-11+Cmab併用療法に対する非劣性が示され、優越性も示唆される結果であった。
(レポート:国立がん研究センター中央病院 消化管内科 レジデント 山口 敏史)
Reference
- 1) Price TJ, et al.: Lancet Oncol. 15(6): 569-579, 2014[PubMed]

監修・レポーター
監修
加藤 健先生
国立がん研究センター中央病院 消化管内科 医長
レポーター
川上 武志先生
静岡県立静岡がんセンター 消化器内科 レジデント
監修
山﨑 健太郎先生
静岡県立静岡がんセンター 消化器内科 医長
レポーター
成田 有季哉先生
愛知県がんセンター中央病院 薬物療法部 専門員
監修
谷口 浩也先生
愛知県がんセンター中央病院 薬物療法部 医長
レポーター
山口 敏史先生
国立がん研究センター中央病院 消化管内科 レジデント