BRAF変異型の切除不能進行・再発大腸癌に対するIrinotecan+Cetuximab療法とIrinotecan+Cetuximab+Vemurafenib療法の無作為化化第II相試験(SWOG S1406試験)
Randomized trial of Irinotecan and Cetuximab with or without Vemurafenib in BRAF-mutant metastatic colorectal cancer (SWOG S1406)
Scott Kopetz, et al.
監修コメント

加藤 健先生
国立がん研究センター中央病院 消化管内科 医長
BRAF変異大腸癌に対しては、抗EGFR抗体薬は効果がなく、メラノーマでは効果が認められたBRAF阻害剤も単独では効果が低いことが分かっている1)。その作用機序としては、BRAFの阻害により、さらに下流のERKからEGFRへのフィードバックがかかるため、BRAF阻害剤単独では効果がないとされている。そのため、BRAF阻害剤だけでなく抗EGFR抗体薬を併用することで効果が得られるのではないか?というのが今回のクエスチョンである。
本試験は、BRAF変異を有する大腸癌に対するIrinotecan+Cetuximab療法へのBRAF阻害剤Vemurafenibの上乗せ効果を検証した無作為化試験である。Vemurafenibの効果はある程度予測されたため、円滑な登録を図るために主要評価項目をPFS(progression-free survival)とし、腫瘍増大後のクロスオーバーを認めるデザインとなっている。Irinotecan+Cetuximab群の48%がクロスオーバーをした結果、OS(overall survival)では両群で有意差が出なかったが、PFSでは明らかにVemurafenibの上乗せ効果が示され、Irinotecan+Cetuximab+Vemurafenib療法はBRAF V600E変異大腸癌に対する新しい治療であると結論づけられている。
最近、同様のコンセプトで、BRAF変異型大腸癌に対するCetuximab+BRAF阻害剤Encorafenib±PI3Kα阻害剤Alpelisib併用療法の有効性、安全性を検討した第Ib相試験の結果が報告され、20%程度の奏効率と約4ヵ月のPFSが示されている2)。ただ、毒性の割にPI3Kα阻害剤の上乗せを認めなかったため、第III相試験であるBEACON試験では、Irinotecan/FOLFIRI+CetuximabとCetuximab+Encorafenib±MEK阻害剤Binimetinib併用療法の3アーム比較により行われている3)。
本試験におけるハザード比0.48という結果を見ると、BRAF阻害剤の有効性は確かであり、予後不良なBRAF変異型大腸癌に対するEGFRとRAFの同時阻害は有効であると考えられた。今後の日常診療において、化学療法適応大腸癌患者に対してはRAS変異、マイクロサテライト不安定性(MSI)とともにBRAF変異も検査する時代が来ると思われる。
(コメント・監修:国立がん研究センター中央病院 消化管内科 医長 加藤 健)
BRAF V600E変異型大腸癌に対する治療戦略
BRAF V600E遺伝子変異を有する患者は切除不能進行・再発大腸癌の7%に認められるが、標準的な化学療法の効果が乏しく、予後不良である4)。また、BRAF V600E変異型大腸癌患者に対するBRAF阻害剤Vemurafenib単独療法の効果は限定的であり、奏効率はわずか5%である1)。BRAF阻害剤への耐性機序としては、MAPK経路におけるBRAFの上流にあたるEGFRの再活性化が考えられており、BRAF阻害剤とEGFR阻害剤の併用療法は、この耐性を克服して単独療法よりも高い抗腫瘍効果を示すことが示されている。また基礎研究では、さらにIrinotecanを併用することで抗腫瘍効果が高まることが示されている5)。
今回、BRAF V600E変異型大腸癌に対し、Irinotecan+Cetuximab(IC)療法とIrinotecan+Cetuximab+Vemurafenib(VIC)療法を比較する無作為化第II相試験(SWOG S1406試験)の結果が報告された。
IC療法へのVemurafenibの上乗せ効果を検討
対象は、BRAF V600E変異型かつRAS野生型で1または2レジメンの前治療歴を有し、ECOG PS 0/1の切除不能進行・再発大腸癌患者であり、抗EGFR抗体薬、BRAF阻害剤、MEK阻害剤の投与歴のある患者は除外された。対象患者は、IC群(Irinotecan: 180mg/m2、Cetuximab: 500mg/m2、2週毎)とVIC群(Irinotecan・Cetuximab: IC群と同様、Vemurafenib: 960mg, 1日2回連日内服)に1:1で割り付けられた。なお、層別因子としてIrinotecanの前治療歴の有無が用いられ、IC群では増悪後のVIC療法へのクロスオーバーが許容された。
主要評価項目はPFSであり、副次的評価項目は安全性、OS、奏効率であった。PFSにおけるIC群に対するVIC群のハザード比を0.5と期待し(中央値: IC群2.4ヵ月 vs. VIC群4.8ヵ月)、両側α=5%、検出力90%で、必要症例数は94例、目標症例数は105例に設定された。
主要評価項目のPFSにおいて、VIC群が有意に良好
106例が登録され、7例の不適格例を除く99例(IC群50例、VIC群49例)が解析対象となった。患者背景(IC群/VIC群)は、年齢中央値62歳/60歳、女性74%/43%、ECOG PS 0が46%/49%、Irinotecanの前治療歴ありが38%/41%、前治療歴2レジメンが34%/39%であった。
主要評価項目であるPFSの中央値は、IC群2.0ヵ月、VIC群4.3ヵ月であり(HR=0.48, 95% CI: 0.31-0.75, p=0.001)、VIC群で有意に良好であった(図1)。
図1
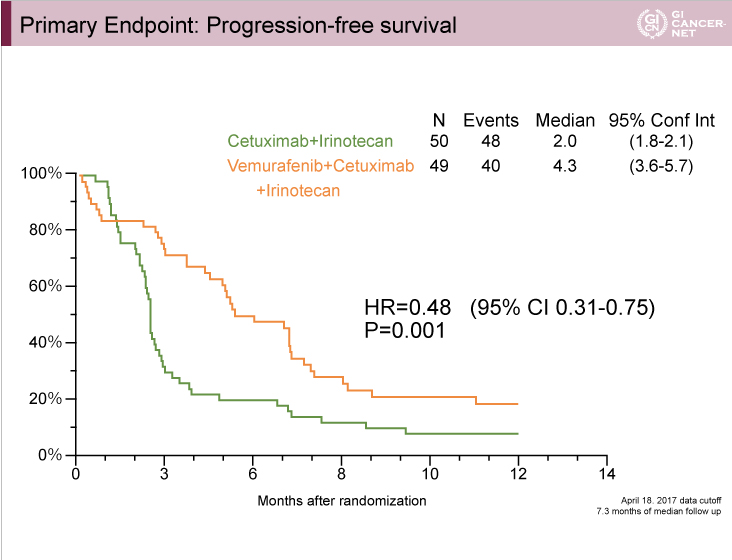
発表者の許可を得て掲載(approved by Scott Kopetz)
奏効率は、IC群4%、VIC群16%であった(p=0.001)(図2)。また、病勢コントロール割合(DCR)は、IC群:22%、VIC群:67%であった。
図2
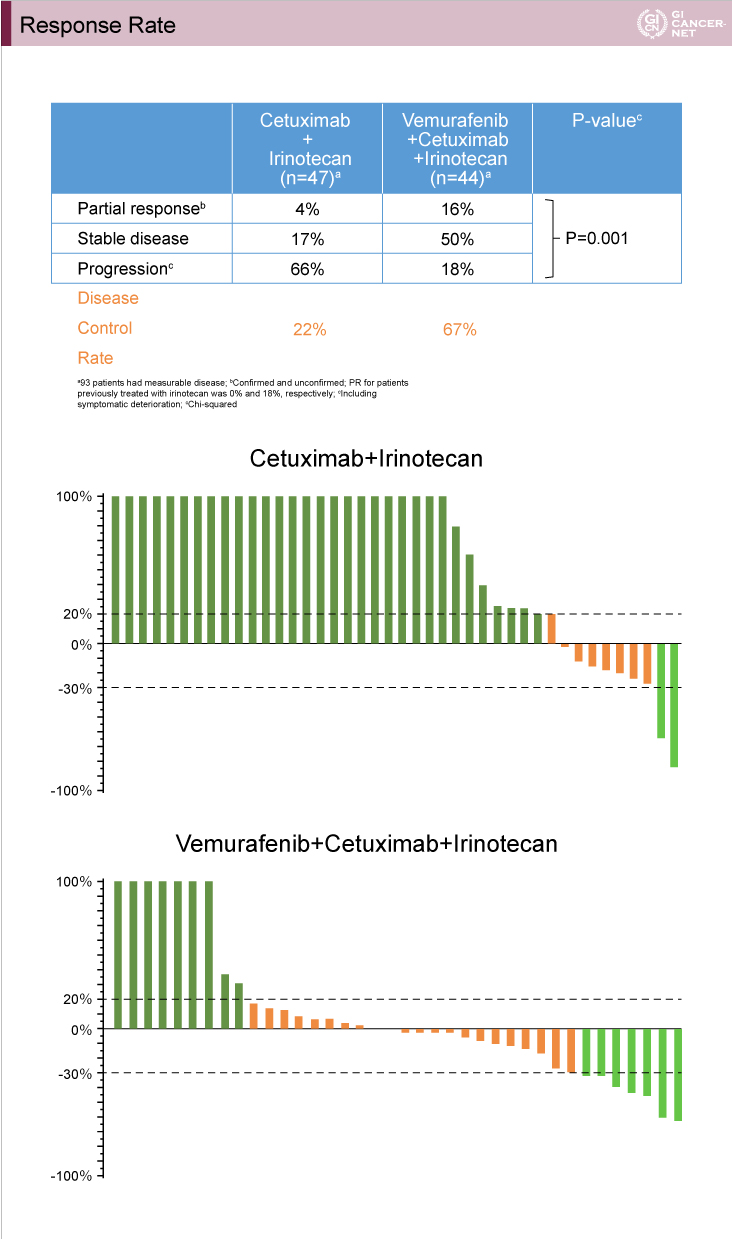
発表者の許可を得て掲載(approved by Scott Kopetz)
PFSにおけるサブグループ解析では、Irinotecanの前治療歴(有/無)、原発巣の部位(右/左)、マイクロサテライト状況(MSS/MSI-H)、PIK3CA変異状況(野生型/変異型)のいずれのサブグループにおいてもVIC群で良好であった。OSの中央値はIC群5.9ヵ月、VIC群9.6ヵ月であった(HR=0.73, 95% CI: 0.45-1.17, p=0.19)。なお、IC群ではクロスオーバーが許容されており、24例(48%)は画像上PDが確認された後にVIC療法が施行されたが、クロスオーバー後においてもPFS中央値5.8ヵ月、OS中央値12.1ヵ月、奏効率17%、病勢コントロール率72%と、VIC療法の効果を認めた。
Grade 3/4の有害事象(IC群/VIC群)は、貧血(0%/13%)、好中球減少(7%/33%)、悪心(2%/20%)をVIC群で多く認めたが、その他は両群で同程度であった(表)。なお、有害事象による治療中止は6%/16%であった。
表
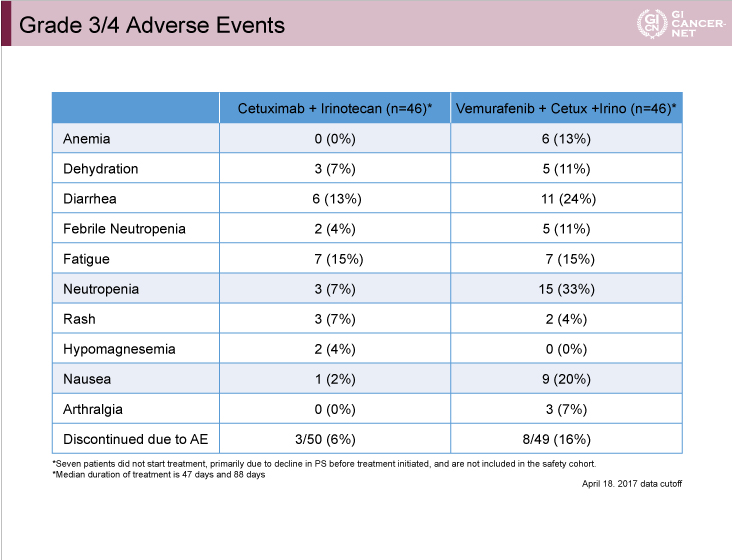
発表者の許可を得て掲載(approved by Scott Kopetz)
まとめ
BRAF V600E変異型の切除不能進行・再発大腸癌に対し、VemurafenibはIC療法への有意なPFSの上乗せ効果を示した。
(レポート:聖マリアンナ医科大学 臨床腫瘍学 診療助手 新井 裕之)
References
1) Kopetz S, et al.: J Clin Oncol. 33(34): 4032-4038, 2015[PubMed]
2) van Geel RMJM, et al.: Cancer Discov. 7(6): 610-619, 2017[PubMed]
3) Study of Encorafenib + Cetuximab Plus or Minus Binimetinib vs. Irinotecan/Cetuximab or Infusional 5-Fluorouracil (5-FU)/Folinic Acid (FA)/Irinotecan (FOLFIRI)/Cetuximab With a Safety Lead-in of Encorafenib + Binimetinib + Cetuximab in Patients With BRAF V600E-mutant Metastatic Colorectal Cancer (BEACON CRC) [CT.gov]
4) Morris V, et al.: Clin Colorectal Cancer. 13(3): 164-171, 2014[PubMed]
5) Hong DS, et al.: Cancer Discov. 6(12): 1352-1365, 2016[PubMed]
関連リンク
BRAF V600変異型大腸癌に対するBRAF阻害剤Encorafenib(LGX818)+Cetuximab ± PI3K阻害剤BYL719(GSK212)併用療法の臨床第I相試験[学会レポート]

監修
谷口 浩也先生
愛知県がんセンター中央病院
薬物療法部 医長
加藤 健先生
国立がん研究センター中央病院 消化管内科 医長
山﨑 健太郎先生
静岡県立静岡がんセンター
消化器内科 医長
レポーター (50音順)
新井 裕之先生
聖マリアンナ医科大学
臨床腫瘍学 診療助手
川上 尚人先生
近畿大学医学部
内科学腫瘍内科部門 医学部講師
中島 雄一郎先生
九州大学大学院
消化器・総合外科 助教
成田 有季哉先生
愛知県がんセンター中央病院
薬物療法部 医長
宮本 敬大先生
国立がん研究センター中央病院
消化管内科 がん専門修練医
山田 武史先生
筑波大学附属病院
消化器内科 病院講師