治療歴のある切除不能食道/食道胃接合部/胃癌患者に対するNivolumab単剤またはNivolumab+Ipilimumab併用療法(CheckMate 032試験)
Nivolumab±Ipilimumab in patients with advanced/metastatic chemotherapy-refractory gastric, esophageal, or gastroesophageal junction cancer: CheckMate 032 study
Yelena Y. Janjigian, et al.
監修コメント

山﨑 健太郎先生
静岡県立静岡がんセンター 消化器内科 医長
CheckMate 032試験は、2016年の米国消化器癌シンポジウム1)および米国臨床腫瘍学会年次集会2)において中間報告が行われ、治療歴のある食道/食道胃接合部/胃癌患者に対してNivolumab単剤とNivolumab+Ipilimumab併用療法は有望な結果を示していた。今回は、そのupdate解析の結果が報告された。
Nivolumab単剤のコホートに関しては、奏効率12%、1年OS割合39%であり、アジアの症例で行われたATTRACTION-2試験と同様の結果3)であった。ディスカッサントが指摘していたように、PembrolizumabのKEYNOTE-012試験4)でもアジアと欧米の症例で効果に違いは認められなかったことから、胃癌における免疫チェックポイント阻害剤の有効性は人種による差はないと考えられる。
NivolumabとIpilimumabの併用療法に関しては、Nivolumab 1mg/kg+Ipilimumab 3mg/kg群において、Nivolumab単剤群よりも奏効率が高い傾向(24% vs. 12%)であったものの、PFS(progression-free survival)、OS(overall survival)では大きな差は認められなかった。一方で有害事象は、悪性黒色腫における報告5)と同様、Nivolumab+Ipilimumab併用群で頻度が高く、注意が必要である。
Nivolumabに関しては、本邦でも2017年秋頃には保険診療として胃癌の実臨床で用いることが可能になると予想される。しかし、他癌種と比較し胃癌における奏効率やPFSなど有効性の点で見劣りすることは否めない。今後、本薬剤の恩恵を受けることができる対象を絞り込むためのバイオマーカーの探索が必要であり、また耐性克服やさらなる有効性の向上へ向けた併用療法の開発が必要である。
現在、NivolumabとIpilimumabまたは殺細胞性抗癌剤との併用に関しては、胃癌初回化学療法において、Nivolumab+Ipilimumab群、XELOX/FOLFOX群、XELOX/FOLFOX+Nivolumab群の3群を比較する第III相臨床試験が進行中であり(CheckMate 649試験)6)、その結果が待たれる。
(コメント・監修:静岡県立静岡がんセンター 消化器内科 医長 山﨑 健太郎)
食道胃接合部/胃癌における免疫チェックポイント阻害剤
ATTRACTION-2試験では、アジア人の3rd line以降の食道胃接合部/胃癌患者に対するNivolumabの有用性が認められている3)。CheckMate 032試験は、治療歴のある食道/食道胃接合部/胃癌に対するNivolumab単剤とNivolumab+Ipilimumab併用療法の有効性と安全性を評価する第II相試験であり、今回はそのupdate解析が報告された。
Nivolumab単剤またはNivolumab+Ipilimumab併用療法のマルチコホート試験
本試験は、NIVO3群(Nivolumab: 3mg/kg, q2weeks)、NIVO1+IPI3群(Nivolumab: 1mg/kg+Ipilimumab: 3mg/kg, q3weeks, 4サイクル以降はNivolumab: 3mg/kg, q2weeks)、NIVO3+IPI1群(Nivolumab: 3mg/kg+Ipilimumab: 1mg/kg, q3weeks, 4サイクル以降はNivolumab: 3mg/kg, q2weeks)の3つの治療コホートで構成されていた。主要評価項目は、RECIST ver.1.1における奏効率であり、副次評価項目は、OS、PFS、TTR(time to response)、DOR(duration of response)、安全性であった。また、探索的評価項目として、Dako 28-8 pharmDx assayを用いた腫瘍細胞のPD-L1発現の評価を行った。
PD-L1発現の有無にかかわらずNivolumab群、Nivolumab+Ipilimumab併用群ともに有効
160例が登録され、各コホートはNIVO3群59例、NIVO1+IPI3群49例、NIVO3+IPI1群52例であった。患者背景はそれぞれ、年齢中央値60歳/53歳/58歳、男性76%/69%/87%、原発巣(胃)が32%/45%/35%、前治療レジメン数(3レジメン以上)が49%/46%/38%であった。本解析時点で試験治療を中止している症例は、NIVO3群97%、NIVO1+IPI3群88%、NIVO3+IPI1群94%であり、その理由の内訳はそれぞれ、病勢進行85%、51%、73%、試験薬関連有害事象が3%、18%、13%であった。
主要評価項目である奏効率は、NIVO3群12%(95% CI: 5-23)、NIVO1+IPI3群24%(95% CI: 13-39)、NIVO3+IPI1群8%(95% CI: 2-19)であった。また、TTR中央値はそれぞれ1.6ヵ月(範囲: 1.2-4.0)、2.7ヵ月(範囲: 1.2-14.5)、2.6ヵ月(範囲: 1.3-2.8)であり、DOR中央値はそれぞれ7.1ヵ月(95% CI: 3.0-13.2)、7.9ヵ月(95% CI: 2.8-NE)、未到達(95% CI: 2.5-NE)であった。なお、PD-L1発現の有無によって、奏効率に違いは認められなかった。
PFS中央値は、NIVO3群1.4ヵ月(95% CI: 1.2-2.5)、NIVO1+IPI3群1.4ヵ月(95% CI: 1.2-3.8)、NIVO3+IPI1群1.6ヵ月(95% CI: 1.4-2.6)であった(図1)。
図1
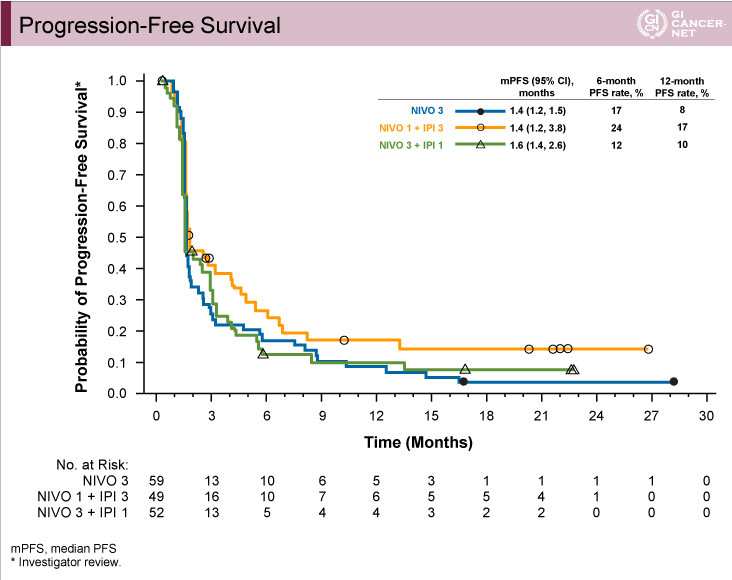
発表者の許可を得て掲載(approved by Yelena Y. Janjigian)
OS中央値は、NIVO3群6.2ヵ月(95% CI: 3.4-12.4)、NIVO1+IPI3群6.9ヵ月(95% CI: 3.7-11.5)、NIVO3+IPI1群4.8ヵ月(95% CI: 3.0-8.4)であり、1年OS割合はそれぞれ39%、35%、24%であった(図2)。なお、PD-L1発現別の1年OS割合は、PD-L1陽性がそれぞれ34%、50%、23%、PD-L1陰性例がそれぞれ45%、32%、25%であった(表)。
図2
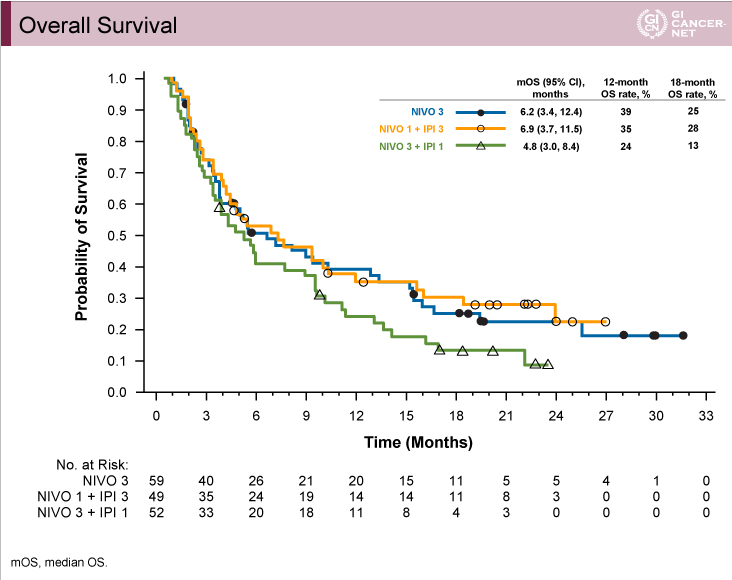
発表者の許可を得て掲載(approved by Yelena Y. Janjigian)
表
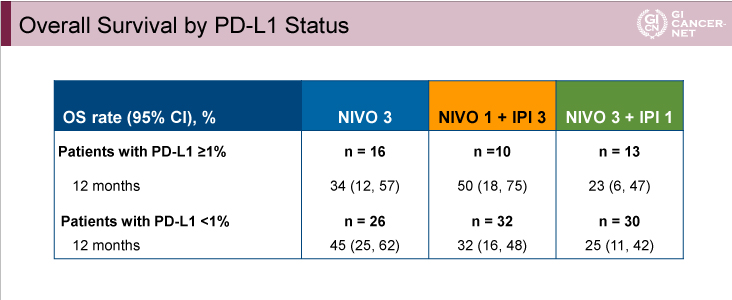
発表者の許可を得て掲載(approved by Yelena Y. Janjigian)
有害事象
NIVO3群、NIVO1+IPI3群、NIVO3+IPI1群におけるgrade 3/4の治療関連有害事象は、全体で17%/47%/27%、ALT上昇3%/14%/4%、AST上昇5%/10%/2%、下痢2%/14%/2%、疲労2%/6%/0%、そう痒症0%/2%/0%に認められ、治療中止の原因となる治療関連有害事象は3%/20%/10%に認められた。
まとめ
治療歴のある食道/食道胃接合部/胃癌において、Nivolumab単剤とNivolumab+Ipilimumab併用療法は、PD-L1発現の有無にかかわらず有用である可能性が示唆された。
(レポート:愛知県がんセンター中央病院 薬物療法部 医長 成田 有季哉)
Refereces
1) Le DT, et al.: 2016 Gastrointestinal Cancers Symposium: abstr #6
2) Janjigian YY, et al.: 2016 Annual Meeting of American Society of Clinical Oncology®: abstr #4010
3) Kang YK, et al.: 2016 Gastrointestinal Cancers Symposium: abstr #2[学会レポート]
4) Muro K, et al.: Lancet Oncol. 17(6): 717-726, 2016[PubMed]
5) Larkin J, et al.: N Engl J Med. 373(1): 23-34, 2015[PubMed]
6) Efficacy Study of Nivolumab Plus Ipilimumab or Nivolumab Plus Chemotherapy Against Chemotherapy in Stomach Cancer or Stomach/Esophagus Junction Cancer (CheckMate649)[CT.gov]

監修
谷口 浩也先生
愛知県がんセンター中央病院
薬物療法部 医長
加藤 健先生
国立がん研究センター中央病院 消化管内科 医長
山﨑 健太郎先生
静岡県立静岡がんセンター
消化器内科 医長
レポーター (50音順)
新井 裕之先生
聖マリアンナ医科大学
臨床腫瘍学 診療助手
川上 尚人先生
近畿大学医学部
内科学腫瘍内科部門 医学部講師
中島 雄一郎先生
九州大学大学院
消化器・総合外科 助教
成田 有季哉先生
愛知県がんセンター中央病院
薬物療法部 医長
宮本 敬大先生
国立がん研究センター中央病院
消化管内科 がん専門修練医
山田 武史先生
筑波大学附属病院
消化器内科 病院講師