HER2陽性胃癌に対するTrastuzumab+S-1+Oxaliplatin併用療法の第II相臨床試験(KSCC/HGCSG/CCOG/PerSeUS1501B試験)
A phase II study (KSCC/HGCSG/CCOG/PerSeUS1501B) of trastuzumab plus S-1 and oxaliplatin for HER2-positive advanced gastric cancer
Katsunori Shinozaki, et al.
監修コメント

谷口 浩也先生
愛知県がんセンター中央病院 薬物療法部 医長
切除不能HER2陰性胃癌に対する初回治療は、G-SOX試験1)の結果を受けて、従来のSP療法(S-1+Cisplatin)から、消化器毒性が低く外来投与が可能なSOX療法(S-1+Oxaliplatin)にシフトしてきている。本試験はHER2陽性胃癌に対してSOX療法とTrastuzumabの併用における安全性と有効性を示した初の臨床試験であり、その臨床的意義は大きい。
本試験の主要評価項目は中央画像判定で評価された奏効割合であったが、82%と非常に良好な結果が得られている。HER2陽性胃癌に対するこれまでの臨床試験における奏効割合は、ToGA試験47%2)、HERBIS-1試験68%3)、WJOG7212G試験61%4)と報告されており、これらと比較しても本試験の奏効割合は高い傾向にある。本試験では、HER2 IHC3+の症例が87%と多くを占めていたことが関与しているのかもしれない。一方、本試験からSOX130療法(S-1+Oxaliplatin 130mg/m2)の有害事象も忍容可能であることが示されたが、減量中止割合やRDI(relative dose intensity)のデータは本発表には含まれていなかったため、PFS、OSを含め今後の報告を待ちたい。いずれにしろ、本発表から、HER-SOX130療法(SOX130+Trastuzumab)は、HER2陽性胃癌に対する治療選択肢の1つと言って良いと考える。
(愛知県がんセンター中央病院 薬物療法部 医長 谷口 浩也)
HER2陽性胃癌に対するHER-SOX130療法を評価
ToGA試験1)の結果から、HER2陽性胃癌に対してはCapecitabine+Cisplatin+Trastuzumab療法が標準治療とされており、S-1+Cisplatin+Trastuzumab療法の有用性も第II相試験において示されている2,3)。一方、S-1+Oxaliplatin 100mg/m2(SOX100)療法は第III相臨床試験においてS-1+Cisplatin療法と同程度の有効性が示されており4)、HER2陰性胃癌に対する標準治療の1つとされている。また、大腸癌においては130mg/m2のOxaliplatinとS-1を併用したSOX130療法5)が用いられている。
本試験は、未治療のHER2陽性胃癌に対するSOX130とTrastuzumabの併用療法(HER-SOX130)の有効性と安全性の評価のために計画された、単アームの多施設共同第II相試験である。
主要評価項目は中央画像判定による奏効割合
対象は、IHC3+、またはIHC2+かつFISH陽性で定義されるHER2陽性の胃腺癌患者であり、測定可能病変を有する切除不能進行・再発例であった。治療方法は、S-1(80~120mg)を1日2回に分けて2週間内服後1週間休薬し、day 1にOxaliplatin(130mg/m2)とTrastuzumab(初回8mg/kg、以後6mg/kg)を3週毎に繰り返し投与された。
主要評価項目は中央画像判定で確認された奏効割合であり、副次評価項目は安全性、PFS(progression-free survival)、OS(overall survival)、TTF(time to treatment failure)、治療期間、TFS(time to failure of strategy)、用量強度であった。奏効割合の閾値を50%、期待値を70%として、片側α=0.05、β=0.2で10%の脱落を見込み、必要症例数は40例に設定された。
奏効割合82.1%を認める
2015年6月~2016年5月の間に本邦の27施設より42例が登録され(ITT)、適格基準を満たさなかった3例を除いた39例がFASとされた。主な患者背景を表1に示す。FASの年齢中央値は66歳、男性31例(79.5%)であり、HER2ステータスはIHC3+ 34例(87.2%)、IHC2+かつFISH陽性5例(12.8%)であった。
表1
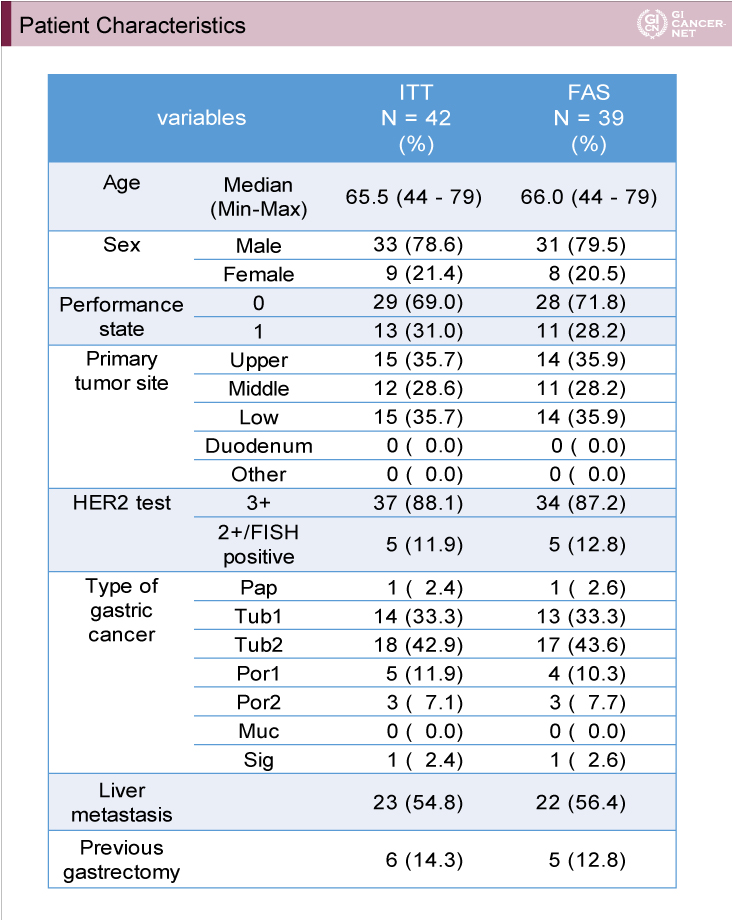
発表者の許可を得て掲載(approved by Katsunori Shinozaki)
FASの39例中9例でCR、23例でPRが得られ、主要評価項目の奏効割合は82.1%(95% CI: 67.3-91.0)であった。また、病勢コントロール率は87.2%(95% CI: 73.3-94.4)であった(図)。
図
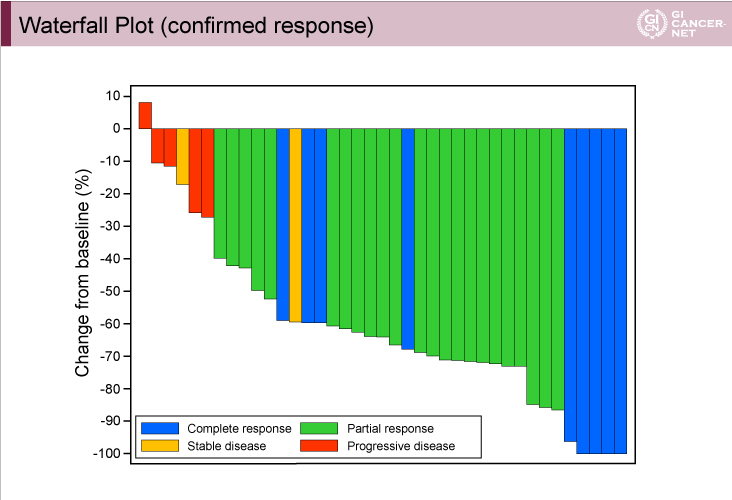
発表者の許可を得て掲載(approved by Katsunori Shinozaki)
主な有害事象を表2に示す。Grade 3/4の血液毒性は、血小板減少7例(17.9%)、好中球減少5例(12.8%)、貧血4例(10.3%)に認められたが、発熱性好中球減少症は認められなかった。また、grade 3/4の非血液毒性は、食欲不振7例(17.9%)、低ナトリウム血症4例(10.3%)、悪心および下痢が3例(7.7%)ずつに認められた。なお、末梢神経障害はgrade 3の2例(5.1%)を含め全gradeで32例(82.1%)に認められた。
表2
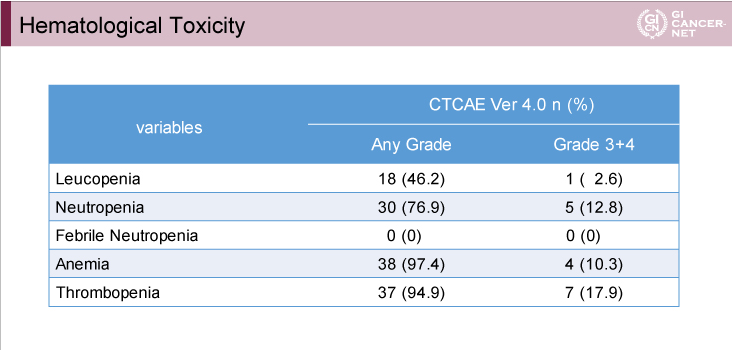
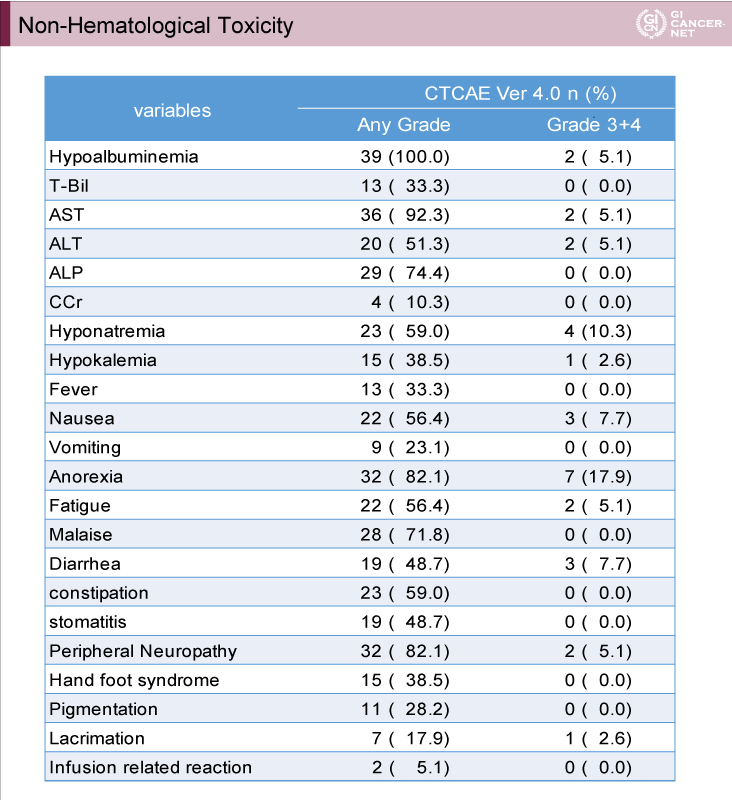
発表者の許可を得て掲載(approved by Katsunori Shinozaki)
まとめ
HER2陽性胃癌に対する初回治療としてのSOX130+Trastuzumab併用療法は忍容可能であり、高い奏効率が示された。
(レポート:筑波大学附属病院 消化器内科 病院講師 山田 武史)
References
1) Yamada Y, et al.: Ann Oncol. 26(1): 141-148, 2015[PubMed][論文紹介]
2) Bang YJ, et al.: Lancet. 376(9742): 687-697, 2010[PubMed][論文紹介]
3) Kurokawa Y, et al.: Br J Cancer. 110(5): 1163-1168, 2014[PubMed]
4) Miura Y, et al.: Gastric Cancer. 2017[Epub ahead of print][PubMed]
5) Yamada Y, et al.: Lancet Oncol. 14(13): 1278-1286, 2013[PubMed][論文紹介]

監修
谷口 浩也先生
愛知県がんセンター中央病院
薬物療法部 医長
加藤 健先生
国立がん研究センター中央病院 消化管内科 医長
山﨑 健太郎先生
静岡県立静岡がんセンター
消化器内科 医長
レポーター (50音順)
新井 裕之先生
聖マリアンナ医科大学
臨床腫瘍学 診療助手
川上 尚人先生
近畿大学医学部
内科学腫瘍内科部門 医学部講師
中島 雄一郎先生
九州大学大学院
消化器・総合外科 助教
成田 有季哉先生
愛知県がんセンター中央病院
薬物療法部 医長
宮本 敬大先生
国立がん研究センター中央病院
消化管内科 がん専門修練医
山田 武史先生
筑波大学附属病院
消化器内科 病院講師