局所進行切除不能膵癌に対するGemcitabine+nab-Paclitaxel療法にヒト型抗CTGFモノクローナル抗体Pamrevlumabを上乗せし、有効性と切除率を検討した無作為化第I/II相試験
Effect of anti-CTGF human recombinant monoclonal antibody pamrevlumab on resectability and resection rate when combined with gemcitabine/nab-paclitaxel in phase 1/2 clinical study for the treatment of locally advanced pancreatic cancer patients
Vincent J. Picozzi, et al.
監修コメント

上野 誠先生
神奈川県立がんセンター
消化器内科 医長
Gemcitabine+Nab-Paclitaxel療法が遠隔転移を有する膵癌(以下、遠隔転移膵癌)の標準治療と確立されて以後、さらなる治療開発として、新たな薬剤を追加する3剤併用療法が注目されている。骨髄抑制の観点から従来の殺細胞薬の追加は難しく、分子標的薬が追加されることが多い。Pamrevlumabは、結合組織増殖因子(CTGF)に対する抗体であり、組織の線維化を抑制することが期待される。膵癌における化学療法抵抗性の原因として、膵線維化による間質圧の増強、薬剤分布の低下が考えられており、線維化の抑制により薬剤分布の改善が期待される。同様の概念として組織のヒアルロン酸を改善するPEGPH20という薬剤が注目され、遠隔転移膵癌での第III相試験が行われている。
今回のPamrevlumabにおいても類似の機序が期待されるが、その機序の証明としては、切除検体での線維化の変化を確認したい。また本試験の結果として切除率が向上したことから、ある一定の抗腫瘍効果はあると思われるが、その効果を遠隔転移膵癌で予後の延長として期待するのか、あるいは、本試験のように局所進行切除不能膵癌における切除率の向上を期待するのか、興味深いところである。次相試験が、今回と同様に局所進行切除不能膵癌の開発として行われるのか、遠隔転移膵癌で行われるのかに注目したい。
(コメント・監修:神奈川県立がんセンター 消化器内科 医長 上野 誠)
膵癌に対する抗CTGFモノクローナル抗体の可能性
膵癌は、結合組織増殖因子(CTGF)を過剰に発現させて細胞外マトリックスを大量に産生し、高度な線維化を形成する。Pamrevlumab(FG-3019)はCTGFに対するヒト型モノクローナル抗体であり、CTGFの過剰発現を阻害することにより抗線維化作用を有する。線維化の阻害は、薬物動態の観点から抗腫瘍効果を発揮する可能性があり、局所進行切除不能膵癌での切除可能性を高める可能性があると考えられた1,2)。本試験では、局所進行切除不能膵管癌患者に対して、Gemcitabine+nab-Paclitaxel療法にPamrevlumabを併用した際の安全性、忍容性、有効性が検討された。
Gemcitabine+nab-Paclitaxel療法にPamrevlumabを併用した無作為化第I/II相試験
本試験の対象は、NCCNガイドライン2014(NCCN)に基づき診断された切除不能局所進行膵癌で、測定可能病変を有する、ECOG PS(performance status) 0/1の未治療患者である。Gemcitabine+nab-Paclitaxel療法にPamrevlumabを併用するA群と、Gemcitabine+nab-Paclitaxel療法のB群に、2:1の割合で無作為に割り付けられた。28日間を1サイクルとして、6サイクルがプロトコール治療とされ、治療終了時に、CA19-9の50%以上低下、PET検査でSUVmaxが30%以上低下、RECIST ver1.1に基づく部分奏効(PR)または完全奏功(CR)、NCCNガイドラインに基づいた診断が切除可能あるいは切除可能境界である、のいずれかを満たす患者を切除適応とあらかじめ定義された(図1)。
図1 Study Design(発表者の許可を得て掲載)
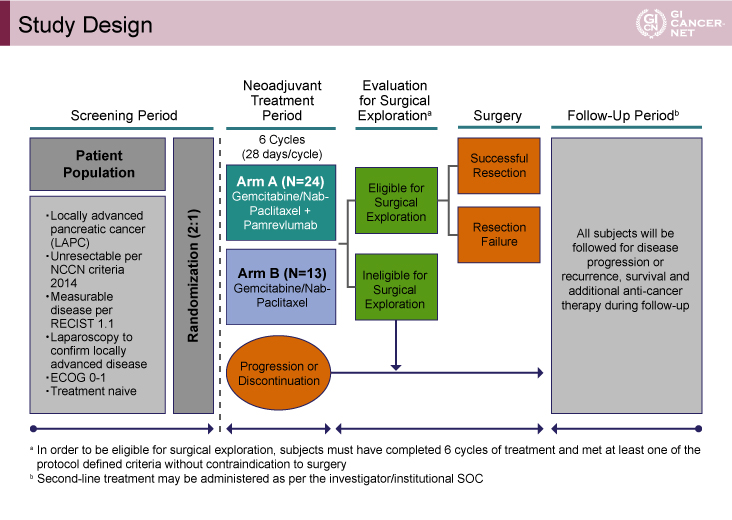
安全性評価項目は有害事象、有効性評価項目は、切除適応患者の割合、R0切除率、全生存(OS)期間の中央値(MST)などであった。
Pamrevlumab併用群における切除率が高かった
Pamrevlumabを併用するA群に24例、Gemcitabine+nab-Paclitaxel療法のB群に13例が組み入れられた。群間比較は示されなかったものの、両群間の患者背景で大きな差異は認められなかった。
重篤な有害事象は、A群9/24例(37.5%)、B群6/13例(46.2%)に認められたが、複数例で認められた事象はB群の2例にみられた胆管炎、敗血症のみであった。
A群の18/24例(75.0%)が6サイクルの治療を完遂し、17/24例(70.8%)が切除適応と判断された。切除適応と判断された17例中、手術拒否1例、手術中止4例(門脈血栓症1例、医学的理由3例)、切除未実施4例(遠隔転移3例、過度のSMA侵襲1例)を除く8/24例(33.3%)で切除が行われた。一方、B群の7/13例(53.8%)が6サイクルの治療を完遂し、2/13例(15.4%)が切除適応と判断されたが、うち1例が血管侵襲で切除未実施となり、最終的に1/13例(7.7%)で切除が行われた(図2)。
図2 Surgical Eligibility and Resection(発表者の許可を得て掲載)
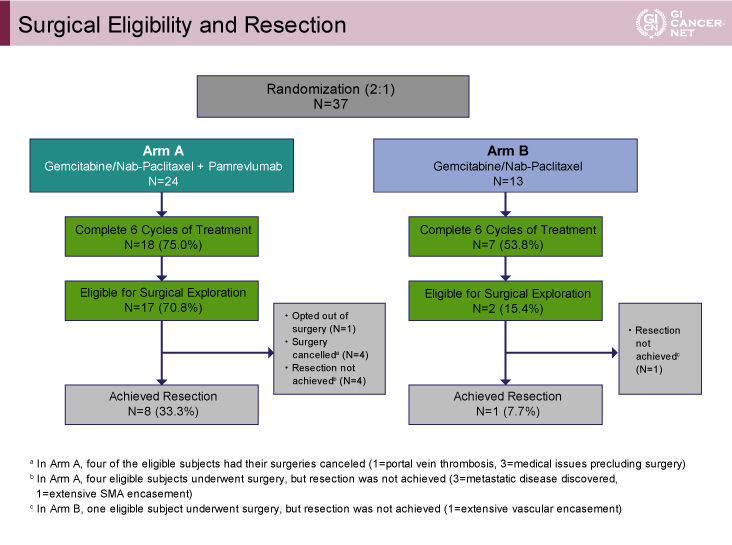
全症例で切除が行われた9/37例(24.3%)のうち、治療終了時にNCCNガイドラインに基づき切除可能あるいは切除可能境界と診断された患者はA群の1例のみであった。また、RECIST ver1.1に基づくPRまたはCRと診断された患者はA群の2例で、7例はCA19-9またはSUVmaxの低下に基づき切除適応と判断された。R0切除は5例、R1切除は4例であった。
切除適応と判断された19例(A群17例、B群2例)のOS期間中央値は27.73ヵ月、切除が行われた9例のOS期間は未到達であった(図3)。
図3 Overall Survival by Surgical Eligibility and Resection(ITT)(発表者の許可を得て掲載)
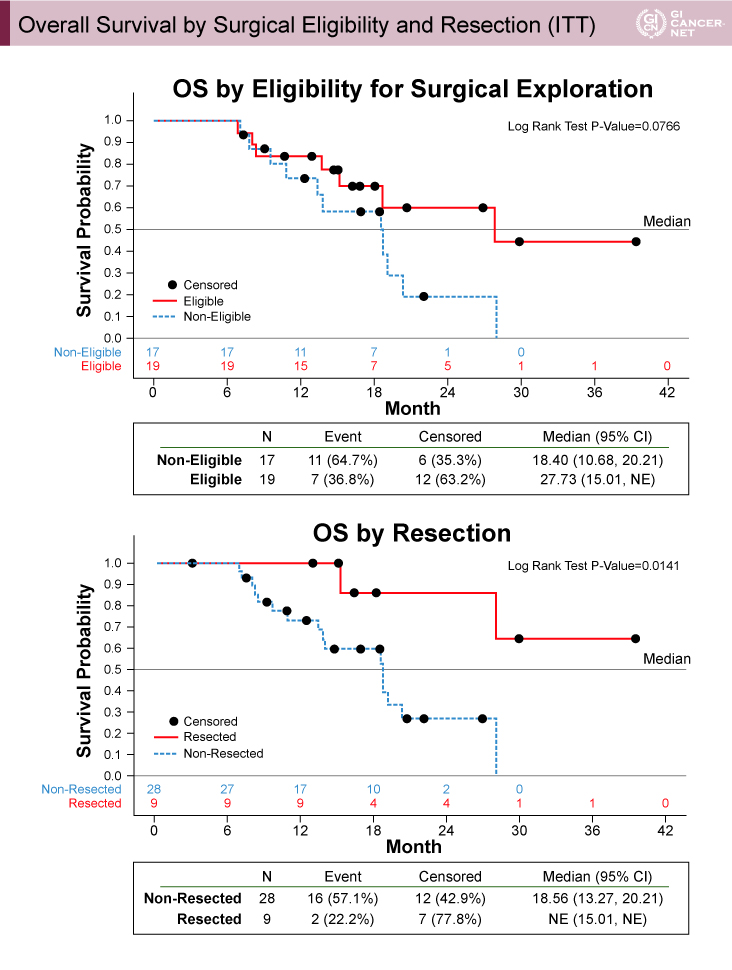
まとめ
局所進行切除不能膵癌患者に対するGemcitabine+nab-Paclitaxel+Pamrevlumabの3剤併用投与の忍容性は良好であった。また、Gemcitabine+nab-Paclitaxel療法にPamrevlumabを併用することにより、切除率を向上させる可能性があることが示された。これらの知見は局所進行切除不能膵癌に対する術前補助化学療法(neoadjuvant chemotherapy)としてさらに検証する必要がある。
(レポート:金沢大学先進予防医学研究センター 寺島 健志)
References
1) Hartel M, et al.: World J Surg. 28(8): 818-825, 2004[PubMed]
2) Wenger C, et al.: Oncogene. 18(4): 1078-1080, 1999[PubMed]

監修
谷口 浩也先生
愛知県がんセンター中央病院
薬物療法部 医長
加藤 健先生
国立がん研究センター中央病院
消化管内科 医長
山﨑 健太郎先生
静岡県立静岡がんセンター
消化器内科 医長
上野 誠先生
神奈川県立がんセンター
消化器内科 医長
レポーター (50音順)
伊澤 直樹先生
聖マリアンナ医科大学
臨床腫瘍学
大北 仁裕先生
香川大学医学部
腫瘍内科
小林 智先生
神奈川県立がんセンター
消化器内科
佐藤 雄哉先生
国立がん研究センター中央病院
臨床研究支援部門
高橋 直樹先生
埼玉県立がんセンター
消化器内科
寺島 健志先生
金沢大学
先進予防医学研究センター
古田 光寛先生
静岡がんセンター
消化器内科
堀田 洋介先生
埼玉医科大学国際医療センター
消化器腫瘍科