ミラノ基準外のBCLC stage A/B切除可能肝細胞癌に対する術前FOLFOX肝動注療法vs.手術先行(upfront surgery)治療の多施設共同無作為化第III相試験の中間解析
Neoadjuvant hepatic arterial infusion chemotherapy (HAIC) with FOLFOX could improve outcomes of resectable BCLC stage A/B hepatocellular carcinoma patients beyond Milan criteria: An interim analysis of a multi-center, phase 3, randomized, controlled clinical trial
Shaohua Li, et al.
監修コメント
本試験は、進行肝細胞癌患者を対象とし、手術先行と比較して術前にFOLFOX肝動注化学療法を2~4サイクル実施する術前補助化学療法の有用性を検証した第III相試験である。主要評価項目に設定された全生存(OS)期間、副次評価項目に設定された無増悪生存(PFS)期間はいずれも術前FOLFOX肝動注化学療法群で良好であった。
切除可能肝細胞癌患者に対する周術期治療としてはこれまで、術後補助化学療法としてSorafenib、ビタミンK2、非環式レチノイドの有用性が検証され、現在も免疫療法を中心にいくつもの術後補助化学療法の開発治験が行われているが、これまでに有用性が検証された治療はない。一般的に、周術期の補助化学療法は、進行期の患者を対象とした試験で有用性が示された治療法を用いて開発が行われるが、FOLFOX肝動注化学療法は同じく今回のASCOで発表されたFOHAIC-1試験において、対照群に設定されたSorafenibと比較して有意にOSを延長させたことが示された。
予後不良の危険因子とされる病理学的脈管侵襲を抑制したことが示されており、高い奏効割合からも微小な他病変を制御することにより術後再発を抑制しOS期間を延長させた可能性が考えられる。対照群の手術成績がやや不良である点や再発病変に対する治療が適切に実施されたか等、詳細な検討の余地はあるものの、忍容性は高く、部分集団解析の結果からも、ミラノ基準外でAFP高値や両葉に分布するといった術後再発高リスク群では、切除可能肝細胞癌に対する術前FOLFOX肝動注化学療法は有望な治療と考えられた。
(金沢大学先進予防医学研究センター 特任准教授 寺島 健志)
ミラノ基準外の肝細胞癌
ミラノ基準とは肝細胞癌の治療において肝移植の適応を判断する基準の一つであり、「遠隔転移と血管侵襲を認めず、かつ、5cm以下の固まりが1個、または、複数ある場合は個数が3個以下で、最大径が3cm以下」と定められている。ミラノ基準外の肝細胞癌症例においては50~60%の症例において微小脈管侵襲が認められることが報告されており、このような症例に対する肝切除術の予後は良好とは言えず(5年生存割合10.7%)、最適な治療戦略が求められている1,2)。肝動注療法は、肝腫瘍局所への化学療法の到達性を高め、全身への毒性が減じられる手法として特に本邦を中心にアジアで開発されてきた3)。進行肝細胞癌を対象としたいくつかの臨床試験において、肝動注療法はTACEやSorafenib単剤療法よりも良好な成績が報告されている4)。今回、ミラノ基準外のBCLC stage A/B切除可能肝細胞癌に対する新たな治療戦略として、術前FOLFOX肝動注療法の有用性を検証する目的で多施設共同無作為化第III相試験が実施された。
術前FOLFOX肝動注療法と手術先行治療の無作為化第III相試験
本試験の対象は「ミラノ基準外のBCLC stage A/B切除可能肝細胞癌」であり、登録患者を術前FOLFOX肝動注療法群(術前2~4サイクル)と手術先行群に1:1に割り付けた。術前FOLFOX肝動注療法群では2サイクル施行後に肝動注療法の忍容性および奏効を評価し、外科切除、肝動注2サイクル追加、他の治療(TACE、全身化学療法など)のいずれかの治療が実施された(図1)。主要評価項目は全生存(OS)、副次評価項目は無増悪生存(PFS)、無再発生存(RFS)、安全性であった。
図1 Treatment Plan(発表者の許可を得て掲載)
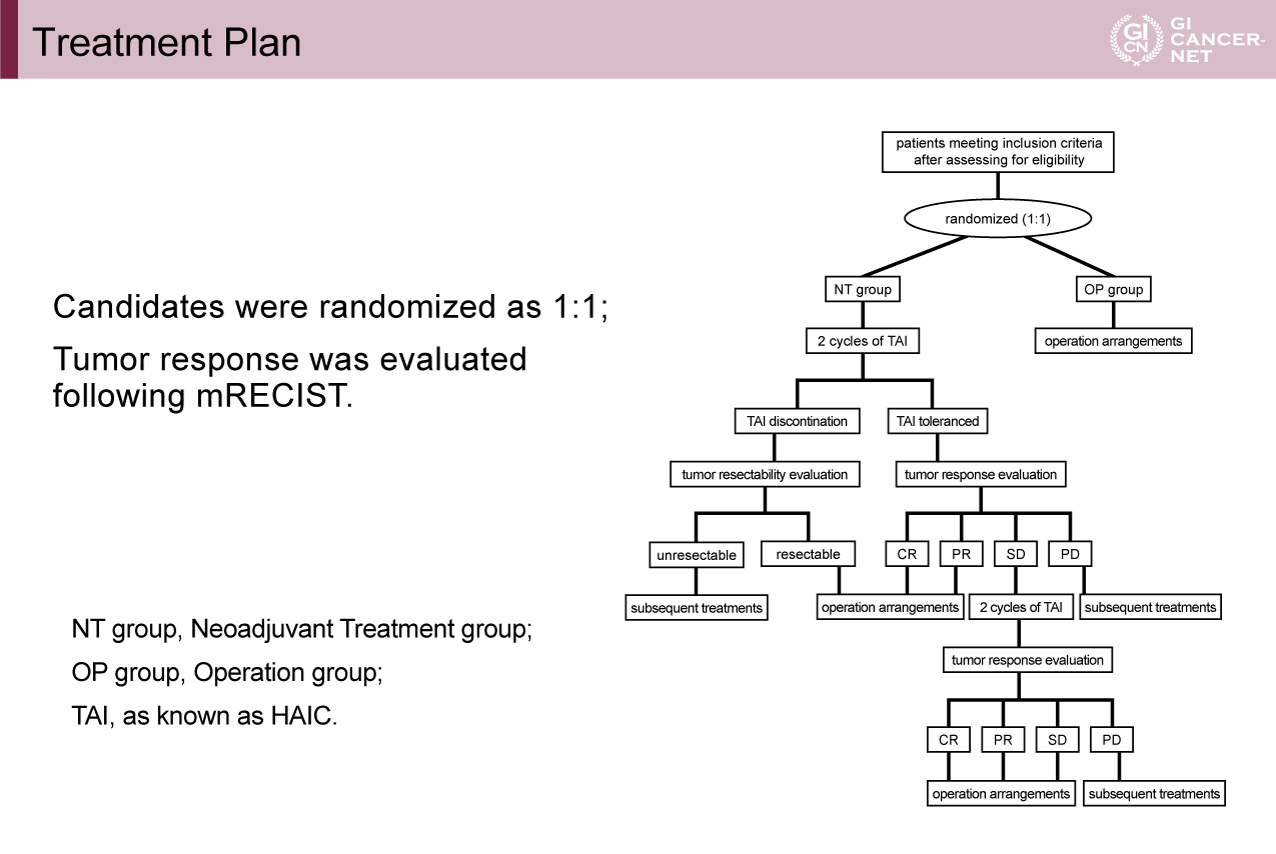
術前FOLFOX肝動注療法は手術先行治療に対して全生存期間における優越性を示した
本研究は中国の5施設で実施され、208例が登録され、各群104症例ずつ割り付けられた。患者背景に関してはT-Bil高値、ICGR15高値が術前FOLFOX肝動注療法群にやや多く認められたが、その他に群間差は認められなかった。主要評価項目のOSに関しては1年OS割合92.9% vs. 79.5%、2年OS割合78.6% vs. 62.0%、3年OS割合63.5% vs. 46.3%、ハザード比(HR)=0.510(95%信頼区間[CI]: 0.288-0.901、p=0.016)と術前FOLFOX肝動注療法群で有意な延長効果が認められた(図2)。副次評価項目のPFSに関しても6ヵ月PFS割合77.6% vs. 52.7%、12ヵ月PFS割合50.4% vs. 42.8%、18ヵ月PFS割合47.4% vs. 34.8%、PFS中央値14.1ヵ月vs. 8.9ヵ月、HR=0.625(95% CI: 0.421-0.929、p=0.017)と術前FOLFOX肝動注療法群で有意な延長効果が認められた(図3)。OS、PFSともにいずれのサブグループにおいても術前FOLFOX肝動注療法群で良好な傾向を示した。術前FOLFOX肝動注療法の有効性に関しては奏効割合(ORR)63.6%、病勢制御割合(DCR)96.0%で外科切除移行割合は88.9%であった。術後病理診断による微小脈管侵襲は手術先行治療群で39.0%、術前FOLFOX肝動注療法群で11.4%に認められた。一方、有害事象に関しては術前FOLFOX肝動注療法群においてgrade 1の有害事象が59.6%、grade 2の有害事象が26.3%の症例に認められたが、いずれも許容範囲内のものであり、周術期合併症の発生率に関しては両群に差を認めなかった。
図2 OS(発表者の許可を得て掲載)
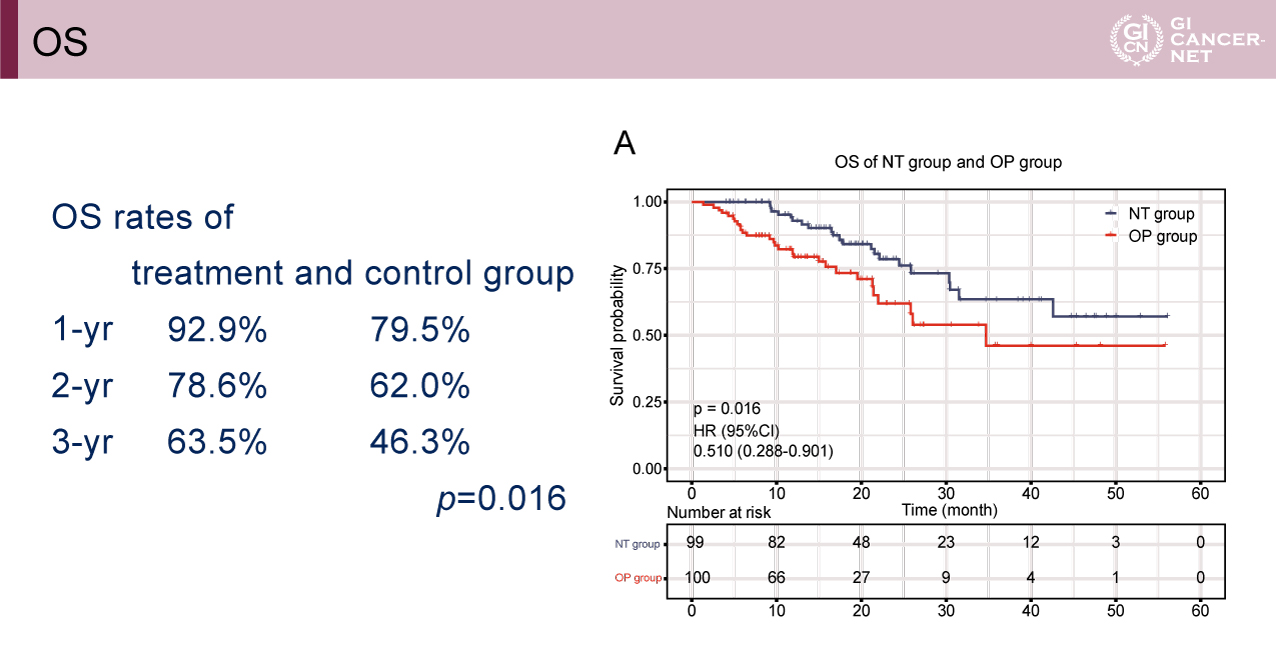
図3 PFS(発表者の許可を得て掲載)
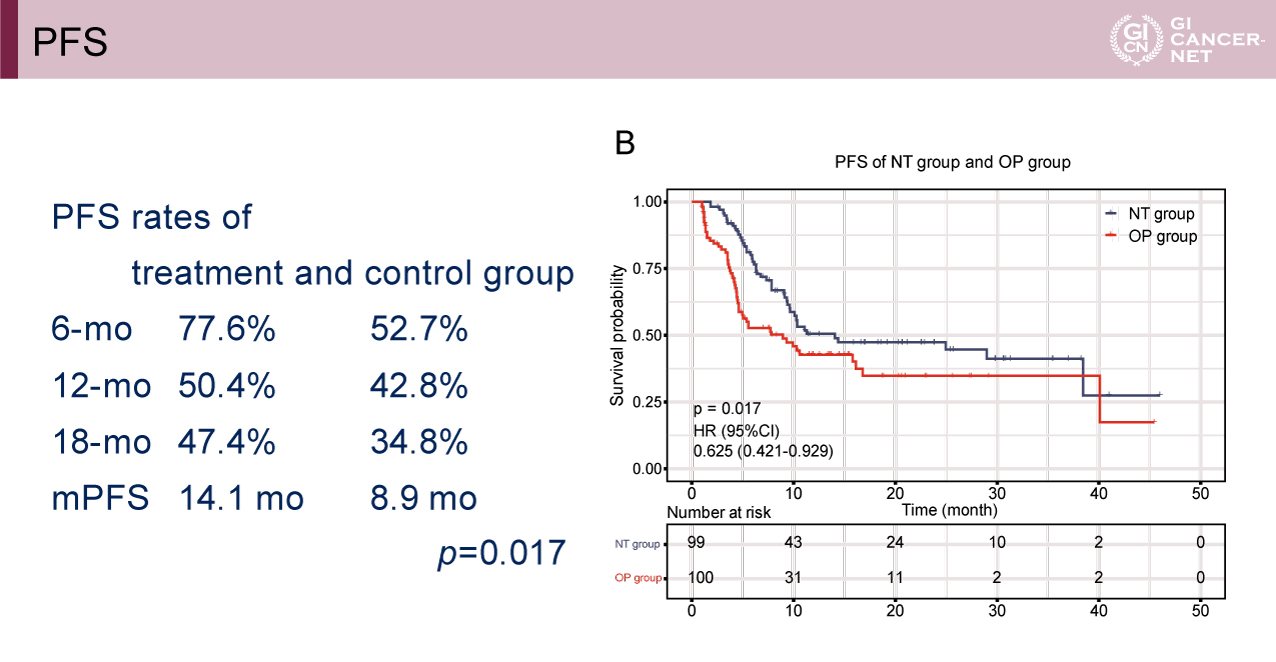
まとめ
ミラノ基準外のBCLC stage A/B切除可能肝細胞癌に対する術前FOLFOX肝動注療法は手術先行治療に対し、生存期間における有意な延長効果を示した。術前FOLFOX肝動注療法は良好な抗腫瘍効果、忍容性を有し、新たな治療オプションの一つになりうると考えられた。
(レポート:慶應義塾大学病院 腫瘍センター 林 秀幸)
References
1) Shen JY, et al.: Int J Surg. 44: 33-42, 2017[PubMed]
2) Kim JM, et al.: J Gastrointest Surg. 24(10): 2219-2227, 2020 [PubMed]
3) Obi S, et al.: Liver Cancer. 4(3): 188-199, 2015[PubMed]
4) Zhang T, et al.: Hepatobiliary Surg Nutr. 10(2): 180-192, 2021[PubMed]
関連サイト
・FOHAIC-1試験[ClinicalTrials.gov]
寺島 健志先生
金沢大学先進予防医学研究センター 特任准教授