限局性の食道/食道胃接合部腺癌患者における、周術期のNivolumab+Ipilimumab療法の第II/III相試験:術前治療の病理学的完全奏効割合の結果(ECOG-ACRIN EA2174)
A phase II/III study of peri-operative nivolumab and ipilimumab in patients with locoregional esophageal and gastroesophageal junction adenocarcinoma-results of the neoadjuvant pathologic complete response (pCR) rate: ECOG-ACRIN EA2174
Jennifer R. Eads, et al.
監修コメント
食道腺癌、食道胃接合部腺癌の標準治療の一つに、CROSS試験の結果により、術前化学放射線療法(CRT)を行った後に手術を行うというものがある。また、CheckMate 577試験の結果により、術後pCRを得られなかった患者には術後Nivolumabを1年間投与することが標準治療となっている。今回の試験は、術前CRTに対してNivolumabの上乗せをみるStep 1、そして術後Nivolumabに対してIpilimumabの上乗せをみるというStep 2の2×2デザインであるが、今回は、そのStep 1パートのみの発表である。
今回の興味は純粋にCROSSレジメンにNivolumabの併用により、有効性の上乗せ効果があるか、であったが、結論からすると、短期的有効性の指標であるpCRではほぼ上乗せがなかった。これは、ESCORT-Neo試験や、FRONTiER試験において、術前化学療法に免疫チェックポイント阻害剤(ICI)を併用した試験では軒並みpCR 10%程度の改善が認められているのとは対象的である。根治的CRTとICIとの同時併用については、他癌種も含めあまりよい結果が出ていないのが現状である。食道癌でも韓国からの報告や、米国からの報告でも、軒並みpCRは増えず、逆に毒性が増えるという報告がある。放射線によるリンパ球へのダメージがその原因だと言われているが、これといった原因が指摘されているわけではない。ICIと放射線の相乗効果であるAbscopal効果も言われているが、比較的多い線量を短期間照射することで、免疫への効果が最大化すると言われており、従来行っていた2.0Gyを20回など、比較的回数が多い場合にはICIとの相乗効果は難しいのかもしれない。
ちょうど、この対象に対して、今回のASCOにて、ESOPEC試験の結果が報告された。術前術後FLOT療法が、術前CRT療法(術後Nivolumabなし)に対して生存期間において、優越性を示しているが、MATTERHORN試験、KEYNOTE-585試験、DANTE試験など、腺癌症例に対して、FLOT療法へICIを併用することで、pCRの改善はすでに示されている。長期生存への影響についてはもう少し時間がないと不明であるが、食道癌・胃癌の次の周術期治療については、術前CRTにICIを併用するよりも、術前術後3剤併用療法へICIを併用するほうが、より効果が期待できそうであると感じられた。
(国立がん研究センター中央病院 消化管内科/頭頸部・食道内科 科長 加藤 健)
食道/食道胃接合部腺癌の周術期におけるICIを用いた治療開発
限局性の食道/食道胃接合部腺癌に対しては、CROSS試験1)の結果から、術前化学放射線療法を行った後に手術を行うという治療戦略が、欧米では標準治療の一つとして認識されている。加えて、術前化学放射線療法後に手術を行い、病理学的完全奏効が得られなかった食道/食道胃接合部癌の患者を対象に、術後補助療法としてNivolumabを投与することで、無病生存期間の延長が示されたというCheckMate 577試験2)の結果から、術後補助化学療法としてのNivolumab療法は、同対象における標準治療の一つと位置付けられている。
しかし、切除不能・再発の食道/食道胃接合部腺癌において適応となっている免疫チェックポイント阻害薬(ICI)の周術期での役割を考えたときに、術前化学放射線療法とICIの併用、あるいは術後補助療法としての他のICIとの併用が、生存期間を延長させうるかどうかは明らかになっていない。このような臨床的疑問を解決するためにECOG-ACRIN EA2174試験が実施された。
ECOG-ACRIN EA2174試験の対象と方法
ECOG-ACRIN EA2174試験は、米国で実施された切除可能な限局性の食道/食道胃接合部腺癌を対象とした無作為化第II/III相試験である。主な適格基準は18歳以上、ECOG PS 0-1、未治療で、食道切除術を予定されているT1N1-3M0またはT2-3N0-2M0の食道/食道胃接合部腺癌(Siewert分類type I/II)であった。1回目の無作為化(ステップ1)では、患者はいわゆるCROSSレジメン(Carboplatin AUC 2+Paclitaxel 50mg/m2を毎週、計5サイクルの静脈内投与)と41.4~50.4Gyの放射線治療を併用し、それに加えて治療開始1週目(1日目)と3週目(15日目)にNivolumab 240mgを静脈内投与しない群(対照群)とする群(Nivolumab併用群)に無作為に割り付けられ、術前治療終了後4~8週以内に食道切除術が行われた(図1)。2回目の無作為化(ステップ2)では、術後補助療法として、Nivolumab 480mgを4週毎、計13サイクルの静脈内投与を行い、それに加えてIpilimumab 1mg/kgを6週毎、計4回(6ヵ月)併用する群と併用しない群に、無作為に割り付けられた。術後補助療法終了後は、2年間は3ヵ月毎に経過観察され、その後5年経過するまでは6ヵ月毎に経過観察された。ステップ1を比較した術前治療の主要評価項目は病理学的完全奏効割合(pCR)で、Nivolumabの上乗せによる15%のpCRの改善が期待された(23% vs. 38%、検出力90%、片側α=0.10)。ステップ2を比較した術後補助療法の主要評価項目は無病生存割合(DFS)であった。副次評価項目はステップ2における全生存期間(OS)とステップ1におけるDFS、ステップ1・2両者における有害事象であった。今回はステップ1のpCRをメインとした短期成績のみの報告であり、ステップ2の長期成績の報告はデータが成熟した時点で報告される予定である。
図1 EA2174 Study Design(発表者の許可を得て掲載)
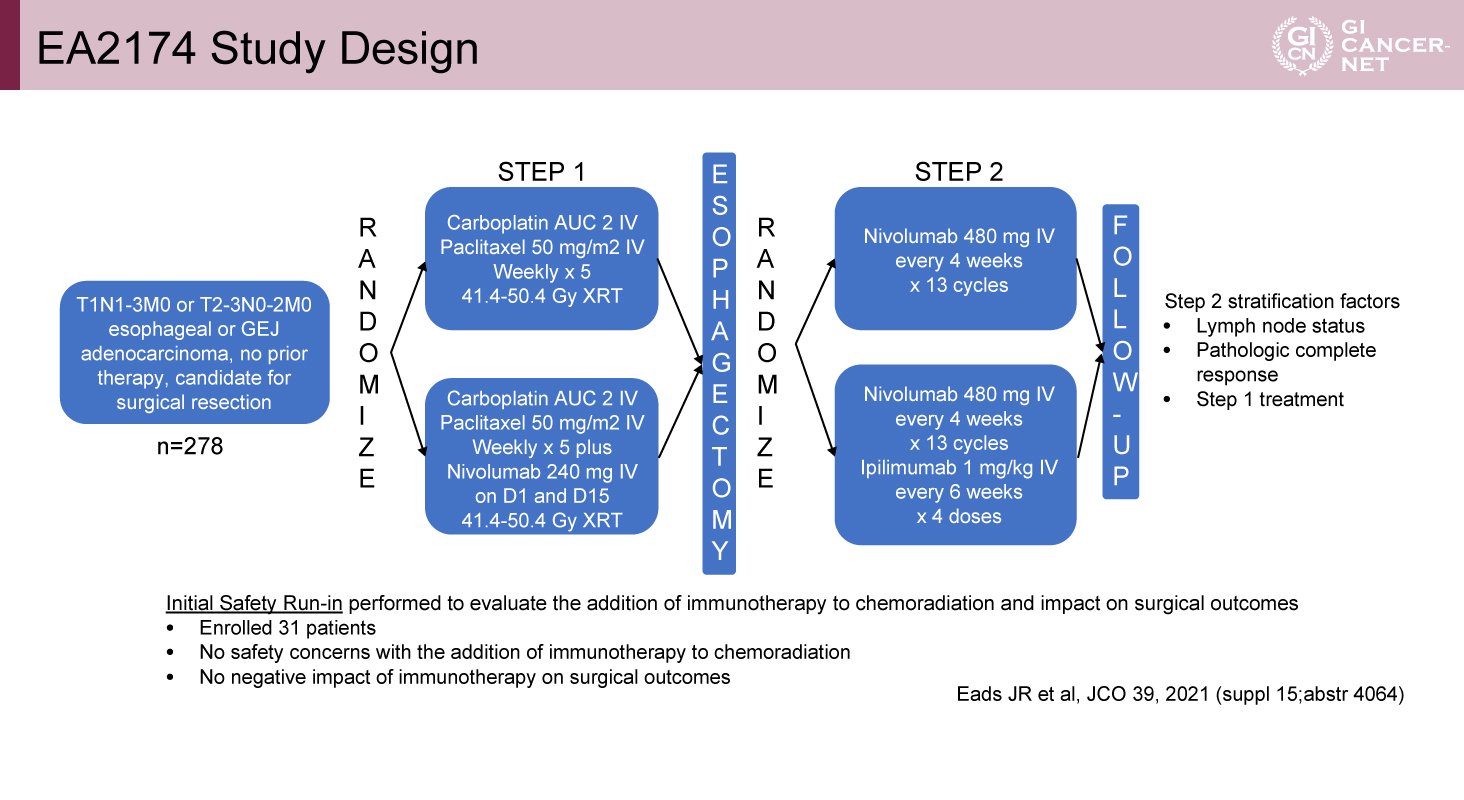
Nivolumabの上乗せによるpCRの改善は認められず
適格基準を満たした計278例が、ステップ1として1:1で各々の治療群に無作為に割り付けられた。患者背景は両群で概ねバランスがとれていたが、治療前にリンパ節転移なしと判断された患者は、Nivolumab併用群のほうが対照群よりもやや多かった(53.3% vs. 35.5%)。術前治療を完遂したのは、Nivolumab併用群で90.2%、対照群で91.1%と差はなく、手術実施割合はNivolumab併用群で82.8%、対照群で77.2%とやや低かった。手術が実施できなかった理由としては、多いほうから有害事象、患者拒否、病勢進行などであった。主要評価項目のpCRの割合は、Nivolumab併用群で24.8%(95%信頼区間17.8-32.9)、対照群で21.0%(95%信頼区間14.5-28.8)であり、有意な差は認められなかった(p=0.27)(表1)。
Grade 3以上の治療関連の主な有害事象(Nivolumab併用群 vs. 対照群)は、リンパ球数減少(63.6% vs. 59.2%)、白血球数減少(23.5% vs. 14.2%)、好中球数減少(15.1% vs. 5.2%)、貧血(7.6% vs. 5.2%)、嚥下障害(6.1% vs. 6.7%)、食道炎(2.3% vs. 5.2%)、胸水貯留(3.1% vs. 4.5%)などで、概ね差はなかった。手術関連の合併症は、Nivolumab併用群30.1%、対照群37.1%と同程度に認められ、主な合併症(Nivolumab併用群 vs. 対照群)としては、縫合不全(9.0% vs. 5.7%)、不整脈(4.5% vs. 11.4%)、気胸(7.2% vs. 11.4%)、治療介入を必要とする胸水貯留(9.9% vs. 8.6%)などが認められた。
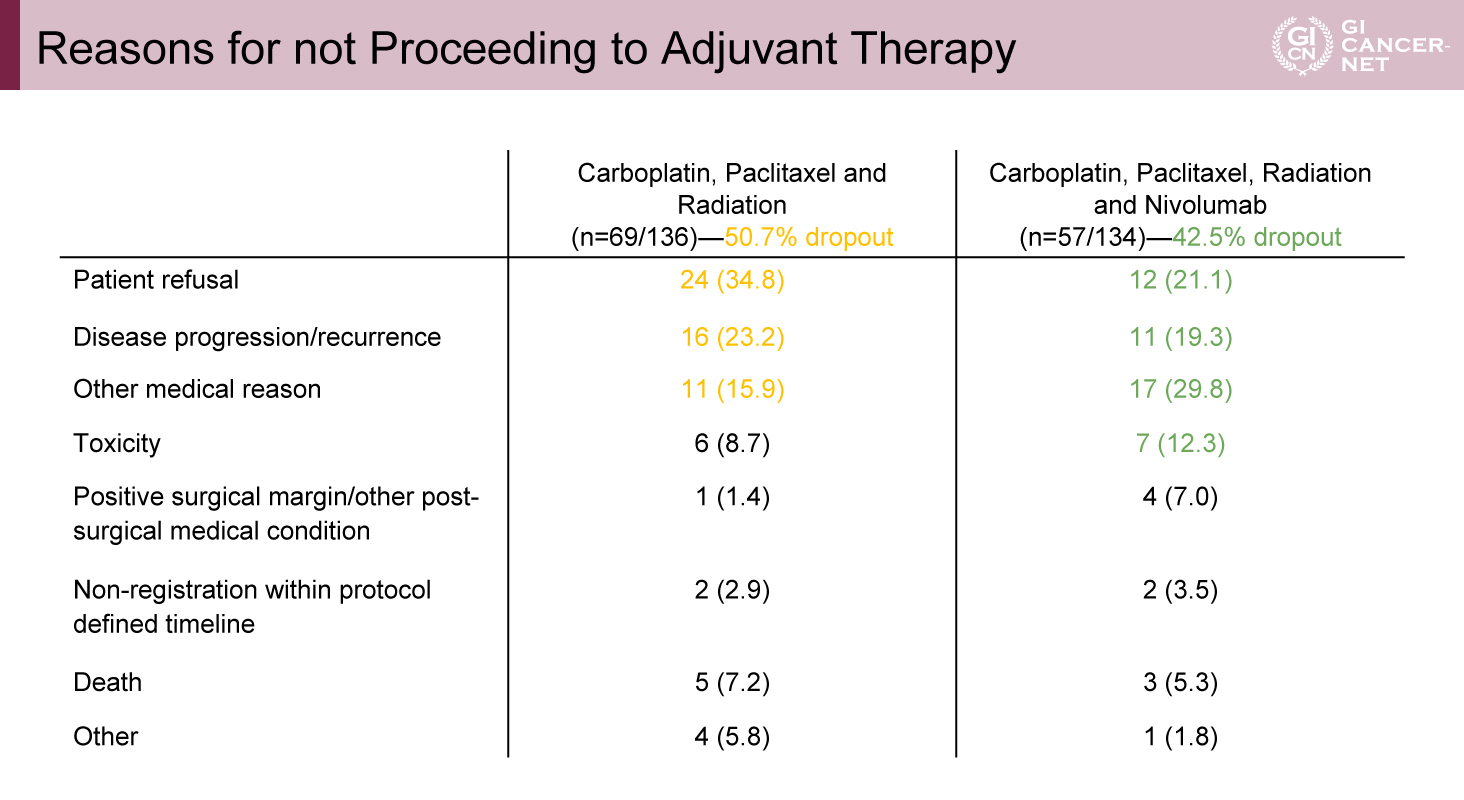
手術後に術後補助療法に進まずに脱落となったのはNivolumab併用群の42.5%、対照群の50.7%であり、かなり脱落が多かった。脱落の主な理由(Nivolumab併用群 vs. 対照群)としては、患者拒否(21.1% vs. 34.8%)、病勢進行・再発(19.3% vs. 23.2%)、有害事象(12.3% vs. 8.7%)、死亡(5.3% vs. 7.2%)などであった(表2)。
表1 Pathologic Complete Response Rate(発表者の許可を得て掲載)
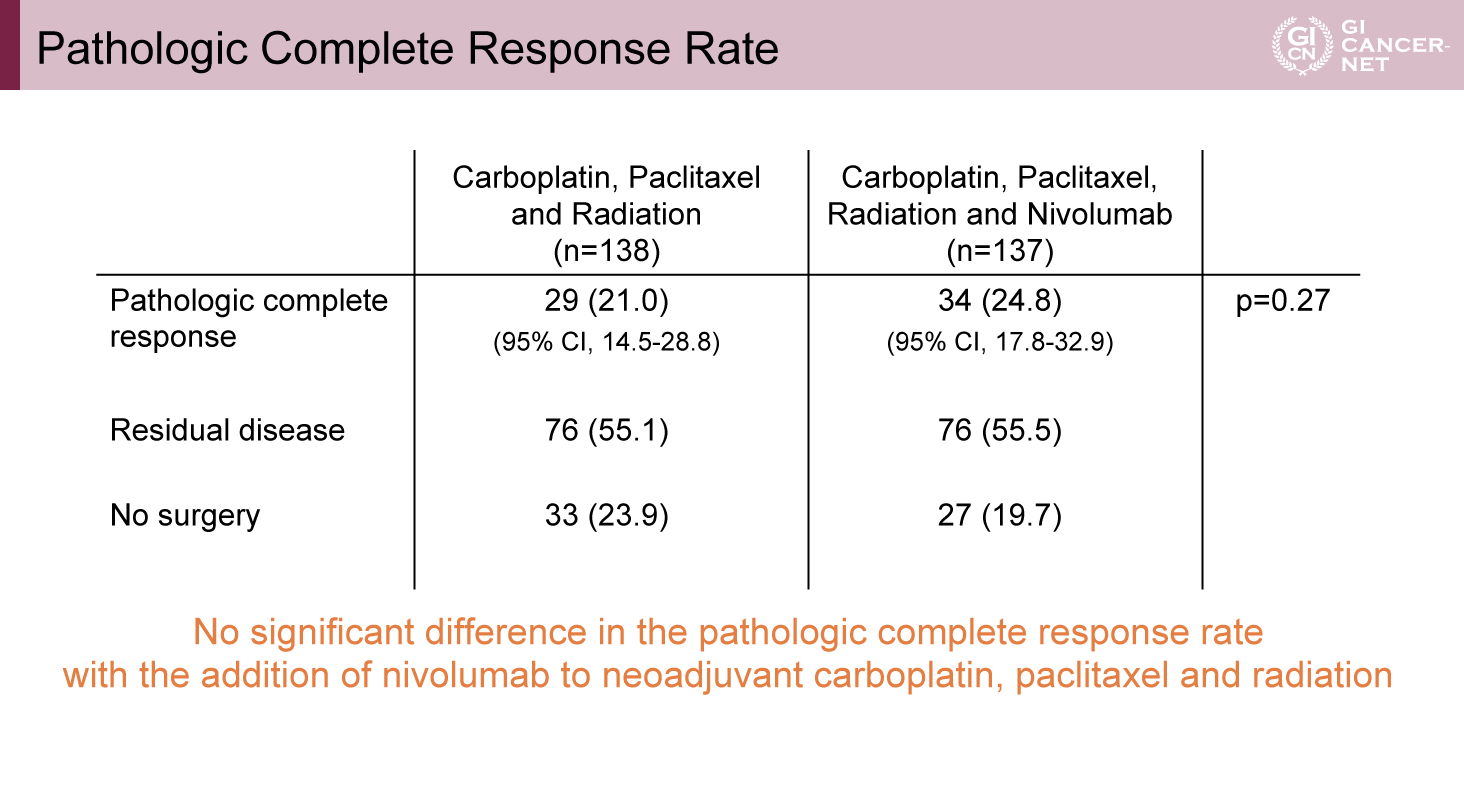
表2 Reasons for not Proceeding to Adjuvant Therapy(発表者の許可を得て掲載)
まとめ
Carboplatin+Paclitaxel+放射線治療という術前治療にNivolumabを上乗せしても、pCRの割合は有意に改善しなかった。化学放射線療法とNivolumabを併用しても、有害事象や手術合併症の増加はなかった。術後補助療法へ移行しなかった脱落例がかなり多く、今後の試験デザインを考慮する必要がある。
(レポート:国立がん研究センター中央病院 頭頸部・食道内科 今関 洋)
References
1) van Hagen P, et al.: N Engl J Med. 366(22): 2074-2084, 2012 [PubMed]
2) Kelly RJ, et al.: N Engl J Med. 384(13): 1191-1203, 2021 [PubMed]
関連サイト
・EA2174試験[ClinicalTrials.gov]
・CheckMate 577試験[ClinicalTrials.gov][論文紹介]
加藤 健先生
国立がん研究センター中央病院 消化管内科/頭頸部・食道内科 科長