BRAF V600E変異を有する切除不能大腸癌に対する一次治療としてのEncorafenib+Cetuximab+mFOLFOX6併用療法(BREAKWATER試験):無増悪生存期間および全生存期間のアップデート解析
First-line encorafenib + cetuximab + mFOLFOX6 in BRAF V600E-mutant metastatic colorectal cancer (BREAKWATER): Progression-free survival and updated overall survival analyses
Elena Elez, et al.
監修コメント
今回のASCO 2025で発表されたBREAKWATER試験のアップデート解析の結果は、BRAF V600E変異を有する切除不能大腸癌(mCRC)の治療戦略を大きく前進させる、きわめて重要なエビデンスとなった。これまで、BRAF V600E変異陽性mCRCは予後不良群とされており、一次治療の有効性は限定的であり、無増悪生存期間(PFS)の中央値は5〜6カ月、全生存期間(OS)の中央値も10〜13カ月程度にとどまっていた1,2)。
こうした中、本試験では、Encorafenib+Cetuximab+mFOLFOX6(EC+mFOLFOX6)療法が、これまでの標準的な一次治療と比較してPFS中央値を12.8カ月(vs 7.1カ月)、OS中央値を30.3カ月(vs 15.1カ月)へと大きく延長し、いずれも統計学的に有意かつ臨床的にも意味のある改善を示した。特にOS中央値が30カ月を超えた点は、これまでのBRAF変異陽性mCRCの治療成績を塗り替える成果である。また、すべてのサブグループにおいて一貫した有効性が確認されており、治療効果の再現性と適用の汎用性が裏付けられている。
一方、BRAF V600E変異陽性mCRCに対して、化学療法なしのECのみの標的治療薬だけの治療戦略が否定されたことも注目される。MSI-High/dMMRを有するmCRCに対しては免疫チェックポイント阻害薬のみの治療戦略が確立されている中、BRAF変異型mCRCでは標的治療薬と化学療法の併用が最も有用な治療レジメンであった。BRAF変異型mCRCのヘテロな分子病理学的特徴から由来する結果を妄想するが、さらなる一次治療の開発の可能性もあるだろう。
本試験結果は、EC+mFOLFOX6療法がBRAF V600E変異陽性mCRCに対する一次治療として新たな標準治療となるにふさわしいデータであり、今後、本レジメンが臨床現場で広く導入されていくことが期待される。
(聖マリアンナ医科大学 臨床腫瘍学講座 主任教授 砂川 優)
BREAKWATER試験:BRAF V600E変異陽性mCRCに対するEC+mFOLFOX6療法のPFSおよびOS(第2回中間解析)の結果が報告
切除不能大腸癌(mCRC)患者の約8~12%に認められるBRAF V600E変異症例では、一次化学療法の有効性は限定的であることがこれまでの知見であった。そこで、未治療のBRAF V600E変異陽性mCRC患者を対象に、Encorafenib+Cetuximab(EC)±mFOLFOX6療法と標準治療(SOC)を比較する第III相試験(BREAKWATER)が実施された。
本試験の2つの主要評価項目のうち、中央判定(BICR)による客観的奏効率(ORR)に関しては、EC+mFOLFOX6療法がSOCと比較して統計学的に有意な改善を示すことがすでに報告されている3)。今回の報告では、もうひとつの主要評価項目である無増悪生存期間(PFS)について、EC+mFOLFOX6群とSOC群の比較における中央判定(BICR)での解析結果が示されたほか、全生存期間(OS)の第2回中間解析結果、EC単独群の有効性データおよび全群の安全性データも発表された。
BREAKWATER試験のデザイン
BREAKWATER試験は、BRAF V600E変異を有し、ECOG PS 0~1の未治療のmCRC患者を対象とした、多施設共同・非盲検の第III相臨床試験である。MSI-H/dMMRおよびRAS変異を有する症例は除外された。対象患者はEC群、EC+mFOLFOX6群、SOC群に1:1:1でランダムに割り付けられた。
主要評価項目は、BICRによるPFSおよびORRの2項目であり、OSが主要な副次評価項目であった。層別化因子には、地域(米国・カナダ、欧州、その他)およびECOG PS(0/1)が用いられた。なお、第II相試験(ANCHOR)の結果を踏まえ、EC単独群がSOC群に対して優越性を示す可能性が低いと判断されたため、試験途中でプロトコル改訂が行われ、EC群への登録は早期に中止となり、以降はEC+mFOLFOX6群とSOC群へ1:1で割り付けられた。
BRAF V600E変異陽性mCRCの一次治療において、EC+mFOLFOX6療法はPFSおよびOSを有意に延長
本試験には合計637例が登録された(EC群:158例、EC+mFOLFOX6群:236例、SOC群:243例)。患者背景は群間でバランスが取れていた。
主要評価項目のPFS(BICR)において、EC+mFOLFOX6群はSOC群と比較して有意な延長が認められた(中央値:12.8カ月 vs 7.1カ月、ハザード比(HR)=0.53[95%信頼区間(CI)0.407-0.677]、p<0.0001)(図1)。
また、すべてのサブグループにおいてEC+mFOLFOX6群は一貫して良好なPFSを示した。さらに、統計学的検定は行われていないが、EC群のPFS中央値は6.8カ月であり、SOC群とKaplan-Meier曲線がほぼ重なっていた。
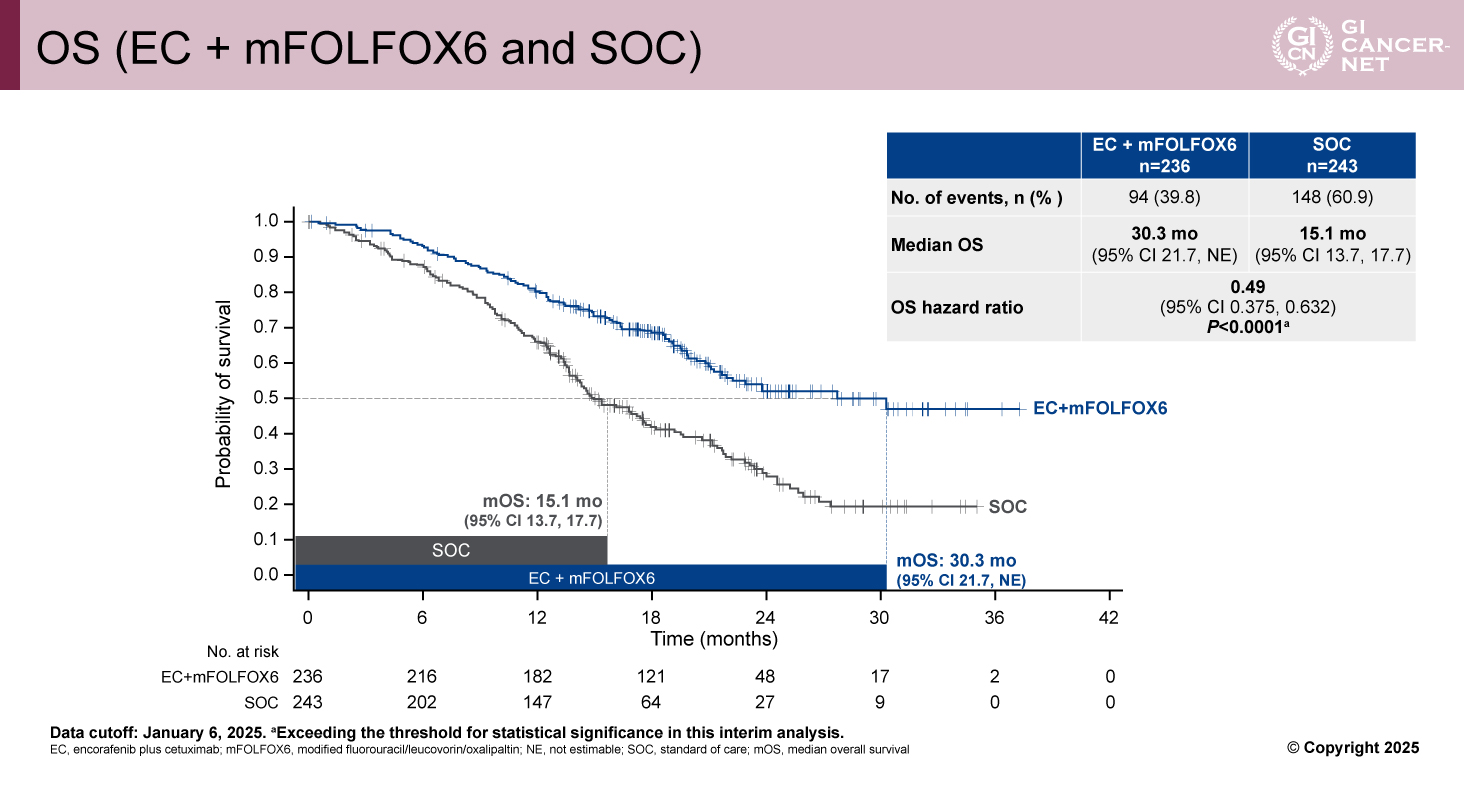
OSに関しても、EC+mFOLFOX6群はSOC群と比較して有意に良好な成績を示しており(中央値:30.3カ月 vs 15.1カ月、HR=0.49[95% CI: 0.375-0.632]、p<0.0001)(図2)、すべてのサブグループで一貫した結果であった。なお、EC群のOS中央値は19.5カ月であり、Kaplan-Meier曲線はEC+mFOLFOX6群とSOC群の中間に位置していた(統計学的検定は行われていない)。
BICR評価によるORRは、EC+mFOLFOX6群で65.7%と最も高く、EC群では45.6%、SOC群では37.4%であった。奏効期間(DOR)の中央値も、EC+mFOLFOX6群で13.9カ月と最も長く、EC群では7.0カ月、SOC群では10.8カ月であった。DORが12カ月以上持続した症例の割合も、EC+mFOLFOX6群で34.8%と最も高く、EC群20.8%、SOC群17.6%を上回った。
治療関連有害事象に関しては、Grade 3/4の発現頻度がEC+mFOLFOX6群で最も高い76.3%を示したのに対し、EC群では15.7%、SOC群では58.5%であった。ただし、新たな毒性シグナルは認められず、殺細胞性抗癌薬の減量や中止の頻度も増加していなかった。
図1 PFS by BICR (EC + mFOLFOX6 and SOC)(発表者の許可を得て掲載)
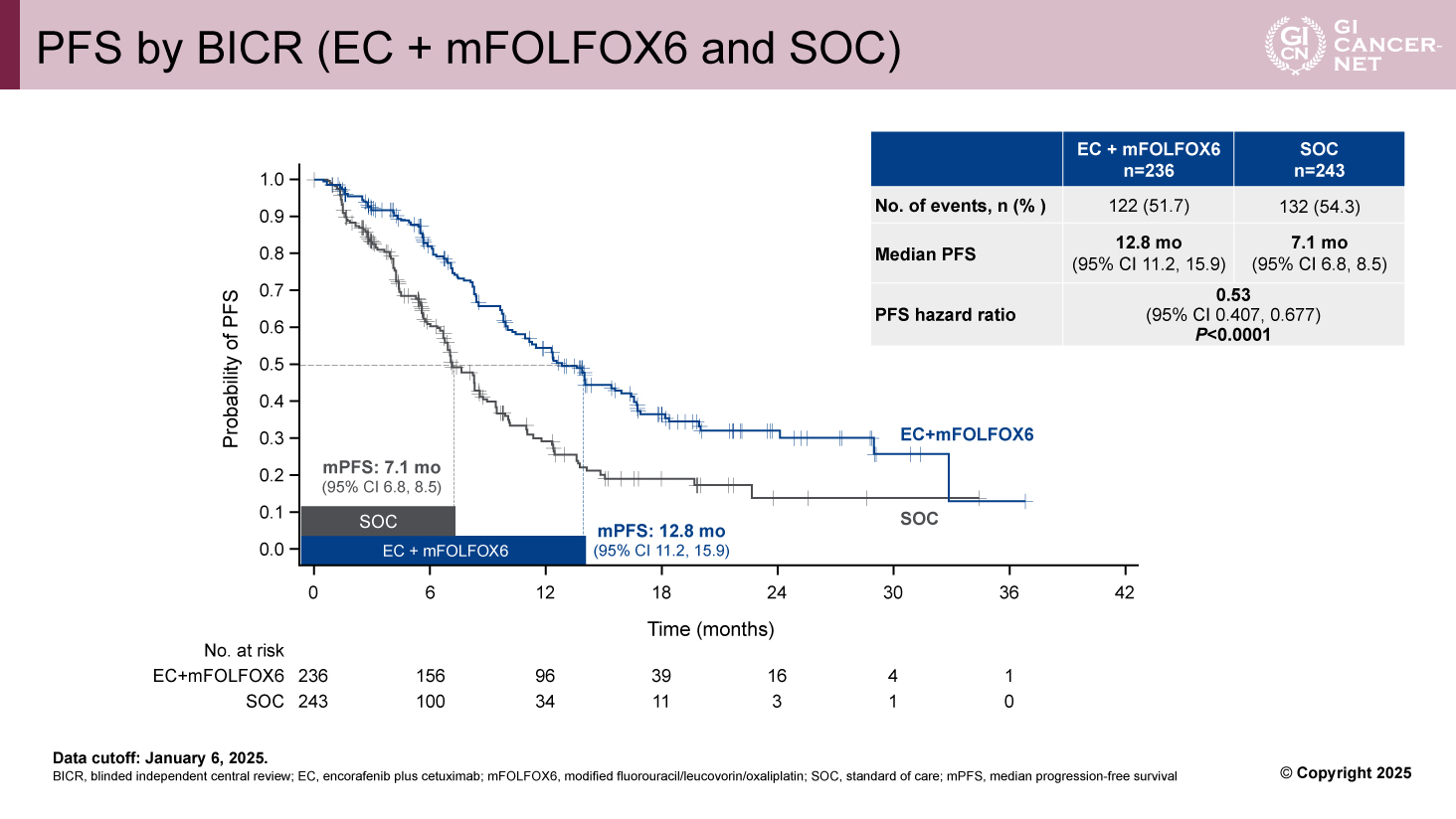
図2 OS (EC + mFOLFOX6 and SOC) (発表者の許可を得て掲載)
結論
EC+mFOLFOX6療法はSOCと比較してPFSおよびOSの両方を統計学的に有意かつ臨床的に意味のあるレベルで延長した。BREAKWATER試験の結果から、BRAF V600E変異を有するmCRCの一次治療において、EC+mFOLFOX6療法が新たな標準治療として確立された。
(レポート:聖マリアンナ医科大学 臨床腫瘍学講座 講師 新井 裕之)
References
1) Cohen R, et al.: J Natl Cancer Inst. 113(10): 1386-1395, 2021[PubMed]
2) Martinelli E, et al.: ESMO Open. 7(6): 100603, 2022[PubMed]
3) Kopetz S, et al.: Nat Med. 31(3): 901-908, 2025[PubMed]
関連サイト
・BREAKWATER試験[ClinicalTrials.gov]
・Elez E, et al.: N Engl J Med. May 30, 2025[Online ahead of print][PubMed]
砂川 優 先生
聖マリアンナ医科大学
臨床腫瘍学講座 主任教授