Stage I-IIIの膵腺癌に対する術前化学療法としてmFOLFIRINOX療法とPAXG療法を比較するランダム化第III相試験(CASSANDRA – PACT-21試験)
Results of a randomized phase 3 trial of pre-operative chemotherapy with mFOLFIRINOX or PAXG regimen for stage I-III pancreatic ductal adenocarcinoma: CASSANDRA – PACT-21 trial
Michele Reni, et al.
監修コメント
近年、切除可能または切除可能境界膵癌に対して切除単独では治療成績に限界があり、術前および術後に化学療法または化学放射線療法を組み合わせる集学的治療が行われている。ただし、その至適レジメンや治療期間に関しては統一した見解が得られておらず、国内外でさまざまな試験が実施されている。
本試験は、切除可能または切除可能境界膵癌に対する術前化学療法として2つのレジメンを比較した第III相試験であり、試験治療のPAXG療法(Gemcitabine+Nab-Paclitaxel+Cisplatin+Capecitabine併用療法)が、対照群に設定されたmFOLFIRINOX療法と比較して、主要評価項目に設定された無イベント生存期間(EFS)の延長が検証され、Positiveな結果であった。これまでは主に進行・再発膵癌で用いられるFOLFIRINOX療法やGEM+Nab-PTX療法が周術期治療として用いられる試験が多かったが、本試験の結果、PAXG療法が新たな治療選択肢と結論づけられる。
ただし、本試験の対象患者に対する治療の実情や治療成績には国内外差があり、本試験の結果解釈や本邦への適用においてはいくつかの注意を要すると考えられる。
一つは切除可能膵癌と切除可能境界膵癌とが同一試験に登録されており、本邦では標準治療が異なる。切除可能膵癌に対してはGEM+S-1併用療法が標準治療として確立している一方、切除可能境界膵癌に対してはGEM+Nab-PTX療法やFOLFIRINOX療法が選択されることが多い。また、特に切除可能境界膵癌のサブグループのEFS、全生存期間(OS)が不良であり、これは切除成績に国内外差があることに由来すると考えられ、切除成績が良好である本邦においても同様の結果が得られるか否かについては検証が必要である。さらに、本試験では主要評価項目としてEFSが設定されているが、膵癌に対するkey drugを全て使い切るレジメンの術前化学療法が行われたにもかかわらず比較的早期に再発した患者に対しては、治療選択に難渋することが想定され、OSでも有意な差が得られるのかについては、今後、長期の経過観察により明らかにされるべきと考える。
(金沢医科大学 腫瘍内科 准教授 寺島 健志)
切除可能膵癌または切除可能境界膵癌に対する標準的な術前治療は定まっていない
切除可能膵癌または切除可能境界膵癌いずれにおいても、術後の再発率が低いとはいえず、周術期の術前・術後補助療法の必要性が認識されている。これまで切除可能膵癌に対する術後補助療法は、mFOLFIRINOX療法やGemcitabine+Capecitabine療法がそれぞれPRODIGE24試験、ESPAC-4試験の結果からNCCNやESMOガイドラインでも推奨され、海外では確立されている。国内ではS-1療法がJASPAC 01試験の結果から標準的な術後補助療法として用いられている。
一方、術前補助療法についてはこれまで化学療法や化学放射線療法による複数の介入試験が行われてきたが、いまだ至適レジメンの探索が続いているのが現状であり、標準治療は確立されていない。切除可能境界膵癌は術後の再発率が高く予後も不良な集団のため何らかの術前補助療法を行うことが国内外で推奨されているが、切除可能膵癌に対しては術前補助療法の実施自体が海外ではいまだ確立されていない。PREOPANC-1試験、PREOPANC-2試験、Alliance A021501試験、SWOG S1505試験といった介入試験の結果から、mFOLFIRINOX療法またはGemcitabine+Nab-Paclitaxel療法による化学療法を行い、引き続いて化学放射線療法を加えるかどうかといった治療法が現在のNCCNやESMOガイドラインでは提示されている。
国内では切除可能膵癌に対しては、Prep-02試験の結果からGemcitabine+S-1療法が術前補助療法として推奨されている。また切除可能境界膵癌に対しては、GABARNANCE試験の結果からGemcitabine+Nab-Paclitaxel療法とS-1併用化学放射線療法の両者が、日常診療における治療オプションとして確立された。
PAXG療法(Gemcitabine+Nab-Paclitaxel+Cisplatin+Capecitabineの4剤併用レジメン)は小規模のランダム化第II相試験において切除不能膵癌(PACT-19試験)に対してGemcitabine+Nab-Paclitaxel療法と比較して良好な成績を示した。またPAXG療法の前身のPEXG療法を術前・術後療法としたランダム化第II相試験において切除可能膵癌(PACT-15試験)に対して術後補助療法群よりも良好な成績を示した。これらの結果から、切除可能膵癌または切除可能境界膵癌に対する術前補助療法としてPAXG療法とmFOLFIRINOX療法を比較する本試験が行われた。
Stage I-IIIの切除可能または切除可能境界膵腺癌を対象とした第III相試験
イタリアの多施設によって行われたランダム化第III相試験(CASSANDRA – PACT-21試験)であり、対象は組織学的に確認された腺癌で、75歳以下、KPS>60%、前治療歴のない切除可能または切除可能境界膵癌であった。
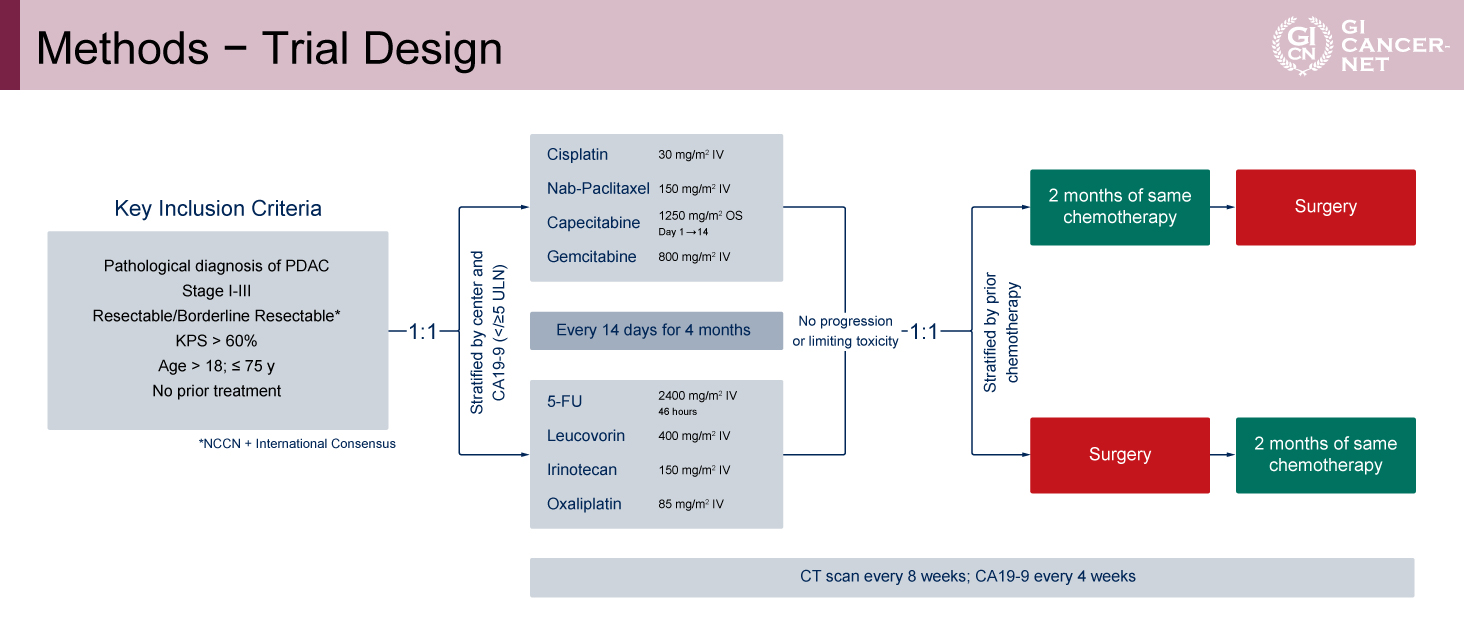
PAXG療法(Day 1:Gemcitabine 800mg/m2、Nab-Paclitaxel 150mg/m2、Cisplatin 30mg/m2、Day 1-14:Capecitabine 1,250mg/m2/回、1日2回内服)またはmFOLFIRINOX療法(Day 1:Oxaliplatin 85mg/m2、Irinotecan 150mg/m2、Leucovorin 400mg/m2、Day 1-3:5-FU 2,400mg/m2、46時間で投与)に1:1にランダム化され、14日毎に4カ月間治療が行われた。その後、毒性や病勢悪化による治療中止を認めなかった場合は、この時点で再度、化学療法の継続(同じレジメンにより2カ月間)+手術、または手術先行+術後に化学療法の再開(同じレジメンにより2カ月間)に1:1にランダム化された(図1)。
主要評価項目は無イベント生存期間(EFS)であり、イベントとしてはRECIST v1.1評価での増悪、再発、切除不能、術中の遠隔転移あり、CA19-9上昇(4週間以上あけて、2連続して20%以上の上昇)、および死亡と規定された。副次評価項目としては、奏効割合、CA19-9奏効割合、切除割合、病理学的奏効割合、有害事象、QOL、全生存期間(OS)が評価された。統計学的設定は、mFOLFIRINOX療法の3年EFS割合20%に対してPAXG療法の3年EFS割合35%への改善を検出(ハザード比[HR]0.65)することであり、両側α=0.05、検出力80%で260例の登録、173例のイベントを要した。
図1 Methods - Trial Design(発表者の許可を得て掲載)
PAXG療法がmFOLFIRINOX療法に対して有意にEFS延長効果を示した
261例がランダム化されてそれぞれの治療を受け、最終的に260例(PAXG療法群132例、mFOLFIRINOX療法128例)がITT(Intention-to-Treat)解析の対象となった。切除可能膵癌と切除可能境界膵癌は約半数ずつ含まれ、治療前のCA19-9が正常値である割合はPAXG療法群24%、mFOLFIRINOX療法群34%であった。
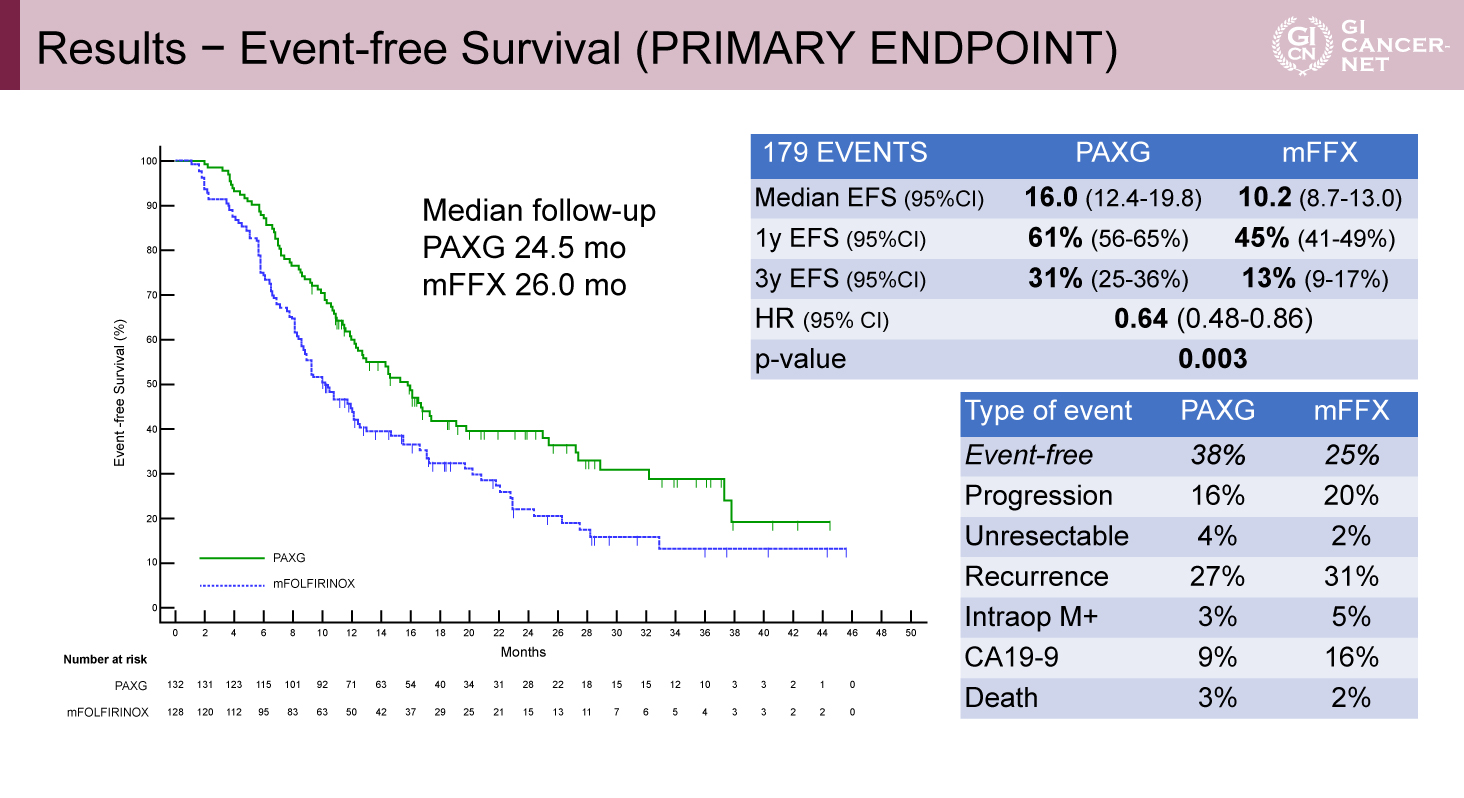
主要評価項目であるEFS中央値はmFOLFIRINOX療法群10.2カ月に対してPAXG療法群16.0カ月(HR=0.64、95%信頼区間[CI]0.48-0.86、p=0.003)であり、mFOLFIRINOX療法に対してPAXG療法が統計学的に有意にEFS延長効果を示した(図2)。
サブグループ解析では、切除可能膵癌においては3年EFS割合がPAXG療法群41%、mFOLFIRINOX療法群22%、切除可能境界膵癌においてはPAXG療法群19%、mFOLFIRINOX療法群9%であった。
副次評価項目として、OS中央値はmFOLFIRINOX療法群26.0カ月に対し、PAXG療法群37.3カ月(HR=0.70、95% CI: 0.47-1.04、p=0.07)であった。Immatureなデータであり、統計学的な有意差は示されていないものの、PAXG療法群でOSも良好な傾向を認めた。病勢制御割合(98% vs 91%)、CA19-9奏効(50%以上の低下)(88% vs 64%)、病理学的CR(3% vs 0%)、N0割合(36% vs 23%)、術中・術後の遠隔転移(5% vs 12%)も同様にPAXG療法群で有意に良好であった。切除割合、R0切除割合には両群で差は認めなかった。
有害事象については、grade 3以上の好中球減少はPAXG療法群で高頻度であり(42% vs 29%)、手足症候群も4%で認められた。下痢(2% vs 6%)や肝障害(3% vs 8%)はmFOLFIRINOX療法群でやや高頻度であったものの大きな差は認めなかった。
図2 Results - Event-free Survival (PRIMARY ENDPOINT)(発表者の許可を得て掲載)
結論
切除可能または切除可能境界膵癌に対して、mFOLFIRINOX療法に対してPAXG療法によりEFSの有意な延長効果が示された。EFSのKM曲線は一貫して上回っており、またOSも良好な傾向が示されていることから、PAXG療法は本試験の対象に対する術前治療として新たな治療選択肢になり得ると考える。
一方、主要評価項目がEFSであり、特にCA19-9上昇がイベントとして規定されていることは一般的な指標とは言えないため本試験結果の解釈に注意を要する。また切除可能膵癌においては国内外ともに術後補助療法を導入することが標準的であるため、本試験の対照群(術前mFOLFIRINOX療法)は現在の標準治療とは言えず、今後、術後補助療法を含むレジメンとの比較試験が必要と考える。
(レポート:国立がん研究センター東病院 肝胆膵内科 佐竹 智行)
関連サイト
・CASSANDRA – PACT-21試験[ClinicalTrials.gov]
寺島 健志先生
金沢医科大学 腫瘍内科 准教授