局所進行膵腺癌に対して腫瘍治療電場療法(TTFields)をGemcitabine+Nab-Paclitaxel療法へ併用する第III相試験(PANOVA-3試験)
PANOVA-3: Phase 3 study of Tumor Treating Fields (TTFields) with gemcitabine and nab-paclitaxel (GnP) for locally advanced pancreatic adenocarcinoma (LA-PAC)
Vincent Picozzi, et al.
監修コメント
本試験は、画像上遠隔転移は認めないものの、主要動脈への浸潤を伴うなどの理由で根治切除が不能な局所進行の膵癌患者を対象に、現在標準治療として用いられているGemcitabine+Nab-Paclitaxel療法を対照群として、腫瘍治療電場療法(TTFields)を併用することの有用性を検証する第III相試験である。 全体として、主要評価項目に設定された全生存期間の延長が検証され、Positiveな結果であった。局所病変の無増悪生存期間(PFS)がハザード比(HR)0.84であったのに対して、遠隔転移のPFSがHR=0.74と、恐らく想定とは逆の結果であった点は、探索的な位置づけであるものの大変興味深い。
本邦ではJCOG1908E試験において、放射線療法によるアブスコパル効果を期待し、S-1+放射線療法にNivolumabを併用することの有用性を検証する第III相試験が実施中である。同様に、TTFields療法によるアブスコパル効果により遠隔転移の増悪が抑制されれば、切除不能例のみならず、周術期治療への応用も期待される。現在、遠隔転移を有する膵癌患者を対象とし、Gemcitabine+Nab-Paclitaxel療法にTTFields療法、さらに抗PD-L1抗体であるAtezolizumabを併用する第II相試験(PANOVA-4試験)が進行中であり、結果が待たれる。
なお、本試験には日本人患者が含まれていないものの、呼吸器領域では海外に続いて本邦でも製造販売承認申請が行われている。バッテリーの重量や駆動時間、装着に伴う日常生活への影響など、改善すべき課題は多く、それらの点でも期限が設けられない切除不能例よりも期間が限定される周術期の患者がよい適応となるかもしれない。
いずれにしても、予後が極めて不良な切除不能膵癌患者に対する新たなアプローチで有用性が示された結果であり、膵癌領域での発展が期待される。
(金沢医科大学 腫瘍内科 准教授 寺島 健志)
局所進行膵癌に対する局所療法の追加の意義は確立されていない
膵癌は早期発見が難しく、進行した状態でみつかることが多い。局所進行の病期で診断される場合は30~35%を占めており、そのうち切除可能な病期に移行できるのは10~15%程度である。そのため大半の症例では根治は望めず、また疼痛をはじめとする症状を有する。
局所進行膵癌に対する治療は、遠隔転移を有する場合と同様にGemcitabine+Nab-Paclitaxel療法やmFOLFIRINOX療法、NALIRIFOX療法を用いた化学療法が国内外で標準治療として行われている。これらの化学療法後に化学放射線療法や定位放射線治療(SBRT)の追加も選択肢としてNCCNやESMOガイドラインでは提示されている。
一方、国内ではJCOG1106試験で化学放射線療法前のGemcitabine療法による導入化学療法の意義が示されなかったため、化学放射線療法は導入化学療法なしで行うことが推奨されている。化学放射線療法は化学療法単独と比較して局所制御の向上やそれによる疼痛緩和といった点が期待される。
腫瘍治療電場療法(TTFields)は、電場の作用により細胞分裂を阻害し、アポトーシス(細胞死)を誘導することで、腫瘍細胞の成長を抑制する治療法である。TTFieldsはジェネレーターと皮膚に貼った電極パッド(アレイ)を用いて治療電場を作り出す、携帯可能な医療機器である。TTFieldsは膠芽腫、悪性胸膜中皮腫、非小細胞肺癌に対する治療として米国や欧州で承認されており、日本でも膠芽腫に対する治療として承認されている。
進行膵癌に対してTTFieldsをGemcitabine+Nab-Paclitaxel療法と併用する第II相試験において忍容性が確認されたため、局所進行膵癌に対してTTFieldsをGemcitabine+Nab-Paclitaxel療法に併用する意義を検討する本試験が行われた。
局所進行膵腺癌を対象とした第III相試験
計20カ国による国際共同ランダム化第III相試験(PANOVA-3試験)であり、対象は組織学的に確認された腺癌で、18歳以上、PS 0-2、前治療歴のない局所進行膵癌患者であった。
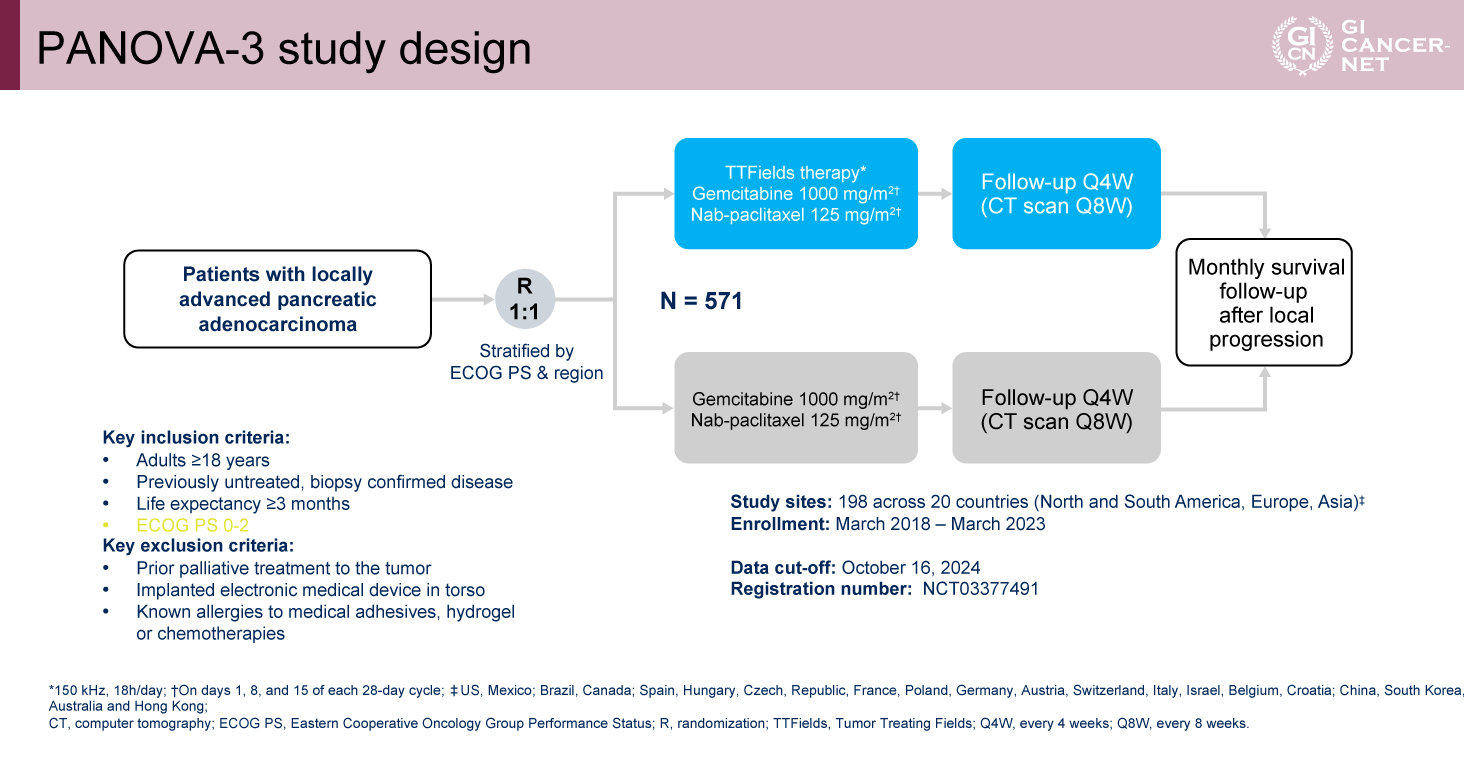
Gemcitabine+Nab-Paclitaxel療法(Gemcitabine 1,000mg/m2、Nab-Paclitaxel 125mg/m2、day1, 8, 15、28日毎)にTTFields(150 kHz、18時間/日)を併用の有無によって1:1にランダム化された(図1)。
主要評価項目は全生存期間(OS)が設定され、副次評価項目としては、無増悪生存期間(PFS)、局所病変のPFS、pain-free survival、1年生存割合、奏効割合、有害事象が評価された。Pain-free survivalはランダム化から疼痛がベースラインより20ポイント以上、視覚的アナログ尺度(visual analogue scale)で上昇するまでの期間と規定された。また事後解析として遠隔転移のPFSも評価された。
図1 PANOVA-3 study design(発表者の許可を得て掲載)
TTFieldsをGemcitabine+Nab-Paclitaxel療法に併用することで有意にOS延長効果を示した
571例(TTFields+Gemcitabine+Nab-Paclitaxel療法群285例、Gemcitabine+Nab-Paclitaxel療法群286例)がランダム化された。Gemcitabine+Nab-Paclitaxel療法群でやや女性の割合が多かったが、そのほかは両群で概ね均等に割り付けられており、年齢は最高で90歳、PS 2も少数(約4%)含まれていた。治療開始前のCA19-9が1,000U/mLを超える割合がTTFields+Gemcitabine+Nab-Paclitaxel療法群30.9%、Gemcitabine+Nab-Paclitaxel療法群27.6%であり、より進行した症例も含まれていることが示唆される。1日あたりのTTFieldsの装着割合は中央値で62.1%であった。
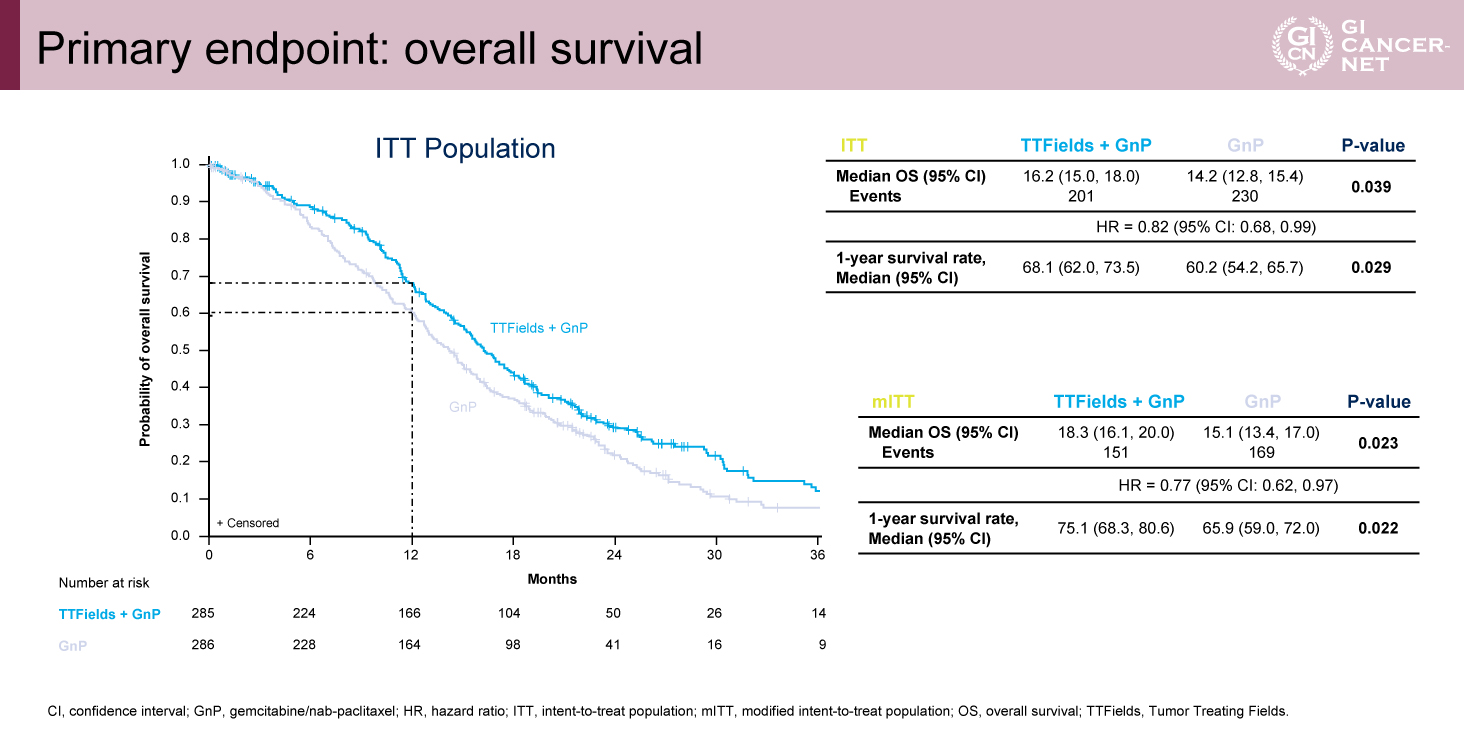
主要評価項目であるOS中央値はGemcitabine+Nab-Paclitaxel療法群14.2カ月に対してTTFields+Gemcitabine+Nab-Paclitaxel療法群16.2カ月(ハザード比[HR]0.82、95%信頼区間[CI]0.68-0.99、p=0.039)であり、Gemcitabine+Nab-Paclitaxel療法に対してTTFields+Gemcitabine+Nab-Paclitaxel療法が統計学的に有意にOS延長効果を示した(図2)。副次評価項目の1年OS割合もTTFields+Gemcitabine+Nab-Paclitaxel療法群68.1%、Gemcitabine+Nab-Paclitaxel療法群60.2%(p=0.029)と有意に良好であった。
そのほかの副次評価項目として、PFS中央値はGemcitabine+Nab-Paclitaxel療法群9.3カ月に対し、TTFields+Gemcitabine+Nab-Paclitaxel療法群10.6カ月(HR=0.85、95% CI: 0.68-1.05、p=0.137)と、統計学的な有意差は示されなかったが、1年PFS割合はTTFields+Gemcitabine+Nab-Paclitaxel療法群43.9%、Gemcitabine+Nab-Paclitaxel療法群34.1%(p=0.026)であり、TTFields+Gemcitabine+Nab-Paclitaxel療法群でPFSも良好な傾向はみられた。同様に、遠隔転移を除いた局所病変のPFSは中央値で12.5カ月 vs 10.4カ月(HR=0.84、95% CI: 0.67-1.06、p=0.151)、1年PFS割合で51.9% vs 41.8%(p=0.027)とTTFields+Gemcitabine+Nab-Paclitaxel療法群で局所病変のPFSも良好な傾向がみられ、事後解析ではあるが、局所病変の増悪を除いた遠隔転移のPFSは中央値、1年PFS割合ともにTTFields+Gemcitabine+Nab-Paclitaxel療法群で有意に良好であった。またPain-free survivalも15.2カ月 vs 9.1カ月(HR=0.74、95% CI: 0.56-0.97、p=0.027)と有意に改善を示した。
有害事象については、大半がGemcitabine+Nab-Paclitaxel療法に関連するものであり両群間で大きな差は認めなかった。TTFields+Gemcitabine+Nab-Paclitaxel療法群では皮膚炎、皮疹、掻痒といった皮膚関連の有害事象が多く認められたが、ほとんどはgrade 2以下で管理可能な範囲であり、装置に関連したgrade 3以上は7.7%であった。
図2 Primary endpoint: overall survival(発表者の許可を得て掲載)
結論
局所進行膵癌において、Gemcitabine+Nab-Paclitaxel療法にTTFieldsを併用することによりOSの有意な延長効果が示された。TTFieldsは本試験の対象に対する新たな治療選択肢になり得ると考える。PFSや局所病変のPFSは統計学的な延長効果は認めなかったものの、事後解析で遠隔転移のPFSは有意な改善を認めた点は興味深く、機序の解明が期待される。Pain-free survivalが有意に改善されている点は患者にとって非常に有意義な指標であり評価されるべきである一方、治療中は常に装置を1日18時間以上も装着していなければならず、皮膚毒性も含めて生活が制限される側面もある。他のレジメンとの併用や局所進行以外の病期でも効果が期待されるのかといった点は今後の検討課題である。
(レポート:国立がん研究センター東病院 肝胆膵内科 佐竹 智行)
関連サイト
・PANOVA-3試験[ClinicalTrials.gov]
寺島 健志先生
金沢医科大学 腫瘍内科 准教授