MATTERHORN試験における無イベント生存期間(EFS):切除可能な胃・食道胃接合部癌(GC/GEJC)に対するDurvalumab+FLOT療法のランダム化第III相試験
Event-free survival (EFS) in MATTERHORN: a Randomized, Phase 3 Study of Durvalumab plus 5-Fluorouracil, Leucovorin, Oxaliplatin and Docetaxel Chemotherapy (FLOT) in Resectable Gastric/Gastroesophageal Junction Cancer (GC/GEJC)
Yelena Y. Janjigian, et al.
監修コメント
近年、胃癌では進行・再発例に対する免疫チェックポイント阻害薬(ICI)の有効性が実証されてきた一方で、周術期治療におけるICIの有効性については明らかではなかった。アジアで標準治療であった術後補助化学療法にNivolumabを併用するATTRACTION-5試験や、術前術後XP/FLOT療法にPembrolizumabを併用したKEYNOTE-585試験(KN-585)は、いずれもネガティブな結果に終わった。そうした中、MATTERHORN試験では中間解析で病理学的完全奏効割合(pCR)の良好な結果が報告され、期待が高まっていた。すでにプレスリリースで報告されていた通り、Durvalumabを周術期FLOT療法へ併用することで、主要評価項目である無イベント生存期間(EFS)の有意な延長が示され、胃癌周術期治療における新たな標準治療の確立が期待された。
サブグループ解析では地域や組織型、PD-L1発現率次第では治療効果が弱まる傾向も示唆されており、今後は適切な患者選択も課題となるだろう。また、免疫関連有害事象(irAE)の発現リスクや、ICIを先行投与することによる再発後治療への影響についても、さらなる議論が必要である。今回、全生存期間(OS)では、ハザード比(HR)0.78(0.62-0.97)と有意差はないものの良好な傾向が示されており、最終解析でのOSの結果にも注目したい。
注目すべきは先に報告されたKN-585との比較である。KN-585では大多数の症例はCapecitabineとCisplatin(XP)による2剤併用療法を受けていたが、FLOT併用コホートに限れば、Pembrolizumab併用群の2年EFS割合はMATTERHORN試験とほぼ同様であった。一方、韓国で行われたPRODIGY試験でも3剤併用術前Docetaxel+Oxaliplatin+S-1(DOS)療法の有効性が示されており、術前DOS+Durvalumabの第II相試験の有望な結果が報告されており、今後、D-FLOT療法など、胃癌周術期化学療法は3剤併用化学療法にICIを併用する治療が主流となっていくと思われる。
中国では、RESOLOVE試験やRESONANCE試験の結果により、術前術後S-1+Oxaliplatin(SOX)療法が標準的治療とされており、これにICIの上乗せ効果を検証する複数の臨床試験(DRAGON IV/CAP 05試験/HLX10-006-GCneo試験)が行われている。また、KN-585ではアジア地域の患者、T4症例、びまん性組織型症例等のICIの上乗せ効果が少ない可能性のある集団がより多く含まれていたことにも留意が必要である。
日本においては、現時点での術前化学療法の適応は、BulkyN2症例など、R0切除の確率が低い症例に限られており、切除可能なものに対しては、まず手術を行い、その後病理診断に基づいて術後化学療法(S-1単剤あるいは、S-1+Oxaliplatin or Docetaxel)を行うことが標準治療とされている。現在進行中のJCOG1509試験では、切除可能症例に対する手術+術後化学療法に対する、術前SOX療法の上乗せ効果が検証されており、数年後に結果が公表される見込みである。さらに、食道胃接合部腺癌に対しては、JCOG2203試験により、術前DOS療法あるいはFLOT療法の有用性が検証されており、現在登録中である。
MATTERHORN試験の結果でいわゆるD-FLOT療法が日本でも1年後に使用可能となる見込みであるが、その時点で日本の標準治療がどのように変化するか、大変興味深いところである。
(国立がん研究センター中央病院 消化管内科/頭頸部・食道内科 科長 加藤 健)
背景
切除可能な周術期進行胃癌に対して、欧米ではMAGIC試験、FLOT4試験の結果から3剤併用による周術期化学療法(FLOT療法:5FU+Leucovorin+Oxaliplatin+Docetaxel、2週毎)が標準治療として確立されたが、さらなる生存向上のための治療開発が試みられてきた1,2)。転移・再発胃癌では免疫チェックポイント阻害薬(ICI)の有効性が実証されているが、周術期化学療法におけるICIの有効性はこれまで明らかではなかった3,4)。ATTRACTION-5試験では、術後補助化学療法へのNivolumabの上乗せ効果は示されず、KEYNOTE-585試験ではXP療法(Capecitabine+Cisplatin)を主とした周術期化学療法へのPembrolizumab併用の意義が検証され、明確な再発抑制効果は示されなかったものの、ICIに対する一定の効果を期待させるものであった5,6)。このような背景の中で、切除可能な胃・食道胃接合部癌の標準治療である周術期FLOT療法に抗PD-L1抗体薬Durvalumabを併用する意義を検証したのが本MATTERHORN試験である。
試験デザイン
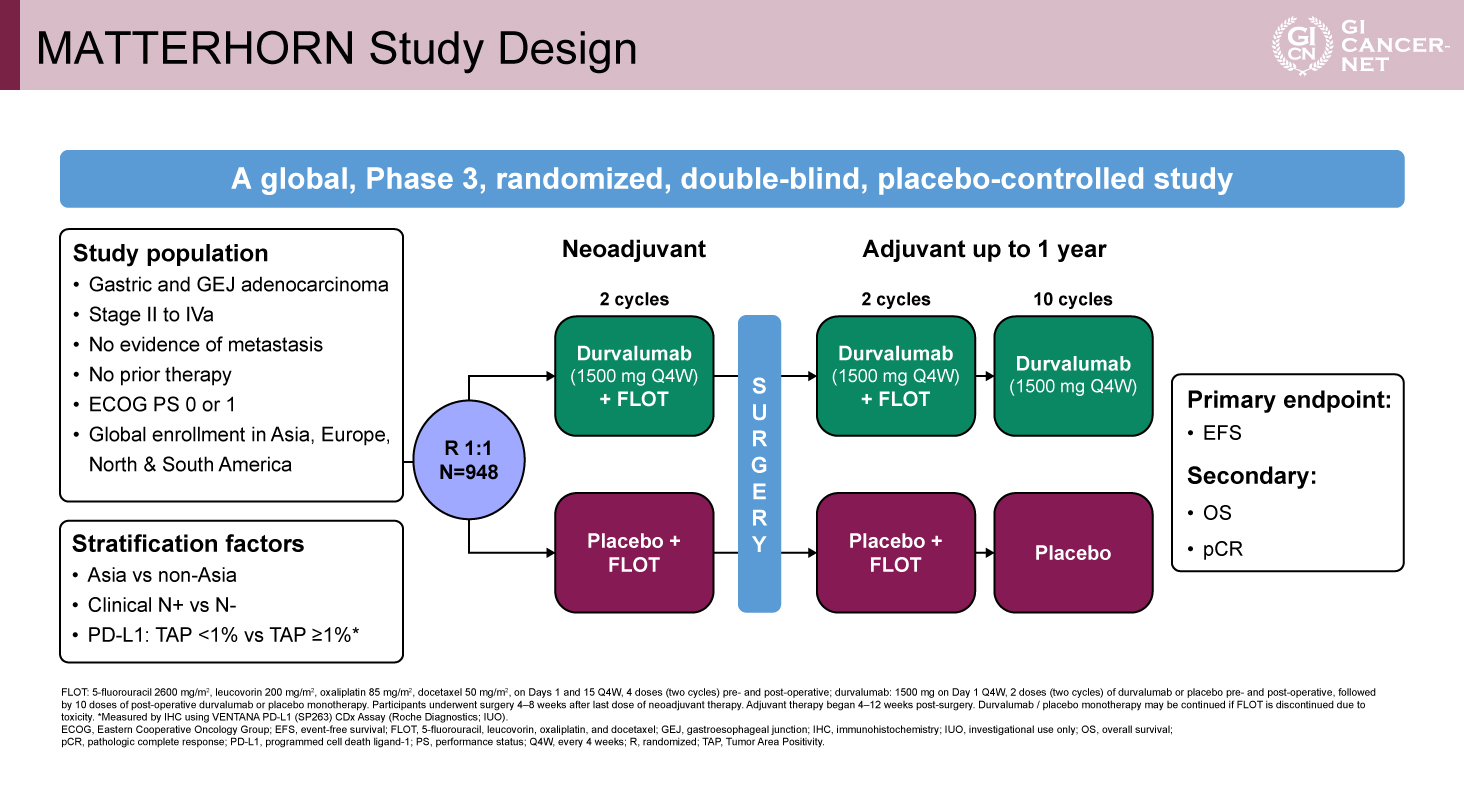
本試験は国際共同第III相プラセボ対照二重盲検ランダム化試験として実施された。対象は、アジア、欧州、北米、南米の計20カ国から登録され、18歳以上で既治療歴がなく、遠隔転移のないStage II-IVaで切除可能なPS 0-1の胃・食道胃接合部癌患者が適格とされた。層別化因子には、アジア/非アジア、リンパ節転移の有無、PD-L1発現(Tumor Area Positivity≧1% vs <1%)を設定し、Durvalumab(1,500mg、4週毎)+FLOT群(Durvalumab併用群)とプラセボ+FLOT群(プラセボ群)に1:1でランダムに割り付けられた(図1)。
両群とも術前にFLOTを2サイクル、術後にFLOTを2サイクル施行し、その後Durvalumabもしくはプラセボは10サイクル継続投与された。主要評価項目は無イベント生存期間(EFS)、重要な副次評価項目として全生存期間(OS)、病理学的完全奏効率(pCR)が設定された。主要解析は全ランダム化集団を対象、層別化ログランク検定によりDurvalumab併用群がプラセボ群に対して優越性を示すかが検証され、主要評価項目に対する有意水準は事前に設定された両側2.39%(p<0.0239)とされた。今回のASCO 2025では予定イベント数の41%に達した時点での第2回中間解析の結果が報告された。
図1 MATTERHORN Study Design(発表者の許可を得て掲載)
Durvalumab併用群はEFSの改善を示した
計948例の患者がDurvalumab+FLOT群(474例)またはプラセボ+FLOT群(474例)にランダムに割り付けられ、薬物治療や手術の完遂率、R0切除率、患者背景は両群でほぼ同様であった(表1、表2)。2割弱がアジアから参加しており、約3割は食道胃接合部原発であった。少数のMSI-high症例も含まれていたが、両群でその割合は同程度であった。
追跡期間中央値31.5カ月時点におけるEFS中央値は、Durvalumab併用群で未達、プラセボ群で32.8カ月であり、Durvalumab群で統計学的に有意なEFSの延長を認めた(ハザード比[HR]0.71、95%信頼区間[CI]0.58-0.86、p<0.001)(図2)。24カ月EFS率はそれぞれ67%、59%であった。サブグループ解析ではおおむね一貫してDurvalumab併用群の有効性を認めたが、女性、アジア地域、リンパ節転移なし、PD-L1低発現、びまん性組織型などでは治療効果が劣る傾向を認めた(表3)。
OS中央値はDurvalumab併用群で未達、プラセボ群で47.2カ月であった(HR=0.78、95% CI: 0.62-0.97、p=0.025)(図3)。事前に規定された有意水準はp<0.0001であるが、成熟度は33.9%であり、最終解析で正式に評価される予定である。
また、pCRはDurvalumab併用群で19%、プラセボ群で7%とDurvalumab併用群で統計学的に有意な改善を認めた(図4)。
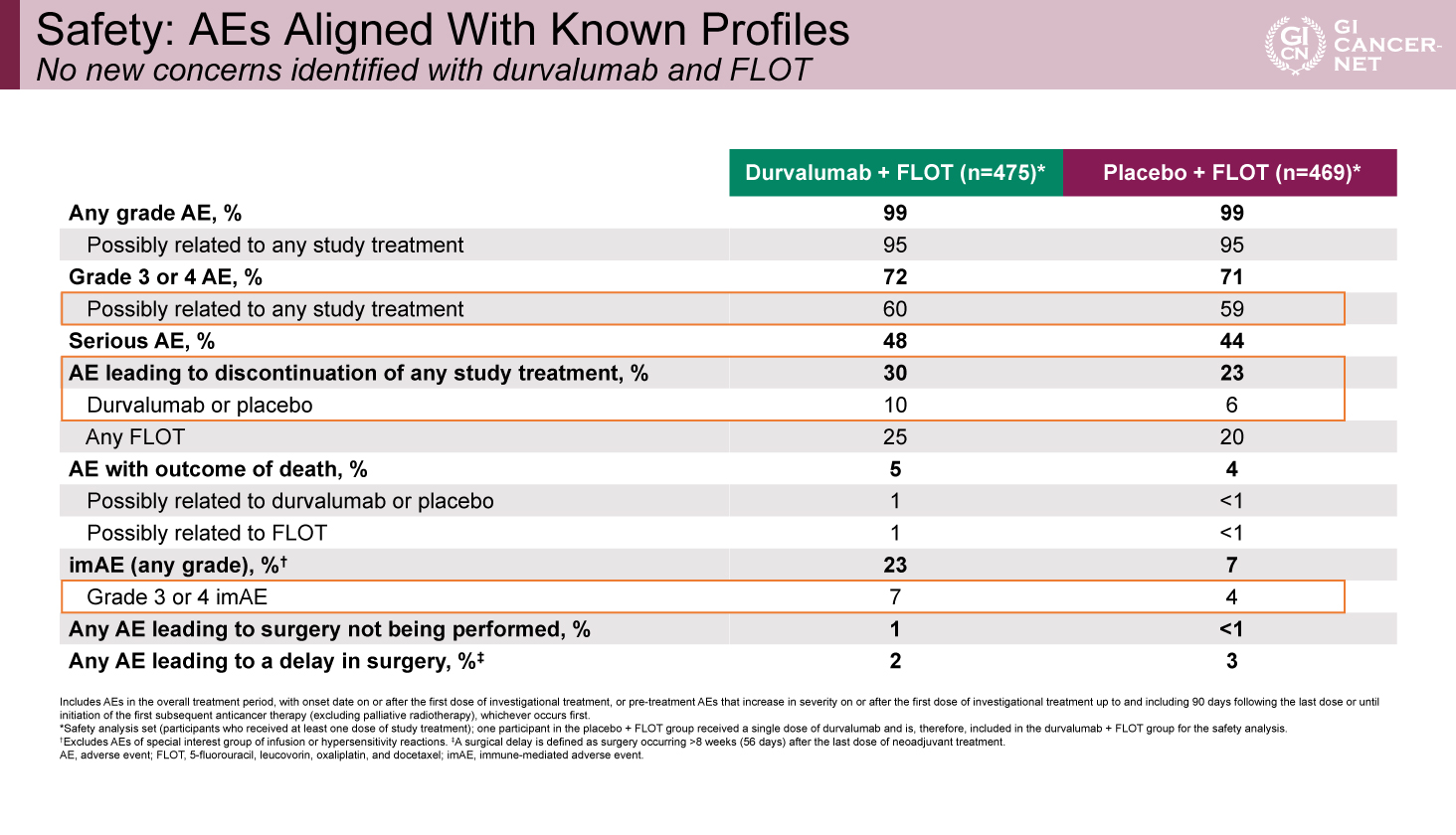
Grade 3/4の治療関連有害事象発現率は両群で同程度であり、FLOTへのDurvalumab併用による新たな安全性上の懸念は認められなかった(表4)。また、主な有害事象のプロファイルも両群でほぼ一致していた。
表1 Participant Disposition(発表者の許可を得て掲載)
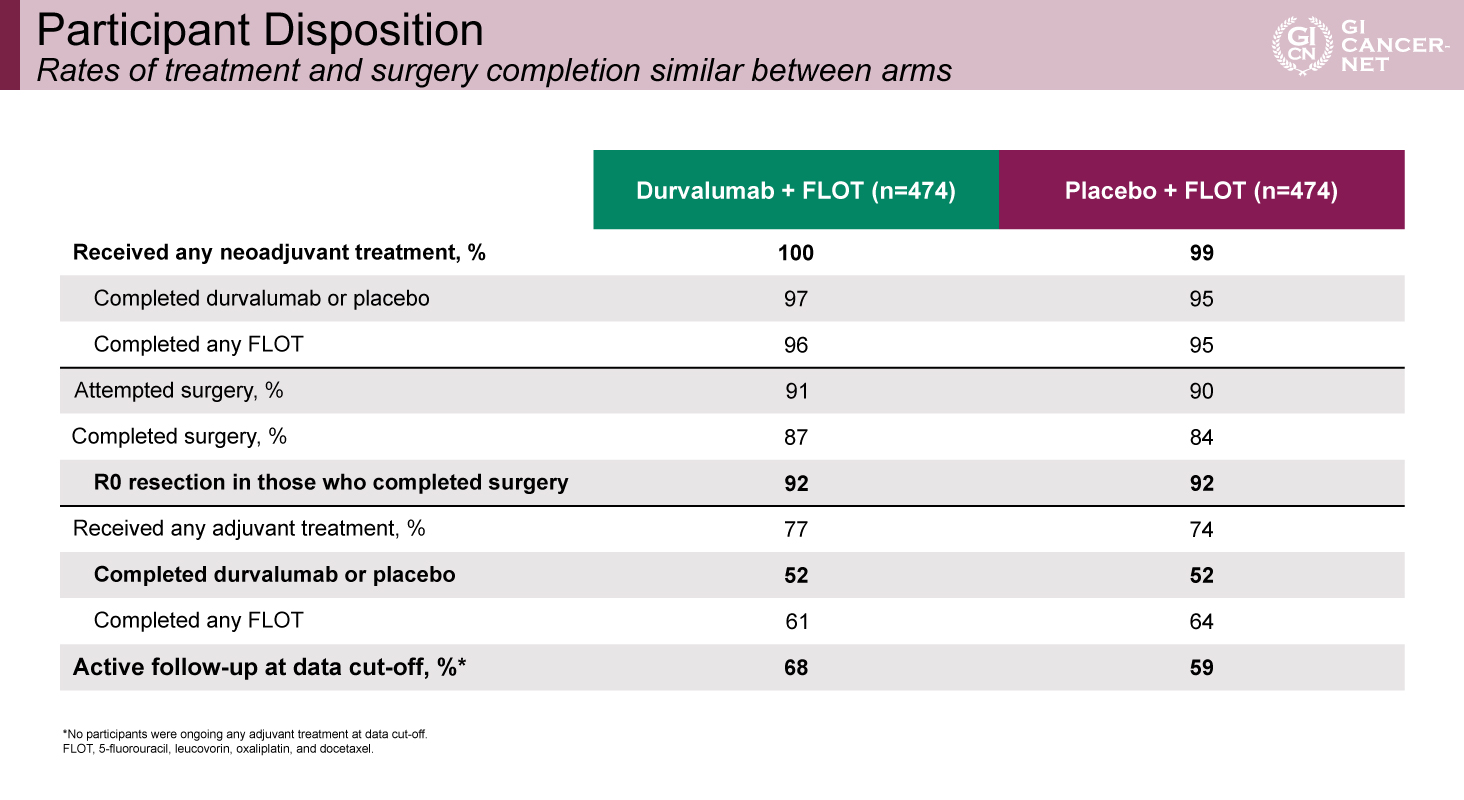
表2 Baseline Characteristics(発表者の許可を得て掲載)
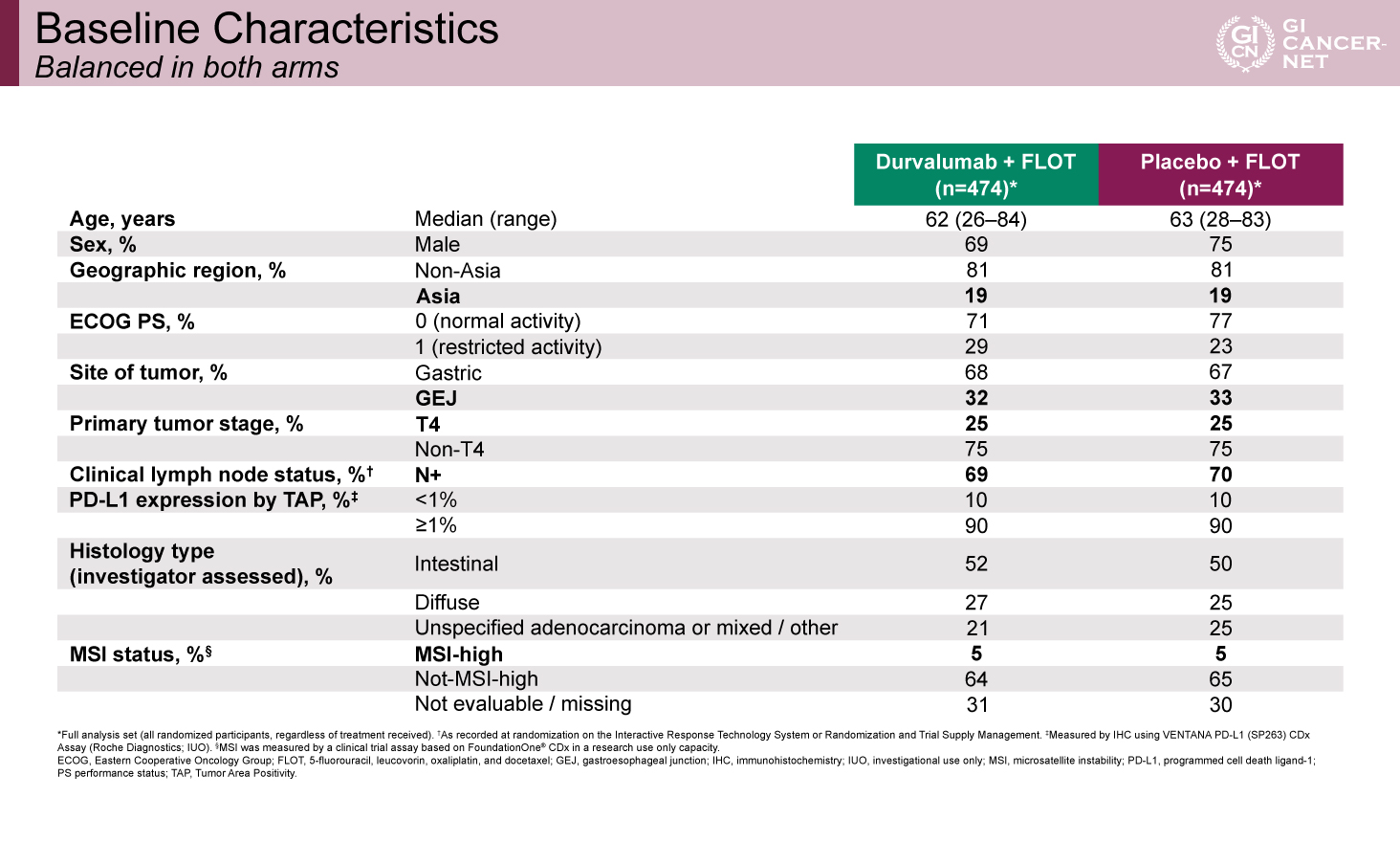
図2 Primary Endpoint of Event-Free Survival (EFS)(発表者の許可を得て掲載)
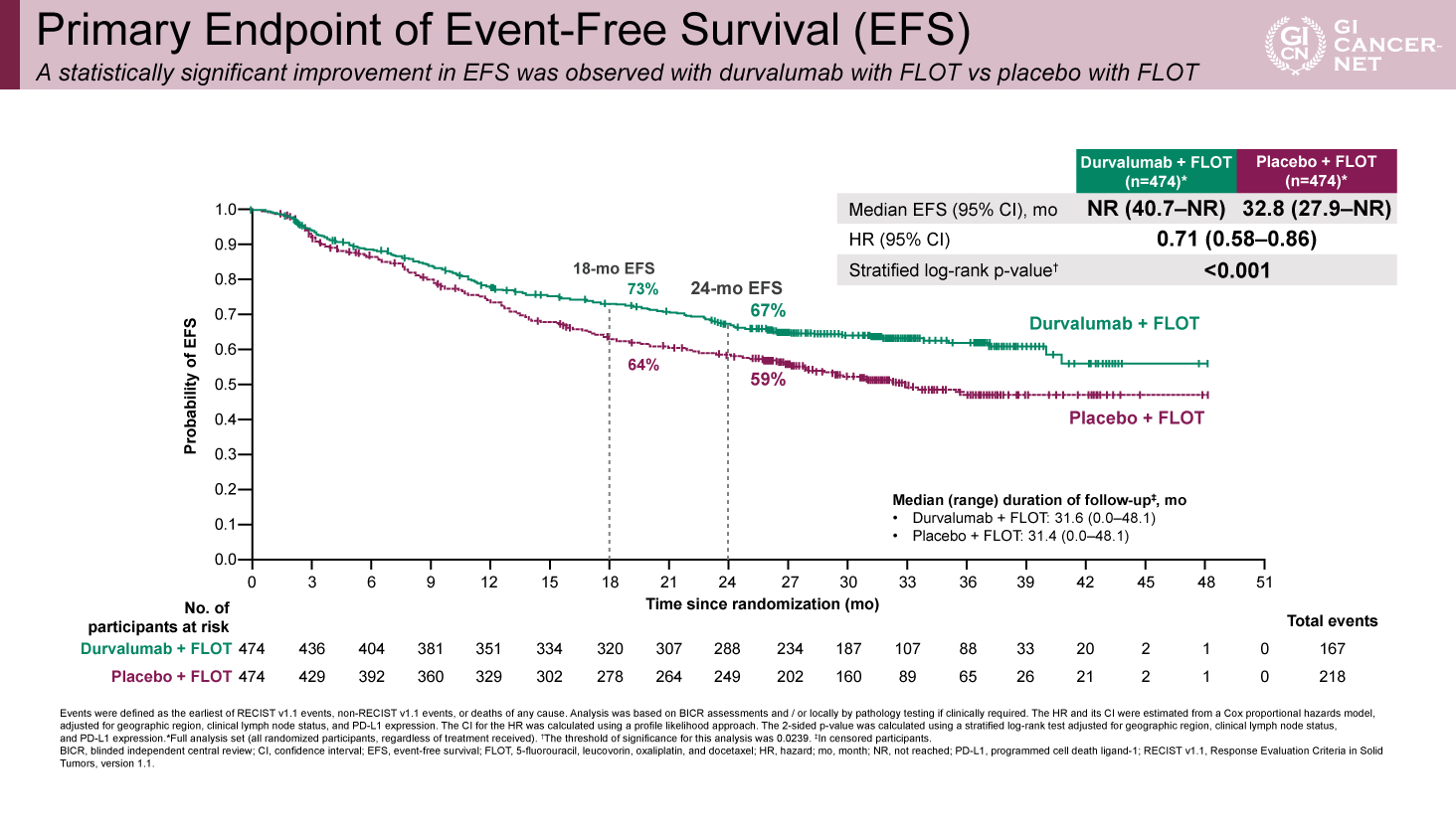
表3 EFS in Key Subgroups: Consistent Benefit Observed(発表者の許可を得て掲載)
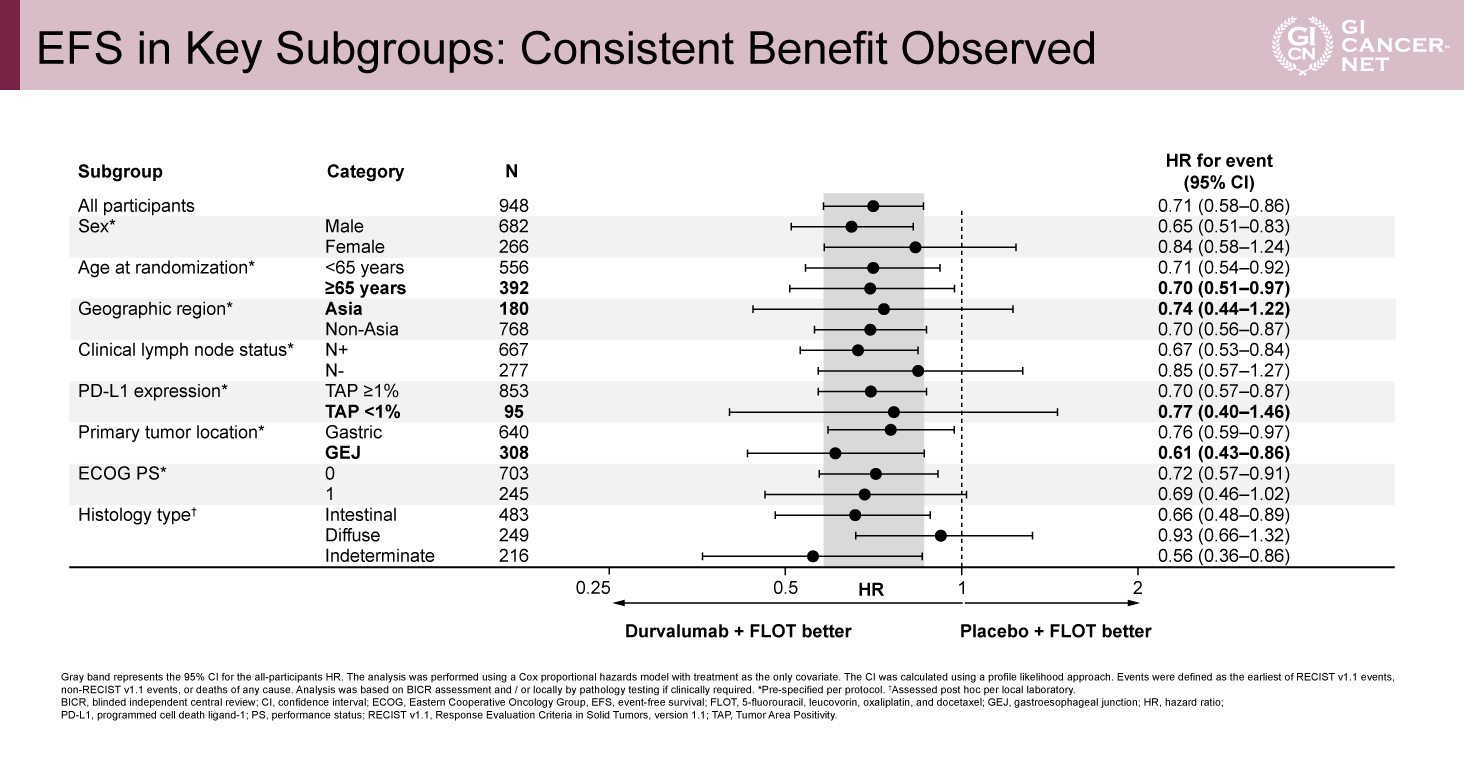
図3 Secondary Endpoint of Overall Survival (OS)(発表者の許可を得て掲載)
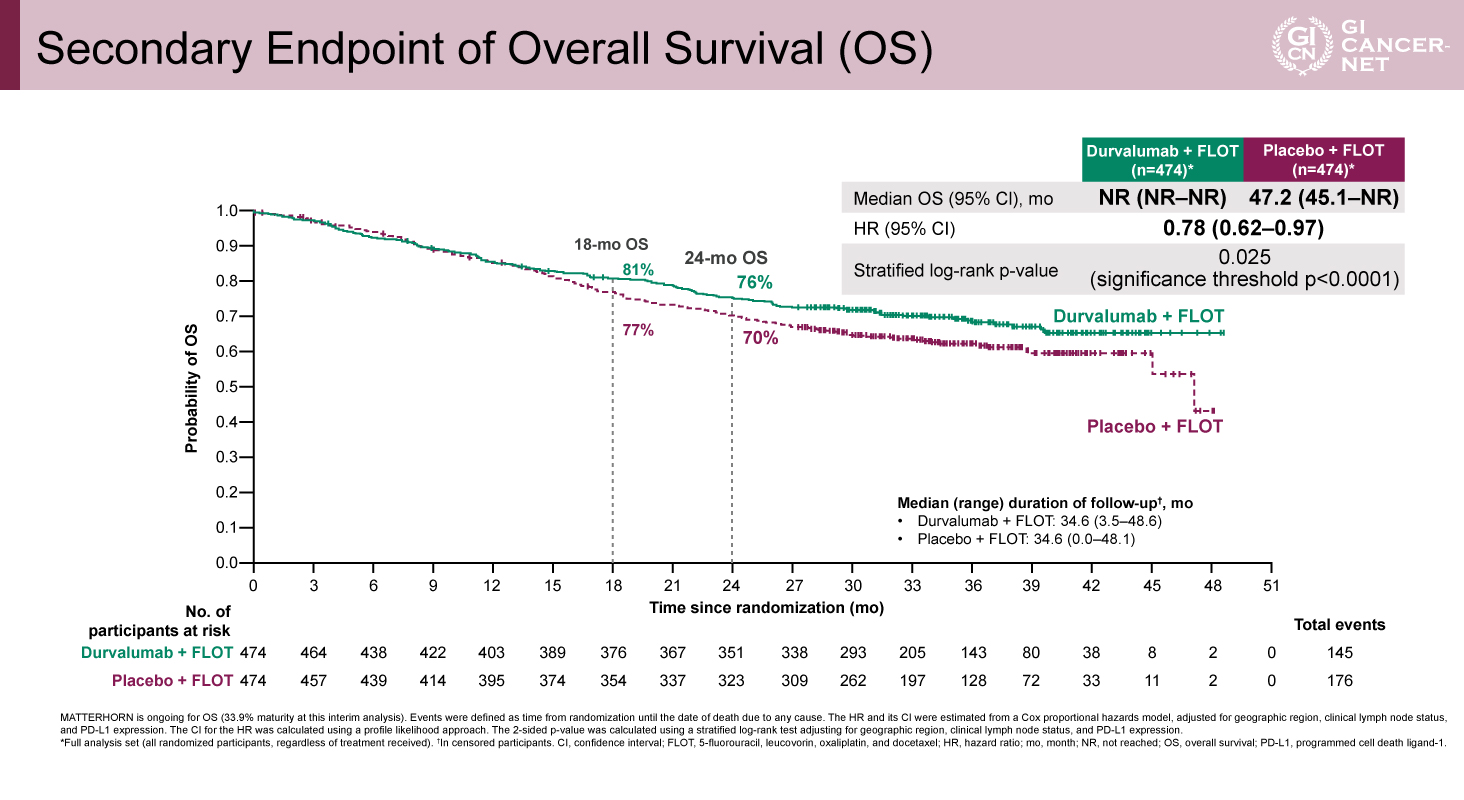
図4 pCR: A Statistically Significant Improvement With the Addition of Durvalumab to FLOT(発表者の許可を得て掲載)
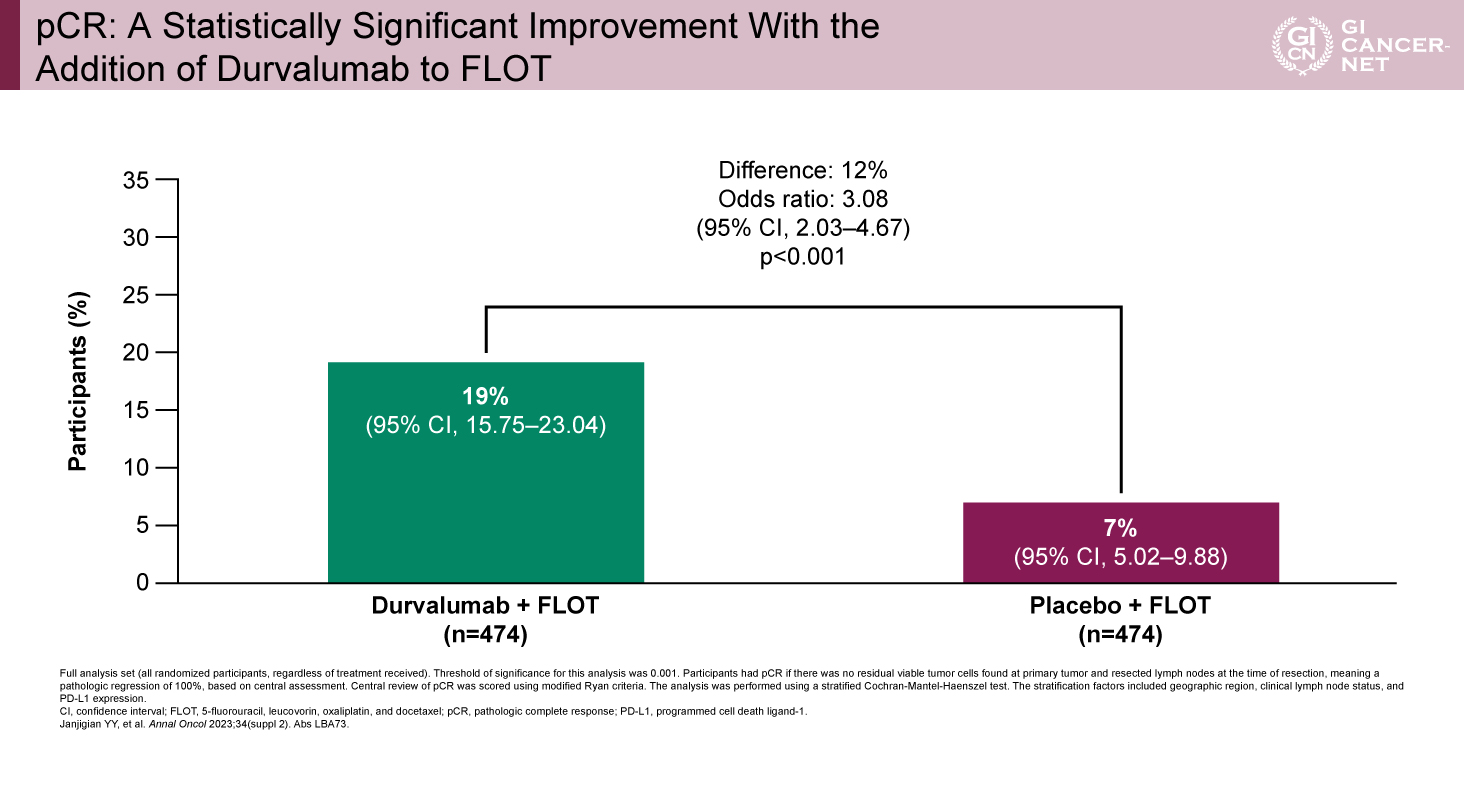
表4 Safety: AEs Aligned With Known Profiles(発表者の許可を得て掲載)
結果
切除可能な胃癌・食道胃接合部癌において、周術期FLOT療法へのDurvalumabの追加はEFSを統計学的に有意に延長し、新たな標準治療の可能性を示した。
(レポート:愛知県がんセンター 薬物療法部 安藤 泰樹)
References
1) Al-Batran SE, et al.: Lancet. 393(10184): 1948-1957, 2019[PubMed]
2) Cunningham D, et al.: N Engl J Med. 355(1): 11-20, 2006[PubMed]
3) Kang YK, et al.: Lancet Oncol. 23(2): 234-247, 2022[PubMed]
4) Rha SY, et al.: Lancet Oncol. 24(11): 1181-1195, 2023[PubMed]
5) Kang YK, et al.: Lancet Gastroenterol Hepatol. 9(8): 705-717, 2024[PubMed]
6) Shitara K, et al.: Lancet Oncol. 25(2): 212-224, 2024[PubMed]
関連サイト
・MATTERHORN試験[ClinicalTrials.gov]
・PRODIGY試験[ClinicalTrials.gov][論文紹介]
・KEYNOTE-585試験[ClinicalTrials.gov][論文紹介]
加藤 健先生
国立がん研究センター中央病院 消化管内科/頭頸部・食道内科 科長