病理学的stage II胃癌に対する術後補助化学療法としてのS-1の投与期間短縮の意義を検討する無作為化第III相試験(JCOG1104 / OPAS-1試験)
A randomized phase III trial comparing 4 courses and 8 courses of S-1 adjuvant chemotherapy for p-stage II gastric cancer: JCOG1104 (OPAS-1)
Takaki Yoshikawa, et al.
監修コメント
本試験は、中間解析の結果より、stage II胃癌に対する術後補助化学療法としてのS-1の投与期間短縮(6ヵ月投与)が、1年投与に対して非劣性を示す可能性が極めて低い(2.9%)ことから、早期無効中止となった。RFS(relapse-free survival)、OSともにイベント数が少ない状況における結果ではあるが、各々のハザード比の95%信頼区間の下限は1を超えており、有意に悪い傾向にある可能性も示された。なお、本試験における1年投与群の3年RFS割合は95.3%と、既報のACTS-GC試験の結果(72.2%)1)と比較して非常に良好であり、もし長期追跡後もこれが維持されるのであれば、その理由についても知りたいところである。いずれにせよ、stage II/III胃癌に対する術後補助化学療法としてのS-1の至適投与期間は1年のままであるとの結果であった。
一方で、stage III胃癌に対するS-1単剤とS-1+Docetaxelを比較した第III相試験(JACCRO GC-07 / START-2試験)は、中間解析の結果、S-1+Docetaxel併用療法のRFSが有意に良好であったことから有効中止となったことが報告されている(http://www.jaccro.com/news/index.html)。詳細の結果はまだ報告されていないが、このSTART-2試験、韓国で実施されたCLASSIC試験2)の結果より、胃癌に対する術後補助化学療法は、stage IIにおいてはS-1単剤(1年投与)、CapeOX(6ヵ月投与)、stage IIIにおいてはCapeOX(6ヵ月投与)、S-1+Docetaxel(1年投与。ただしDocetaxelは18週)が選択肢となり、複雑化することが予想される。今後、これらの治療法を実臨床でどのように使い分けるのが適切か、有用な情報が待たれる。
(コメント・監修:静岡県立静岡がんセンター 消化器内科 医長 山﨑 健太郎)
S-1単剤による術後補助化学療法の至適投与期間は不明
本邦で実施されたACTS-GC試験において、病理学的stage II/IIIの胃癌根治切除例に対する1年間の術後補助S-1療法が手術単独に対して生存期間を改善することが示された1,3)。また、韓国のCLASSIC試験では、同対象に対する6ヵ月間のCapecitabine+Oxaliplatin(CapeOX)の術後補助化学療法が、手術単独に対してRFSの優越性を示し2)、本邦のガイドラインでも標準治療としてCapeOXが加えられたものの4)、S-1単剤が術後補助化学療法の標準治療の1つであることには変わりない。
一方で、1年間という投与期間については背景となる理論的根拠がなく、その期間が妥当であるか否かは不明であり、上記のCLASSIC試験では6ヵ月間の治療で手術に対する優越性が示されている。ACTS-GC試験においても、全体におけるS-1の1年継続割合は65.8%であったことを考慮すると、1年間継続しなくとも同様の結果が得られていた可能性が考えられ、治療期間を短縮しても有効性が変わらないならば、患者負担の軽減および医療費の削減につながる。
ACTS-GC試験において、病理学的stage IIに対する1年間のS-1術後補助化学療法による5年OS割合は84.2%、5年RFS割合は79.2%であり、OSの手術単独に対するハザード比は0.509(95% CI: 0.338-0.765)と良好な成績であった。そのため、病理学的stage II胃癌を対象に、治療期間を6ヵ月に短縮することの非劣性を評価する無作為化第III相試験が行われた。
Stage II胃癌を対象として投与期間短縮の非劣性を検討
主な適格規準は、①組織学的に胃癌と診断されている、②胃癌取り扱い規約第14版での病理学的stage II(T1N2-3およびT3N0を除く)、③D1+以上のリンパ節郭清を伴う胃切除を受け、R0切除が行われている、④20歳以上80歳以下、⑤手術後7週以内に本試験に登録可能である、などであった。
対象は、1年投与群(S-1 80mg/m2, 4週投与2週休薬, 8コース)と6ヵ月投与群(S-1 80mg/m2, 4週投与2週休薬, 4コース)に1:1の割合で無作為に割り付けられた。なお、層別因子は、病理学的stage(IIA vs. IIB)、年齢(70歳未満 vs. 70歳以上)、術式(開腹網嚢切除 vs. 開腹網嚢非切除 vs. 腹腔鏡切除)、施設であった。
主要評価項目はRFSであり、副次評価項目はOS、有害事象、TTF(time to S-1 treatment failure)、時点ごとの治療継続割合であった。両群の3年RFS割合を85%、非劣性マージンを1.37とし、片側α=5%、検出力80%で、予定登録数は1,000例とされた。
中間解析により早期無効中止
2012年2月~2017年3月に590例が登録された段階で、あらかじめ規定された第1回中間解析が実施された。中間解析の対象となった528例において、主要評価項目であるRFSは1年投与群と比べて6ヵ月投与群は有意に不良であり、最終的に6ヵ月投与群が非劣性を示す可能性は2.9%であるとされ、効果安全性評価委員会より早期中止が勧告された。そのため、本試験は早期無効中止となった。なお、患者背景は両群間で偏りはみられなかった。
主要評価項目であるRFSは、3年RFS割合が1年投与群95.3%、6ヵ月投与群88.9%であり、6ヵ月投与群で有意に不良であった(HR=2.52, 95% CI: 1.11-5.77)(図1)。
図1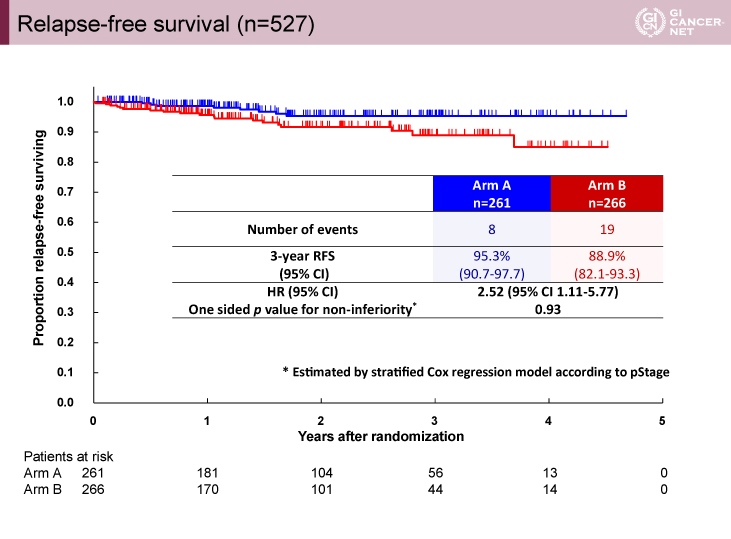
副次評価項目であるOSは、3年OS割合が1年投与群97.7%、6ヵ月投与群91.7%であり、6ヵ月投与群で有意に不良であった(HR=5.18, 95% CI: 1.50-17.89)(図2)。なお、サブグループ解析では、RFS、OSともに、いずれのサブグループにおいても一貫して1年投与群が良好な傾向を認めた。
図2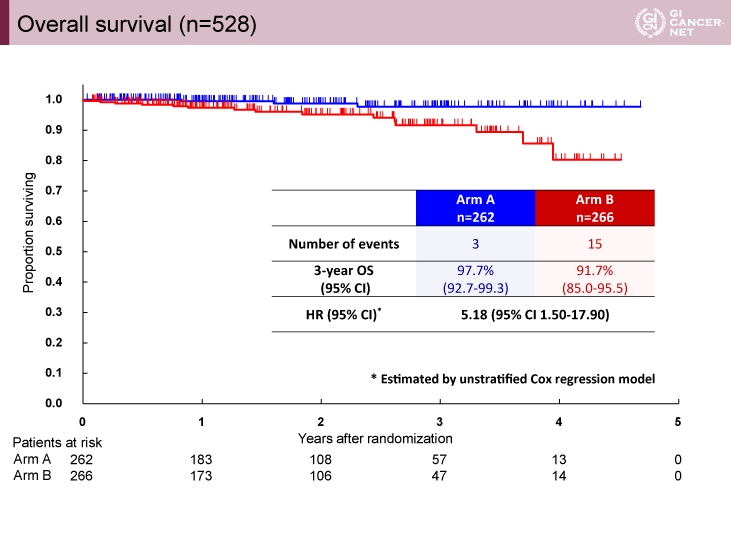
まとめ
病理学的stage II胃癌に対するS-1単剤の術後補助化学療法は、6ヵ月に投与期間を短縮することで、標準治療である1年投与より治療成績が有意に不良であり、本試験は早期無効中止となった。病理学的stage II胃癌に対するS-1単剤の術後補助化学療法は、従来どおり1年継続投与が標準治療である。
(レポート:愛知県がんセンター中央病院 薬物療法部 三谷 誠一郎)

山﨑 健太郎 先生
静岡県立静岡がんセンター 消化器内科 医長