Stage III結腸癌に対するOxaliplatin併用術後補助化学療法の投与期間(3ヵ月 vs. 6ヵ月)に関する無作為化第III相試験(ACHIEVE試験)
Efficacy of 3 versus 6 months of Oxaliplatin-based adjuvant chemotherapy for stage III colon cancer: Results from phase III ACHIEVE trial as part of the international duration evaluation of adjuvant therapy (IDEA) collaboration
Takayuki Yoshino, et al.
監修コメント
ACHIVE試験はIDEA collaborationの6試験の1つであり、2017年米国臨床腫瘍学会年次集会でforest plotのみが提示されていたが、本学会にて初めて有効性に関する詳細な解析結果が発表された。単体試験としては統計学的な症例数設定が行われていないことから、本試験のみで結論を言うことはできない。しかし、1,200例を超える大規模な第III相試験であり、本邦での実地臨床には大いに参考にできる。結果として、IDEA collaboration本体と同様の傾向が示されており、IDEA Recommendationsは本邦においても適用できると考えられる。すなわち、DFS低下のリスクと有害事象軽減のtrade-offを念頭に置いて、再発リスクやレジメン毎に投与期間の短縮が可能、特に低リスク群ではCAPOX 3ヵ月投与へ短縮できると考える。
ACHIEVE試験でなぜCAPOX群の治療成績がFOLFOX群よりも良好なのか、低リスク例におけるT1-2N1とT3N1、高リスク例におけるT4とN2を同様に考えてよいのか、高リスクstage IIや下部直腸癌では補助療法の期間短縮は可能か、など新たな疑問も生じてきた。IDEA collaborationの長期OS結果を待ちつつ、これらの疑問についても一つ一つ解決されることを望む。
(コメント・監修:愛知県がんセンター中央病院 薬物療法部 医長 谷口 浩也)
ACHIEVE試験
ACHIEVE試験は、本邦におけるstage III結腸癌に対する術後補助化学療法としてのFOLFOXまたはCAPOXの投与期間について、6ヵ月間投与と3ヵ月間とを比較した無作為化第III相比較臨床試験であり、本試験は国際共同のIDEA collaborationのひとつである。
本試験は、stage IIIの盲腸から直腸S状部に病変を有する腺癌に対し、根治度Aの手術が施行された患者を対象に、術後補助化学療法として、CAPOXまたはFOLFOX療法を担当医が選択し、標準治療群[6ヵ月群; mFOLFOX6療法(2週毎、12コース)もしくはCAPOX療法(3週毎、8コース)]、または試験治療群[3ヵ月群; mFOLFOX6療法(2週毎、6コース)もしくはCAPOX療法(3週毎、4コース)]に1:1で割り付けられた。なお、mFOLFOX6療法の用量は、Oxaliplatin(85mg/m2, day 1)+bolus 5-FU(400mg/m2, day1)+infusion 5-FU(2,400mg/m2)+l-LV(200mg/m2, day 1)、CAPOX療法の用量はCapecitabine(1,500-2,000mg/m2, day 1夕-15朝)+Oxaliplatin(130mg/m2, day1)であった。
主要評価項目はDFSであり、副次評価項目はOS、TTF(time to treatment failure)、治療完遂率、有害事象であった。なお、本試験は単体試験として統計学的仮説に基づいた症例数設定は行われていない。
IDEA統合解析と再現性のある結果
2012年8月~2014年6月の間に1,313例が登録され、解析対象は1,291例であった。患者背景は、年齢中央値66歳、T stage(T1-2/T3/T4)が15%/57%/28%、N stage(N1/N2)が74%/26%であり、治療レジメンはCAPOX/mFOLFOX6が75%/25%であった1)。IDEAの各試験と比較した場合のACHIEVE試験の特徴として、CAPOXレジメンの割合が6試験中最も高いこと、T4症例の割合が高いことが挙げられた。
主要評価項目であるDFSは、観察期間中央値39.0ヵ月において、3年DFS割合が6ヵ月群77.9%(95% CI: 74.4-80.9)、3ヵ月群79.5%(95% CI: 76.2-82.4)であった(HR=0.95, 95% CI: 0.76-1.20)(図1)。
図1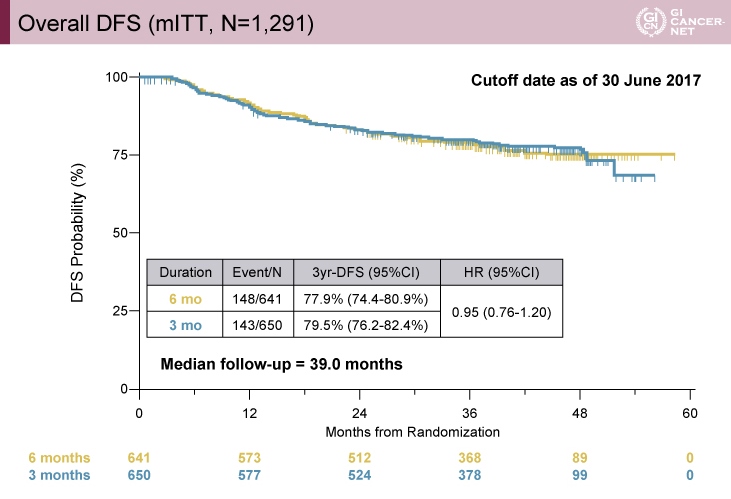
再発リスク別のサブグループ解析では、低リスク群(T1-3かつN1)における3年DFS割合は6ヵ月群87.3%(95% CI: 83.3-90.5)、3ヵ月群90.5%(95% CI: 87.0-93.1)であり(HR=0.81, 95% CI: 0.53-1.24)、高リスク群(T4またはN2)では6ヵ月群66.5%(95% CI: 60.6-71.7)、3ヵ月群65.4%(95% CI: 59.6-70.7)であった(HR=1.07, 95% CI: 0.81-1.40)。
治療レジメン別の解析では、mFOLFOX6群における3年DFS割合は6ヵ月群72.3%(95% CI: 64.5-78.7)、3ヵ月群73.9%(95% CI: 66.4-80.0)であり(HR=1.07, 95% CI: 0.71-1.60)、CAPOX群では6ヵ月群79.7%(95% CI: 75.8-83.1)、3ヵ月群81.4%(95% CI: 77.6-84.6)であった(HR=0.90, 95% CI: 0.68-1.20)。
リスク分類/治療レジメン別の解析は、図2のとおりである。
図2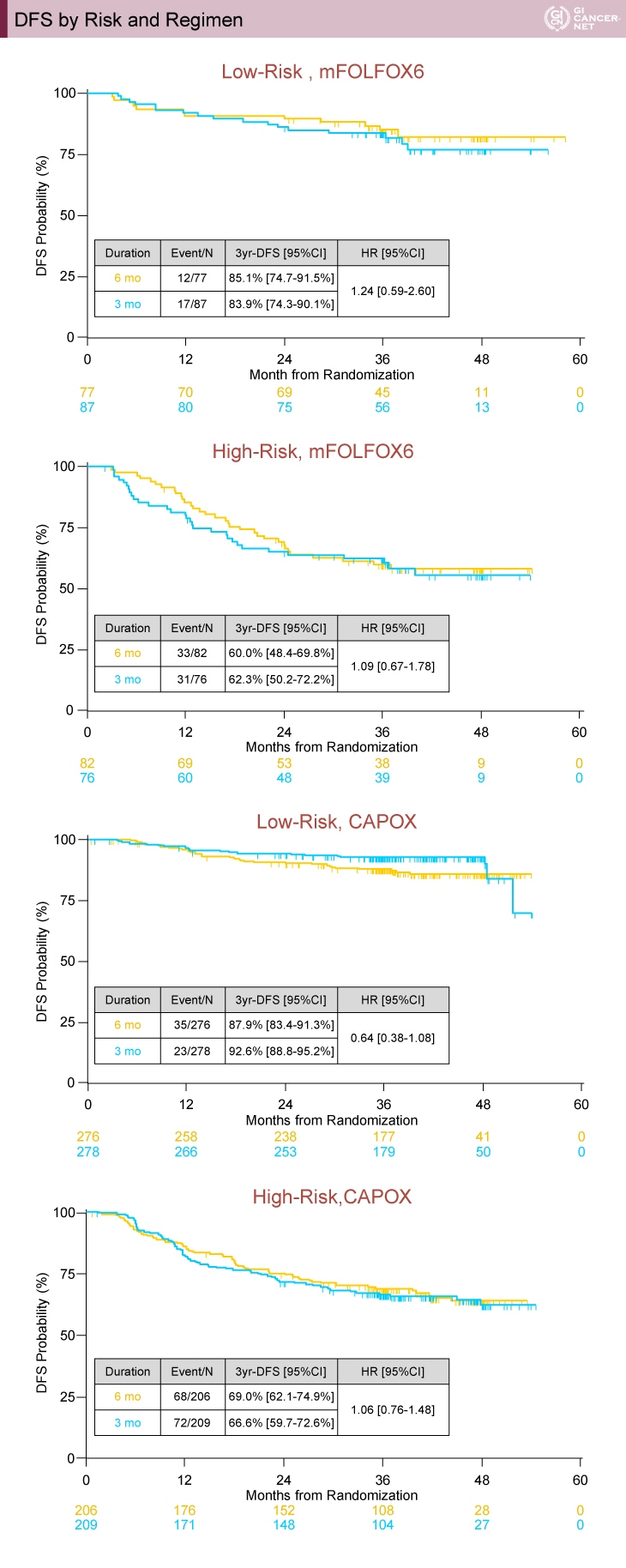
結論
ACHIEVE試験は、アジアで唯一となる、IDEA collaborationの6試験の1つである。治療レジメンやリスク分類に応じて3ヵ月間投与は6ヵ月間投与に劣らない可能性が示唆された。低リスク患者では、3ヵ月間が適切、高リスク患者では6ヵ月の治療期間が必要かもしれない。なお、grade 2以上の神経毒性の発現頻度は、3ヵ月群14%、6ヵ月群37%(p<0.001)、grade 3以上の神経毒性はそれぞれ0.9%、6%(p<0.001)であり、3ヵ月群で有意に低値であった。これらの結果はIDEA統合解析と一致しており、再現性のある結果であった。
(レポート:静岡県立静岡がんセンター 消化器内科 白数 洋充)
Reference
- 1) Shi Q, et al.: 2017 Annual Meeting of American Society of Clinical Oncology®: abstr #LBA1[学会レポート]

谷口 浩也 先生
愛知県がんセンター中央病院 薬物療法部 医長