既治療の切除不能進行・再発胃癌/食道胃接合部癌に対するRivoceranib(Apatinib)+best supportive care(BSC)の有効性を検証する無作為化第III相試験(ANGEL試験)
Randomized phase 3 ANGEL study of rivoceranib (apatinib) + best supportive care (BSC) vs placebo + BSC in patients with advanced/metastatic gastric cancer who failed ?2 prior chemotherapy regimens
Yoon-Koo Kang, et al.
監修コメント
2014年、胃癌に対する分子標的治療薬の開発が進まないなか、ASCOにおいて中国からApatinib単剤での有用性を検証した第III相試験の良好な結果が報告された1)。
本ANGEL試験は中国以外での胃癌に対するApatinibの有効性を検証する国際共同第III相試験であったが、結果はnegativeとなったため、今後本邦においてApatinibを実地臨床で使用することはないだろう。無増悪生存(PFS)期間延長や奏効例が認められ、一定の薬効はあると考えられただけに残念である。
Negativeに終わった要因としては、人種差というよりは、2014年以降、Ramucirumab(Ram)、Nivolumab(Nivo)、FTD/TPI(TAS-102)などの新規薬剤の有効性が示され、日本を含め各国で胃癌の治療体系が変化したことが影響したと考えられる。また、胃癌においてVEGF受容体(VEGFR)を含むマルチキナーゼ阻害剤の有効性は複数報告されているが、ApatinibはVEGFR-2への選択性が高いことから、安全性が高い一方で有効性が今ひとつ物足りなかったのかもしれない。
後治療移行割合(特にNivo)や国・地域別結果の詳細など、今後の続報にも期待したい。
(コメント・監修:国立がん研究センター東病院 消化管内科 医長 谷口 浩也)
Apatinibの進行性胃癌に対する有効性と安全性を検証
Apatinib(Rivoceranib、YN968D1)は、VEGFR-2を選択的に阻害する新規小分子チロシンキナーゼ阻害剤である。二次治療抵抗性進行再発胃癌を対象に中国で実施された第III相試験において全生存(OS)期間のプラセボ群に対する優越性が検証され[Apatinib群:6.5ヵ月(95% CI: 4.8-7.6)vs. プラセボ群:4.7ヵ月(95% CI: 3.6-5.4)、ハザード比(HR)=0.709、p=0.0149]1)、中国ではすでに薬事承認が得られ、実地臨床で使用されている。
今回、中国以外でのApatinibの有効性と安全性を検証するため、国際共同第III相試験としてANGEL試験が行われた。
主要評価項目はOS期間
本試験は、国際共同プラセボ対照無作為化第III相試験であった。2ライン以上の薬物療法に抵抗性の切除不能進行・再発胃癌/食道胃接合部癌患者を、地域、測定可能病変の有無、Ramucirumab(Ram)の投与歴および治療ライン数を割付因子とし、Apatinib群とプラセボ群に2:1に割り付けた。各群はbest supportive care(BSC)に加え、Apatinibおよびプラセボは28日を1サイクルとして、700mgを1日1回連日内服とした。
主要評価項目はOS期間であり、副次評価項目は、無増悪生存(PFS)期間、全奏効割合(ORR)、病勢コントロール割合(DCR)、QOL、安全性であった。既報の結果をもとにOS期間中央値をApatinib群6.5ヵ月、プラセボ群4.7ヵ月(HR=0.72)と期待し、検出力80%、両側α=0.05として目標サンプル数を459例と設定した。
Apatinib群はOS期間の延長を示せなかった
12ヵ国の460例の患者が割り付けられ、Apatinib群308例、プラセボ群152例となった。患者背景は、性別、年齢、ECOG PS(Eastern Cooperative Oncology Group performance status)、原発巣部位(胃癌/食道胃接合部癌)、胃切除の有無、転移臓器数、肝転移の有無などにおいて両群間で差を認めなかった。
主要評価項目であるOS期間の中央値は、Apatinib群5.8ヵ月vs. プラセボ群5.1ヵ月であり、有意差は認めなかった(HR=0.93、95% CI: 0.74-1.15、p=0.485)(図1)。
OS期間のサブ解析では、四次治療以降および肝転移症例においてApatinib群で良好な傾向が認められた(図2)。
副次評価項目であるPFS期間はApatinib群2.8ヵ月vs. プラセボ群1.8ヵ月(HR=0.57、95% CI: 0.46-0.79、p<0.0001)であり、Apatinib群で有意な延長を認めた(図3)。
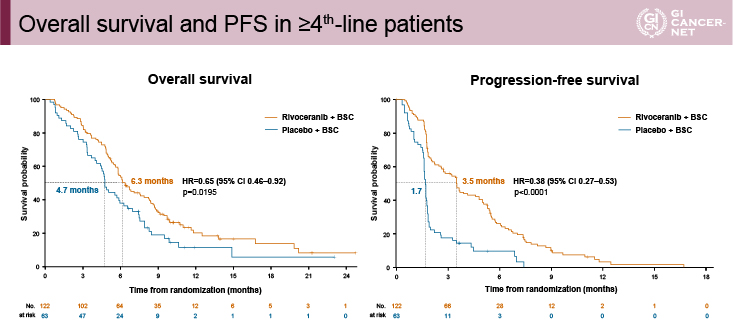
四次治療以降の症例に限った解析では、OS期間中央値がApatinib群6.3ヵ月vs. プラセボ群4.7ヵ月(HR=0.65、95% CI: 0.45-0.92、p=0.0195)であり、Apatinib群で有意な延長を認めた。PFS期間中央値は、Apatinib群3.5ヵ月vs. プラセボ群1.7ヵ月(HR=0.38、95% CI: 0.27-0.53、p<0.0001)であった(図4)。
ORRはApatinib群6.9% vs. プラセボ群0%(p=0.002)、DCRは同様に42.4% vs. 13.1%(p<0.0001)であり、Apatinib群で有意に高かった。
また、Apatinib群において20%以上にみられた有害事象のうち高頻度の発現は、高血圧(34.2%)、尿蛋白(29.3%)、手足症候群(26.4%)であった。
図1 Overall survival(発表者の許可を得て掲載)
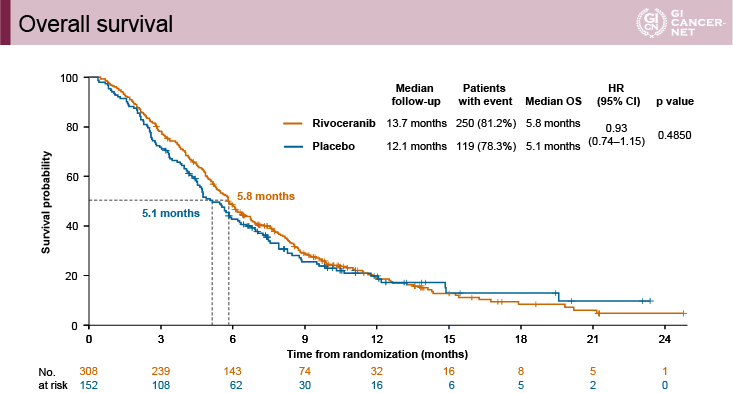
図2 Overall survival - subgroup analysis(発表者の許可を得て掲載)
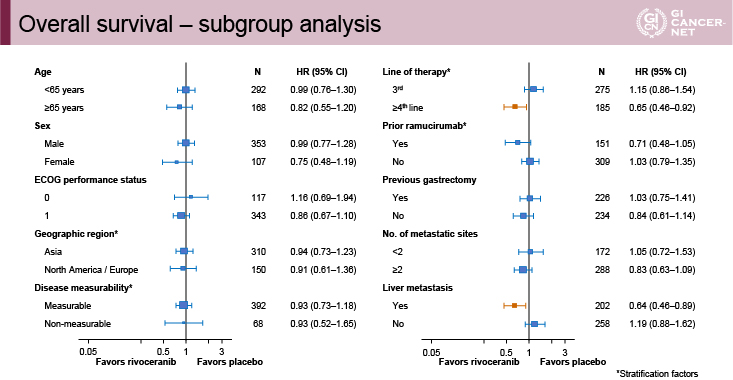
図3 Progression-free survival (central review)(発表者の許可を得て掲載)
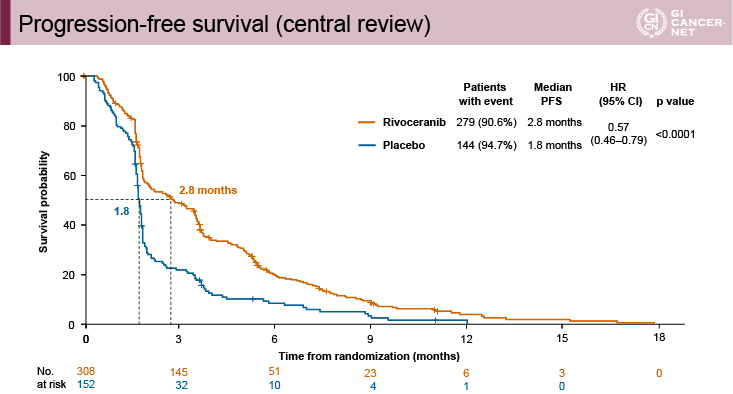
図4 Overall survival and PFS in ?4th-line patients(発表者の許可を得て掲載)
まとめ
Apatinib群は、主要評価項目であるOS期間では有効性を示すことができなかった。PFS期間、ORR、DCRはApatinib群で有意に良好であり、有害事象も忍容可能であった。四次治療以降の症例に限ればOS期間、PFS期間ともにApatinib群で有意に延長が認められた。切除不能進行・再発胃癌/食道胃接合部癌において、Apatinibの一定の有効性が示唆された。
(レポート:国立がん研究センター東病院 消化管内科 三島 沙織)
Reference
- 1) Li J, et al.: J Clin Oncol. 34(13): 1448-1454, 2016 [PubMed]
関連サイト
- ・ANGEL試験 [ClinicalTrials.gov]

谷口 浩也 先生
国立がん研究センター東病院 消化管内科 医長