切除不能進行・再発大腸癌の一次化学療法における、Oxaliplatin(OX)計画的追加+CapecitabineまたはFluorouracil(5-FU)+Bevacizumab(Bmab)療法vs. 初回OX併用+5-FU+Bmab療法の検討:C Cubed Study(C3)
Randomized phase III study of sequential treatment with capecitabine or 5-fluorouracil (FP) plus bevacizumab (BEV) followed by the addition with oxaliplatin (OX) versus initial combination with OX+FP+BEV in the first-line chemotherapy for metastatic colorectal cancer: The C-cubed study (C3)
Takeshi Nagasaka, et al.
監修コメント
大腸癌に対するFluorouracil(5-FU)、Oxaliplatin(OX)、Bevacizumab(Bmab)の3剤を使用した併用療法について、その使い方の治療戦略を検証した本邦で行われた第III相試験の結果である。切除不能進行・再発大腸癌の日常臨床では、key drugの1つであるOXに関連した末梢神経障害がいつも問題となる。OXの使用で用量蓄積性に末梢神経障害の発現率が高くなり、毒性が長く継続する場合も多いことから、QOLに影響するとても重要な毒性である。本試験では、一次治療において、OXの使用を控え計画的に追加使用する治療戦略が、標準的に使用される併用療法より有用性が高いかどうかが検証された。
結果として、主要評価項目のtime to failure of strategy(TFS)はA群(wait & go)がB群(stop & go)よりも有意に優れており、末梢神経障害の発現割合が低く、B群よりも全奏効割合(ORR)が低いものの病勢コントロール割合(DCR)が90%もあることが示された。2群のTFS中央値は、それぞれ15.2ヵ月と7.6ヵ月であり、個人的に2群の差が想像以上に大きいと感じた。B群(stop & go)では、計画的stop後に病勢進行(PD)となった際、OXを再導入するよりも後治療へ移行したケースが多い可能性はないかについて、今後の追加報告や論文発表を参照したい。
3剤が耐性となる無増悪生存(PFS)期間は2群で差がなく、A群は全生存(OS)期間でも劣っていなかった。本試験では、ECOG PS(Eastern Cooperative Oncology Group performance status)0の症例は80~85%登録されていた。本邦の大腸癌治療ガイドラインでは、vulnerable(薬物療法の適応に問題がある)症例に対して5-FU+Bmabが一次治療のpreferred regimenとして推奨されているが、本試験では多くの症例がfit(薬物療法の適応となる)症例であった。すなわち、wait & goは日常臨床で考慮できる治療オプションとなり得るであろう。ドイツのAIOが行ったXELAVIRI(KRK0110)試験では、5-FU+Bmab followed by Irinotecan(IRI)併用療法とCAPIRI[Capecitabine(Cape)+Irinotecan(IRI)]/FOLFIRI[5-FU+Leucovorin(LV)+IRI]+Bmab併用療法の非劣性が検証され、5-FU+Bmab群の非劣性は証明されなかった。しかしながら、KRAS/BRAF遺伝子のサブ解析において、KRAS遺伝子変異型症例ではこの5-FU+Bmab群の非劣性が示されていた1)。本試験では、全体の症例の50%以上がRAS遺伝子変異型であり、この患者背景も結果にpositiveに働いた可能性があるのかもしれない。
(コメント・監修:聖マリアンナ医科大学 臨床腫瘍学 准教授 砂川 優)
未治療切除不能進行・再発大腸癌に対する最適治療戦略を検証
C Cubed Studyは、未治療の切除不能進行・再発大腸癌に対する最適な治療戦略を検証した試験である。すなわち、フッ化ピリミジン系薬剤であるFluorouracil(5-FU)+Bevacizumab(Bmab)を先行し、初回病勢進行(PD)時にOxaliplatin(OX)+5-FU+Bmabへと変更する群(A群:OX “wait & go”)の、OX+5-FU+Bmab群(B群:OX “stop & go”)に対する優越性を検証した。
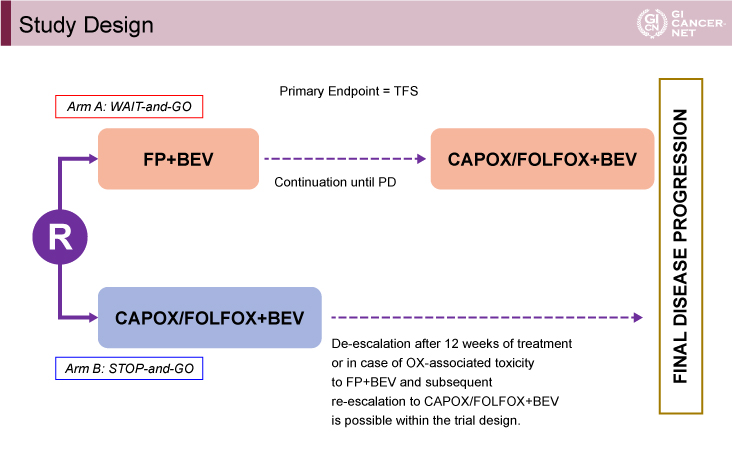
対象は、ECOG PS(Eastern Cooperative Oncology Group performance status)0-2の未治療切除不能進行・再発大腸癌とした。A群は5-FU+Bmabで開始し、PD確認後にOX+5-FU+Bmabとする「wait & go」群、B群はOX+5-FU+Bmabで開始し、12週投与後OXを計画的に中止後PD確認時にOXを再導入しPDまで継続する、または、OX不耐中止後5-FU+BmabでPDまで継続する「stop & go」群とした(図1)。検出力80%、両側有意水準5%と仮定し、B群に対するA群のTFSのハザード比(HR)を0.69未満と期待し、必要な症例数は304例と算出した。
図1 Study Design(発表者の許可を得て掲載)
主要評価項目はtime to failure of strategy(TFS)
主要評価項目はtime to failure of strategy(TFS)、副次評価項目は無増悪生存(PFS)期間、全生存(OS)期間、全奏効割合(ORR)、安全性、QOLであった。TFSは、OX含有レジメンの中止までの期間を検証するために設定された。初回レジメンに使用していない薬剤追加、全薬剤使用中のPD、死亡をイベントと定義し、A群(wait & go)においてはOXを導入できなかった場合、センサーと定義した。
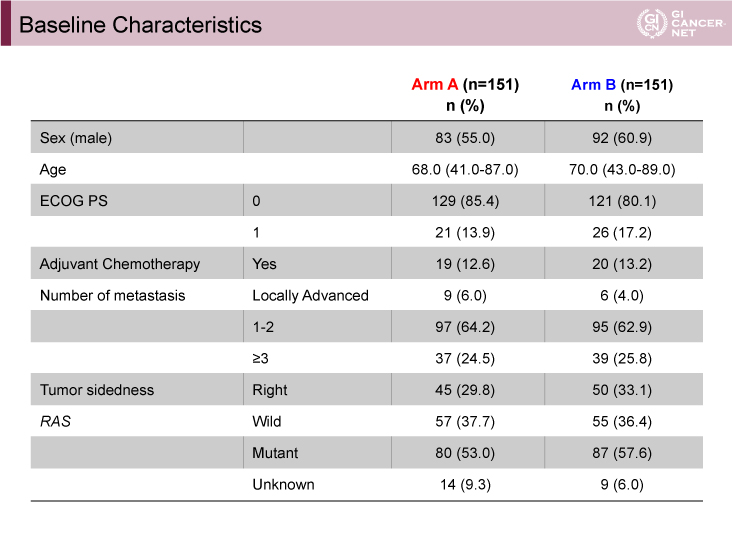
2014年12月?2016年9月に311例が登録され、302例が無作為化された。FAS(Full Analysis Set)はA群(wait & go)、B群(stop & go)で各151例であった。患者背景は両群間で偏りを認めなかった(表1)。
表1 Baseline Characteristics(発表者の許可を得て掲載)
TFSにおいて、B群(stop & go)に対するA群(wait & go)の優越性が示された
主要評価項目のTFSは、A群(wait & go)15.2ヵ月vs. B群(stop & go)7.6ヵ月(層別解析HR=0.474、95% CI: 0.362-0.623、層別log-rank検定p<0.0001)であり、B群(stop & go)に対するA群(wait & go)の優越性が示された(図2)。
OS期間は、A群(wait & go)27.5ヵ月vs. B群(stop & go)29.4ヵ月(層別解析HR=0.930、95% CI: 0.666-1.298、層別log-rank検定p=0.6692)であり、両群間で有意差を認めなかった(図3)。
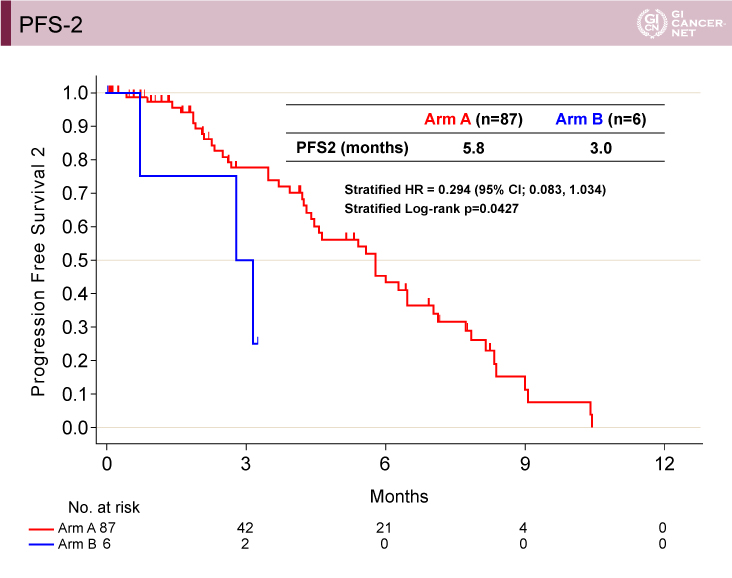
PFS-1[治療開始日?初回PD確認または死亡日(PD1)]は、A群(wait & go)12.0ヵ月vs. B群(stop & go)12.9ヵ月(層別解析HR=1.281、95% CI: 0.912-1.798、層別log-rank検定p=0.1514)であり、PFS-2(PD1?PD2)は、A群(wait & go)5.8ヵ月vs. B群(stop & go)3.0ヵ月(層別解析HR=0.294、95% CI: 0.083-1.034、層別log-rank検定p=0.0427)であった(図4、図5)。
ORR、DCRはA群(wait & go)vs. B群(stop & go)でそれぞれ、33.1% vs. 51.0%、90.7% vs. 85.4%であった。
Grade 3以上の有害事象は、好中球数減少、末梢神経障害、高血圧などがB群(stop & go)で多い傾向にあったが、その他の有害事象は両群間で偏りを認めなかった。
図2 Time to Failure of Strategy (TFS)(発表者の許可を得て掲載)
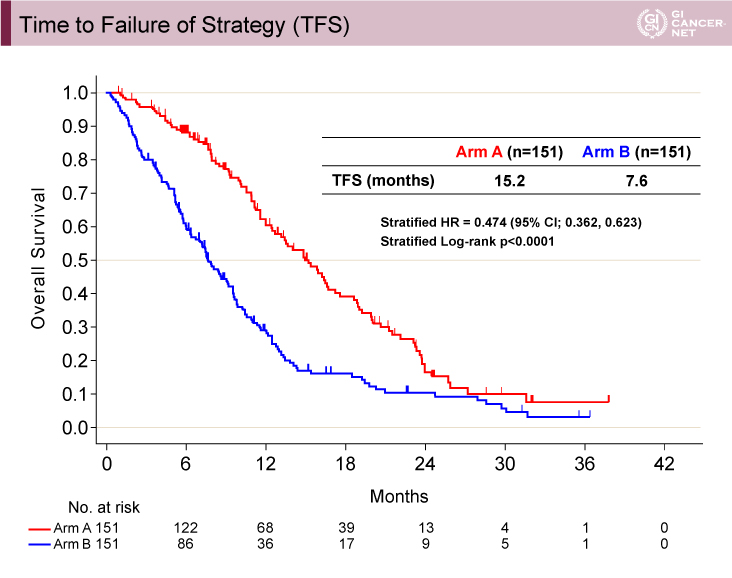
図3 Overall Survival (OS)(発表者の許可を得て掲載)
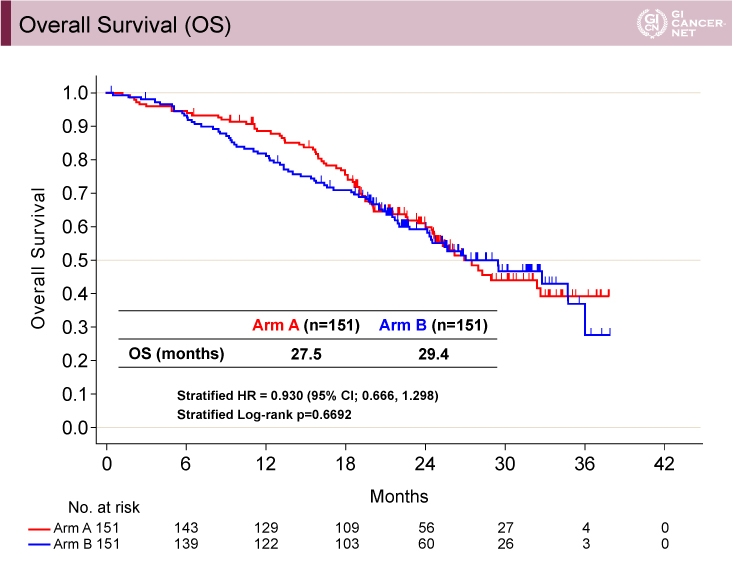
図4 PFS-1(発表者の許可を得て掲載)
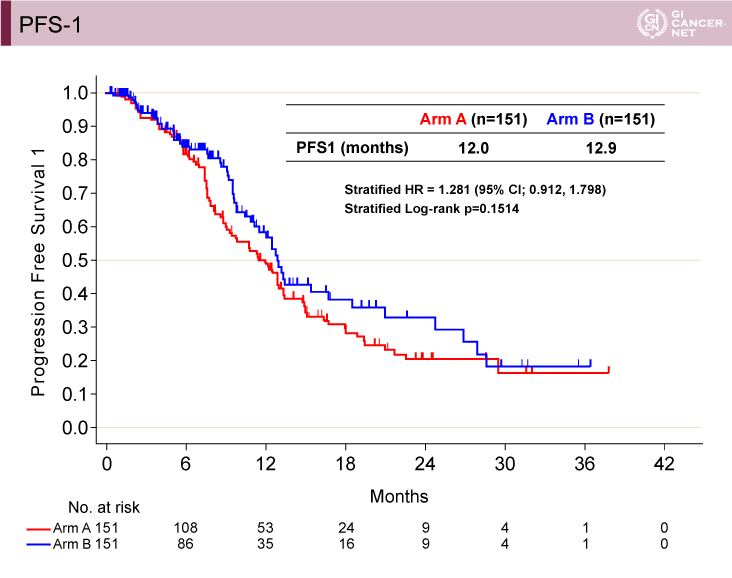
図5 PFS-2(発表者の許可を得て掲載)
まとめ
OXのwait & goは、stop & goに対するTFSの優越性を示し、OS期間は同等であった。OXのwait & goは切除不能進行・再発大腸癌に対する治療戦略の1つとして許容される。
(レポート:静岡がんセンター 消化器内科 川上 武志)
Reference
- 1) Modest DP, et al.: J Clin Oncol. 37(1): 22-32, 2019 [PubMed]
関連サイト
- ・C Cubed Study [UMIN-CTR][PubMed]
- ・XELAVIRI試験(AIO KRK0110/ML22011) [ClinicalTrials.gov][学会レポート(ESMO 2017 #486O)]

砂川 優 先生
聖マリアンナ医科大学 臨床腫瘍学 准教授