血中循環腫瘍DNA(ctDNA)に基づくStage II結腸癌の術後補助化学療法(DYNAMIC試験)
Adjuvant chemotherapy guided by circulating tumor DNA analysis in stage II colon cancer: The randomized DYNAMIC Trial
Jeanne Tie, et al.
監修コメント
「ctDNA」「リキッドバイオプシー」という言葉も陳腐なものになってきて飽き飽きしている読者も多いだろう。しかし、本試験は、ctDNA結果に基づく補助療法実施と従来の治療選択とを比較した初めてのランダム化比較試験であり、今までの報告とは一線を画す。そのため、検証的な第III相試験ではないにもかかわらず、発表当日にNew England Journal of Medicineにpublishされており、本試験の価値がすでに認められている1)。
本試験では、ctDNA結果に基づく補助療法の実施は、再発率を損ねることなく、補助療法の実施率を下げることができる可能性が示唆された。無駄な補助療法を減らすことができ、患者あるいは社会全体へのベネフィットは大きい。一方で、臨床病理学的な再発高リスク因子から補助療法の実施を判断する従来法を上回る治療成績が示されなかった点は、少し残念である。ctDNA陰性で臨床的に再発高リスクの患者は本試験では補助療法が実施されていなかったことが足を引っ張ったのかもしれない。ctDNAアッセイという新しい検査を活用するには、従来の再発リスク因子とctDNAステータスを合わせて考える必要性を示唆している。
ctDNA陽性でどのような補助療法が最適か、ctDNA陰性例では本当に補助療法をしなくても良いのか、については本試験デザインとは異なるが、ctDNA陽性例、陰性例でのランダム化比較試験が必要である。世界中で臨床試験が行われており、本邦でも、CIRCULATE-Japanの中で、VEGA試験やALTAIR試験が患者集積中である2)。また、補助療法への新しい治療も開発中で、今回のASCOでは膵癌でがんmRNAワクチンの有効性が示唆される画期的な発表があった(#2516)3)。新しい補助療法の時代は確実に近づいている。
(愛知県がんセンター 薬物療法部 医長 谷口 浩也)
Stage II結腸癌においてctDNA検査を活用したさらなる再発リスク層別が期待されている
術後補助化学療法の臨床試験においてStage II全体での生存率を改善した報告はなく、その有効性は確立されていない。ガイドラインでは、壁深達度T4など再発高リスク因子が定義され、術後補助化学療法の実施が推奨されているが、再発高リスク群でもその有効性は中等度(5%未満)である。そのため、恩恵を受ける集団に限って補助化学療法を実施し、再発低リスクには補助療法を実施しないという、より洗練された再発リスク層別が求められている。
根治治療後のctDNA検査により、微小残存腫瘍(MRD)の検出が可能であり、ctDNA陽性例で術後補助療法を行わない場合には80%を超える再発率が報告されている4)。しかし、ctDNA陽性例への術後補助化学療法の有効性は確立されていない。DYNAMIC試験は、ctDNAに基づく治療戦略が、既存の治療戦略に対して、生存性を損なうことなく、補助化学療法を受ける患者を減らすことができるかを明らかにすることを目的としたランダム化第II相試験である。
ctDNA-Guided Management vs. Standard Managementのランダム化第II相試験
本試験は、治癒切除されたStage II結腸癌を対象に、従来の臨床病理学的な再発リスク因子に基づき担当医判断で補助療法が実施される群(Standard Management:標準治療群)に対するctDNA結果に基づき補助療法が行われる群(ctDNA-Guided Management:ctDNA治療群)の再発率に対する非劣性を探索する多施設ランダム化比較第II相試験である。主な適格基準は、治癒切除されたStage IIの結腸癌、術後4週以内に腫瘍組織検体を提出できた、8週以内のCTで遠隔転移を認めない症例であった。ctDNA解析は、大腸癌で頻度が多いとされる15遺伝子を対象に腫瘍組織を用いた遺伝子解析にて患者固有の遺伝子異常が同定され、以後その遺伝子異常を対象にctDNA解析(Safe-Sequencing System)が行われた。ctDNAは、術後4週および7週に評価され、ctDNA治療群と標準治療群に2:1で割り付けされた。ctDNA治療群では、術後4週/7週いずれかのctDNA陽性の場合にはOxaliplatin(OX)併用またはFP単独による補助療法が実施され、いずれもが陰性の症例は無治療で経過観察されることを原則とした。標準治療群では、ctDNA検査の結果は知らされず、従来の臨床病理学的なリスク評価により担当医判断で補助療法が実施された。主要評価項目は2年無再発生存(RFS)率で、主たる副次評価項目は補助化学療法実施率であった。また、他の副次評価項目として、ctDNA治療群におけるctDNAステータス別の2年RFS率、再発までの期間、OSが評価された。検出力80%、α=0.05、2年RFS率の95%信頼区間の下限が-8.5%までであれば非劣性が許容されるとし、10%の脱落を考慮して、目標症例数は450例と設定された。
ctDNA治療群における補助化学療法実施率は標準治療群の約55%であった
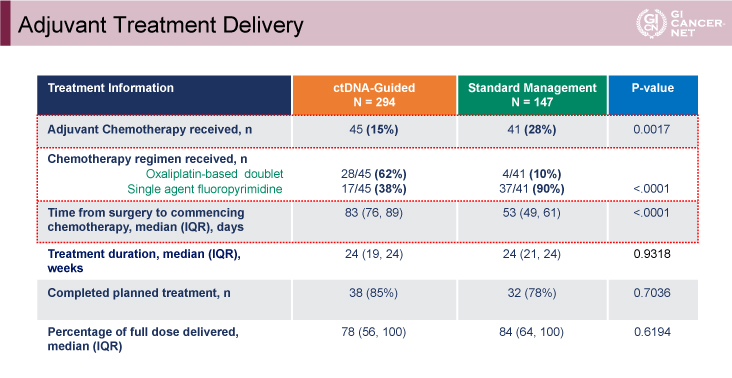
2015年8月から2019年8月までに455例が登録された。適格基準を満たした441例(ctDNA治療群294例、標準治療群147例)が解析対象集団とされた。年齢、性別、ECOG PS、壁深達度(T3:85%)、MMRステータス(MMR deficient:20%)、リンパ節検索個数、臨床病理学的再発高リスク症例(proficient MMRかつT4、①低分化型、②リンパ節検索個数12個未満、脈管侵襲あり、③穿孔・閉塞発症のいずれか1つ以上:40%)など、主な患者背景に両群間で差を認めなかった。結果、補助化学療法実施率は、ctDNA治療群15%、標準治療群で28%であり、ctDNA治療群で有意に低かった(p=0.0017)(表)。また、ctDNA治療群ではOX併用治療が多く選択されていた(62% vs. 10%、p<0.0001)。
表 Adjuvant Treatment Delivery(発表者の許可を得て掲載)
ctDNA治療群と標準治療群のRFSはほぼ同程度であり非劣性が示された
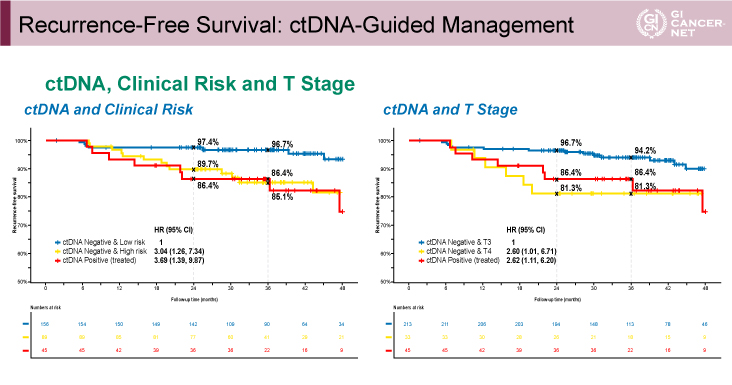
主要評価項目である2年RFS率は、ctDNA治療群93.5%、標準治療群で92.4%であった(HR=0.96、95% CI: 0.51-1.82)。2年RFS率の差の95% CI下限値が-4.1%であり、非劣性マージンとして設定された-8.5%を上回ったため、ctDNA治療群の標準治療群に対する非劣性が示されたと判断された(図1)。サブグループ解析において、壁深達度T3は、標準治療群で再発率が低く(HR=0.73)、T4はctDNA治療群で再発率が低い(HR=1.88)傾向があり、交互作用が認められた(interaction p<0.001)。また、ctDNA治療群においてctDNA陽性集団はctDNA陰性集団と比較して3年RFS率は低い傾向にあった(86.4% vs. 92.5%、HR=1.83、95% CI: 0.79-4.27、p=0.155)。さらにctDNA陰性の中で臨床病理学的再発高リスク集団は、低リスク集団と比較して、3年RFS率が低かった(86.4% vs. 96.7%、HR=3.04、95% CI: 1.26-7.34)(図2)。
図1 Recurrence-Free Survival(発表者の許可を得て掲載)
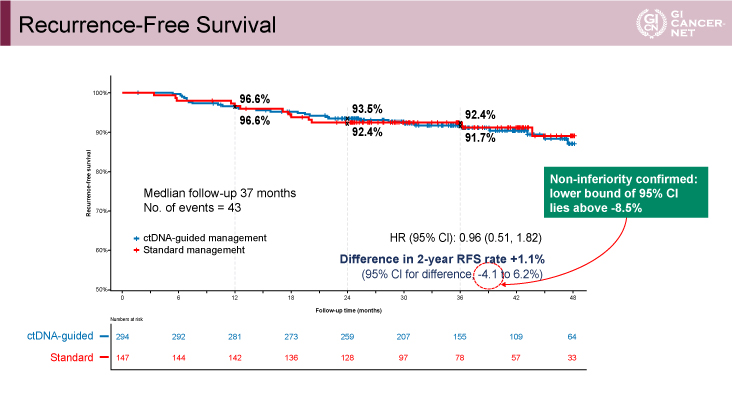
図2 Recurrence-Free Survival: ctDNA-Guided Management(発表者の許可を得て掲載)
結論
Stage II結腸癌におけるctDNA結果に基づく補助化学療法の実施は、従来の臨床病理学的因子に基づく実施と比較して、無再発生存率を損なうことなく、補助化学療法実施率を減少させた。
(レポート:愛知県がんセンター 薬物療法部 中田 晃暢)
References
1) Tie J, et al.: N Engl J Med. June 4, 2022[Online ahead of print]
2) Taniguchi H, et al.: Cancer Sci. 112(7): 2915-2920, 2021[PubMed]
3) Balachandran VP, et al.: J Clin Oncol. 40(suppl 16): abstr 2516, 2022
4) Tie J, et al.: Sci Transl Med. 8(346): 346ra92, 2016[PubMed]
関連サイト
・DYNAMIC試験[ANZCTR]
・VEGA試験[臨床研究実施計画・研究概要公開システム]
・ALTAIR試験[ClinicalTrials.gov]
・GALAXY試験[学会レポート]
谷口 浩也先生
愛知県がんセンター 薬物療法部 医長