Bevacizumabの前治療歴が治療に与える影響:KRAS exon2野生型の切除不能進行・再発大腸癌に対するPanitumumabとCetuximabを比較したASPECCT試験とWJOG6510G試験における患者個別データを用いた統合解析
Influence of treatment with prior bevacizumab: A combined analysis of individual patient data from ASPECCT and WJOG6510G trial which compared panitumumab versus cetuximab in patients with wild-type KRAS exon2 metastatic colorectal cancer.
Hiroya Taniguchi, et al.
監修コメント
抗EGFR抗体薬であるPanitumumab(Pmab)とCetuximab(Cmab)はこれまで抗腫瘍効果に違いはないとされてきたが、ASPECCT試験1,2)およびWJOG6510G試験3,4)のサブグループ解析において、Bevacizumab(Bmab)前治療歴の有無でPmabとCmabの治療効果が異なる可能性が示唆されていた。
今回、患者個人データを用いたASPECCT試験とWJOG6510G試験の統合解析において、Bmab前治療歴がある症例では、ECOG PS(performance status)や転移臓器個数、ベースラインのCEA(carcinoembryonic antigen)値といった予後因子での調整後も、Pmab治療効果はCmabと比較し有意に良好であったことが報告され、PmabのCmabに対する優越性は患者背景の偏りのために生じたものではないことが示唆された。
しかし、なぜBmab前治療歴の有無によってPmabとCmabの治療効果に差が生じるのかといった分子生物学的な機序に関する情報は不足しているのが現状である。発表者らは仮説として、Bmab投与によって腫瘍環境が低酸素となり、epidermal growth factor receptor(EGFR)に対する強い親和性(affinity)を有する血管新生因子[heparin binding-epidermal growth factor-like growth factor(HB-EGF)、betacellulin(BTC)、epidermal growth factor(EGF)など]が増加することが、よりEGFRへの結合親和性が高いPmab治療効果が高くなる原因と考え、基礎的検討を進めている。
本報告は、同じ抗腫瘍効果を有すると考えられる抗EGFR抗体を選択する際に考慮してもよい結果であったと考える。Ramucirumab、Aflibercept、Regorafenibといった他の血管新生阻害薬もBmabと同様の影響を及ぼすのか、抗EGFR抗体をre-challengeとして使用する際にも本結果を外挿できるのか、前述のEGFRに対する強い親和性を有する血管新生因子が抗EGFR抗体薬の効果を予測するバイオマーカーとなり得るかなど、基礎的検討も含め今後の解析に期待したい。
(コメント・監修:静岡県立静岡がんセンター 消化器内科 医長 山﨑 健太郎)
ASPECCT試験とWJOG6510G試験におけるCetuximabに対するPanitumumabの非劣性を検討
ASPECCT試験1,2)とWJOG6510G試験3,4)はいずれも、化学療法に不応となったKRAS exon2野生型の切除不能進行・再発大腸癌患者を対象とし、Cetuximab(Cmab)に対するPanitumumab(Pmab)の非劣性を検討した臨床試験である。両試験のサブグループ解析において、Bevacizumab(Bmab)前治療歴がある症例ではCmabよりもPmabの予後延長効果が高かったことが報告されている。
今回、他の予後因子を加味したより詳細な検討を行うため、患者個別データを用いた2試験の統合解析が行われた。
Bevacizumab(Bmab)前治療歴がある症例を対象に患者個別データを用いて検討
両試験の対象は、Irinotecan(IRI)やOxaliplatin(OX)を含む治療に不応または不耐、かつ抗EGFR抗体薬治療歴のないKRAS exon2野生型の切除不能進行・再発大腸癌患者で、ASPECCT試験ではPmab(499例)またはCmab(500例)が、WJOG6510GではPmab+IRI(61例)またはCmab+IRI(59例)が投与された。
今回の統合解析では、Bmab前治療歴がある症例(ASPECCT試験:Pmab 126例とCmab 132例、WJOG6510G試験:Pmab+IRI 59例とCmab+IRI 57例)を対象に患者個別データを集計し、統計学的検討を行った。
全生存(OS)、無増悪生存(PFS)ともにPanitumumab群が有意に良好
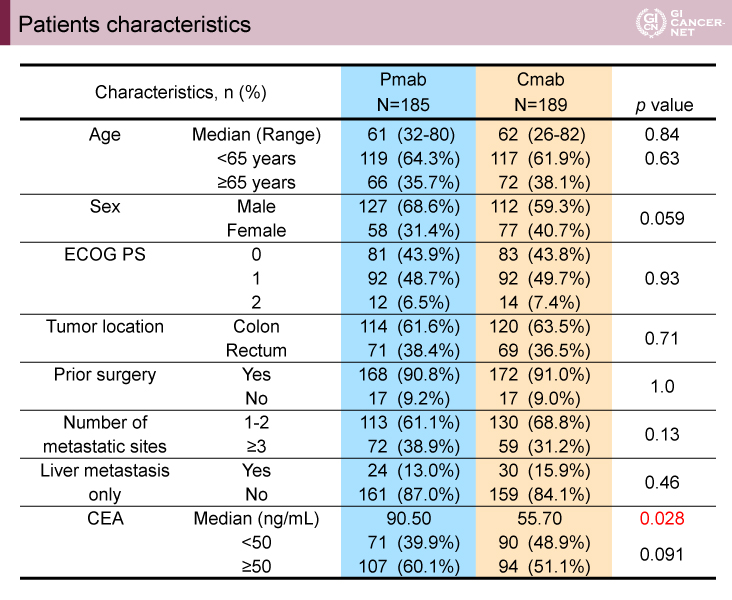
患者背景では、CEA(carcinoembryonic antigen)値がPmab群で有意に高かった(CEA中央値:Pmab群90.50 ng/mL、Cmab群55.70 ng/mL、p=0.028)が、それ以外でPmab群とCmab群における偏りはみられなかった(表1)。
表1 Patients characteristics(発表者の許可を得て掲載)
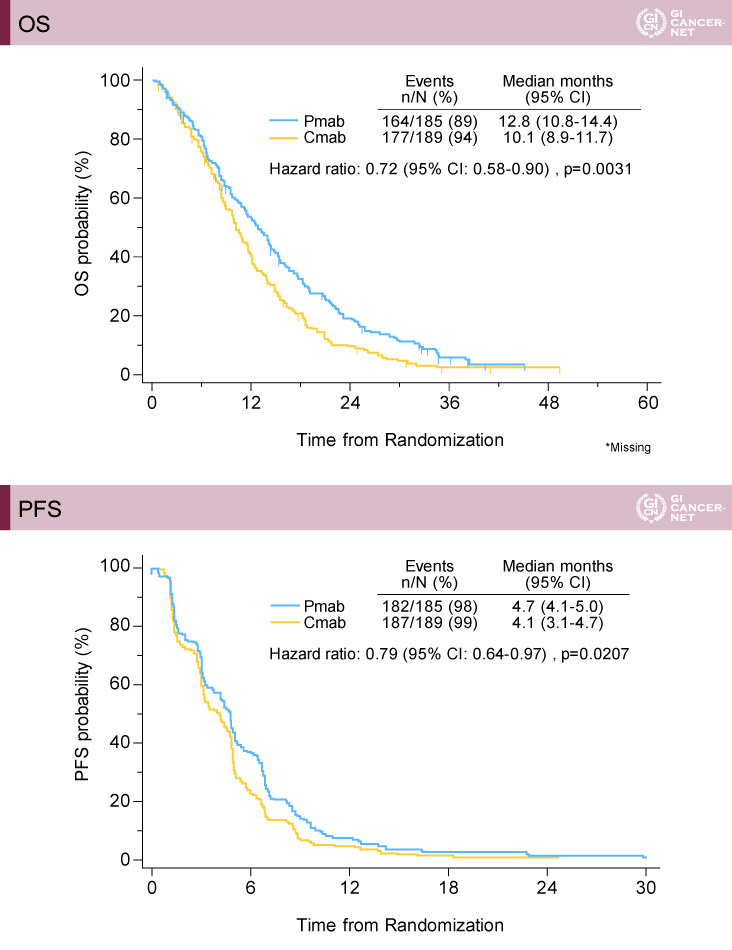
統合解析において、OS中央値[Pmab群12.8ヵ月、Cmab群10.1ヵ月、ハザード比(HR)=0.72、p=0.0031]、PFS中央値(Pmab群4.7ヵ月、Cmab群4.1ヵ月、HR=0.79、p=0.0207)ともにPmab群が有意に良好であった(図1)。
抗EGFR抗体薬に関連する有害事象としては、grade 3以上の低Mg血症がPmab群で有意に多かった(Pmab群12.0%、Cmab群3.7%、p=0.0033)。
図1 OSとPFS(発表者の許可を得て掲載)
年齢(<65/≧65)、性別(男/女)、ECOG PS(performance status)(0,1/2)、原発巣占居部位(結腸/直腸)、手術歴(有/無)、転移臓器個数(1,2/≧3)、肝単独転移(Yes/No)、CEA値(<50/≧50)、試験(ASPECCT/WJOG)、治療レジメン(Cmab/Pmab)を含めた単変量解析では、ECOG PS、転移臓器個数、CEA値、治療レジメンが有意にOSと関連していた。
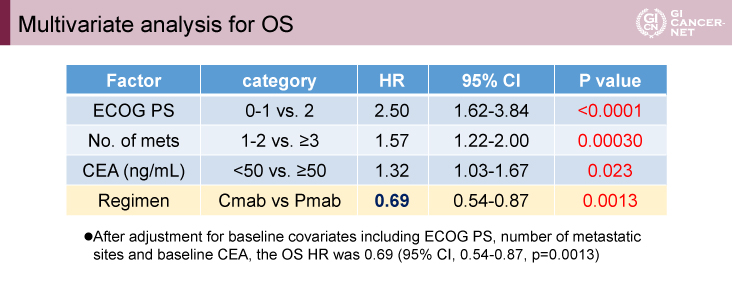
多変量解析では、ECOG PS、転移臓器個数、CEA値、治療レジメンがそれぞれ独立した予後因子であり、治療レジメンによるOSのHRは0.69であった[95%信頼区間(CI):0.54-0.87、p=0.0013](図2)。
図2 OSの多変量解析(発表者の許可を得て掲載)
まとめ
本統合解析では、Bmab前治療歴がある切除不能進行・再発大腸癌患者において、PmabはCmabと比べて有意にOSとPFSを延長した。Pmabの優越性は他の予後因子を含めた多変量解析でも変わらなかった。今後、分子生物学的な作用機序の解明が急がれる。
(レポート:石川県立中央病院 腫瘍内科・消化器内科 医長 木藤 陽介)
References
関連サイト
- ・ASPECCT・WJOG6510G患者個別データの統合解析:GCS 2018 #745[学会レポート]

山﨑 健太郎 先生
静岡県立静岡がんセンター 消化器内科 医長