進行食道癌に対する一次治療におけるPembrolizumab+化学療法vs.化学療法単独:KEYNOTE-590試験(第III相試験)
Pembrolizumab plus Chemotherapy versus Chemotherapy as First-Line Therapy in Patients with Advanced Esophageal Cancer: The Phase 3 KEYNOTE-590 Study
Ken Kato, et al.
監修コメント
食道癌の初回化学療法は、日本食道学会ガイドラインによると、Cisplatinと5-FUの併用療法が弱く推奨されている。これは、第III相試験で明白な優越性が示されておらず、いくつかの第II相試験において、30~40%の奏効割合と8ヵ月前後の生存期間中央値が示されていること、および、同じ扁平上皮癌である頭頸部癌でも有効性が報告されているためである。20年以上にわたり、5-FU+Cisplatinは標準治療とされており、抗EGFR抗体との併用療法の試験でもポジティブな結果は報告されなかった。ATTRACTION-3試験1)によりNivolumabが、KEYNOTE-181試験によりPembrolizumabが、二次治療以降の食道癌に使えるようになり、他の癌種と同様に、初回化学療法に対する免疫チェックポイント阻害剤の上乗せ効果があるかについて検討された。
KEYNOTE-590試験は、扁平上皮癌(ESCC)が70%登録され、先行する試験の結果から効果が期待できる集団であるESCC群、あるいはCPS≧10群についての有効性をみたのちに、全体の有効性をみるデザインとなっていた。結果は、差が出ると予想されていたESCCや、CPS≧10の集団だけでなく、腺癌も含めた全登録者における集団でも、有意な差が認められた。サブグループ解析でも、腺癌患者でのHRはOSで0.74、PFSで0.63と、ESCCとあまり変わらず、その点については意外な結果と言える。胃癌を対象に、化学療法と化学療法+Pembrolizumabを比較したKEYNOTE-062試験2)では、接合部腺癌のサブグループでは、HRは1.0付近であるが、この違いを説明するためにはもう少しデータが必要である。
毒性については特に新たな所見はなく、5-FU+Cisplatin+Pembrolizumabは、標準治療として行うに足る結果であったと思われた。ESCCを対象に、5-FU+Cisplatinと、5-FU+Cisplatin+Nivolumab、そしてNivolumab+Ipilimumabを比較したCheckMate 648試験の解析が近い将来出てくると思われ、初回化学療法から免疫チェックポイント阻害剤を併用する治療が標準治療になっていくことが予想される。二次治療以降では、併用療法などによるリチャレンジなど、単剤の効果を増すような治療開発が行われていくことが予想される。いずれにしても、何十年ぶりに食道癌初回化学療法を変えた、歴史的な結果であった。
(コメント・監修:国立がん研究センター中央病院 頭頸部内科 科長 加藤 健)
進行食道癌に対する治療開発
進行食道癌に対する治療は現在、一次治療でFluoropyrimidine+プラチナ系薬剤併用(FP)療法を使用し、二次治療としてTaxane系、Irinotecan、腺癌の場合にはRamucirumab+Paclitaxelの使用が推奨されている。
Pembrolizumab単独療法はKEYNOTE-180試験において、食道扁平上皮癌(ESCC)かつPD-L1 Combined Positive Score(CPS)≧10の患者で奏効率(ORR)14%かつ奏効持続期間(DOR)中央値は未到達となっていた3,4)。またKEYNOTE-181試験において、ESCCかつPD-L1 CPS≧10の患者で化学療法との比較が行われ、生存期間(OS)中央値が10.3ヵ月vs. 6.7ヵ月(HR=0.64)、ORRが22% vs. 7%、DORが9.3ヵ月vs. 7.7ヵ月となっていた5)。この結果を受け、FDAならびにPMDAは局所進行再発もしくは遠隔転移を有するESCCでかつPD-L1 CPS≧10に対して、二次治療以降でのPembrolizumab単独療法を承認した。
本試験は、腺癌も含めた進行食道癌の一次治療における、Pembrolizumab+化学療法と化学療法単独を比較する、第III相無作為化二重盲検プラセボ対照試験である。
主要評価項目はOSとPFS
本試験のデザインは、進行食道癌に対するPembrolizumab+FP療法(以下、P+C群)の、FP単独療法(以下、C群)に対する優越性を検証する第III相無作為化比較試験であり、二重盲検プラセボ対照で行われた(図1)。
本試験の主な適格基準は、未治療の局所進行切除不能または遠隔転移を有する食道腺癌もしくは食道扁平上皮癌、もしくは進行/遠隔転移を有する食道胃接合部腺癌(Siewert type 1)で、ECOG PS(Eastern Cooperative Oncology Group Performance Status)0-1、RECIST v1.1で測定可能病変を有することであった。
治療スケジュールは、P+C群はPembrolizumab 200 mg+FP療法(5-FU 800 mg/m2 days 1-5+Cisplatin 80 mg/m2)を3週毎に施行した。Cisplatinは6コースまで、そのほかは35コースまで施行した。またC群ではプラセボ+FP療法(5-FU 800 mg/m2 days 1-5+Cisplatin 80 mg/m2)を3週毎に施行した。こちらも同様にCisplatinは6コースまで、そのほかは35コースまで施行した。
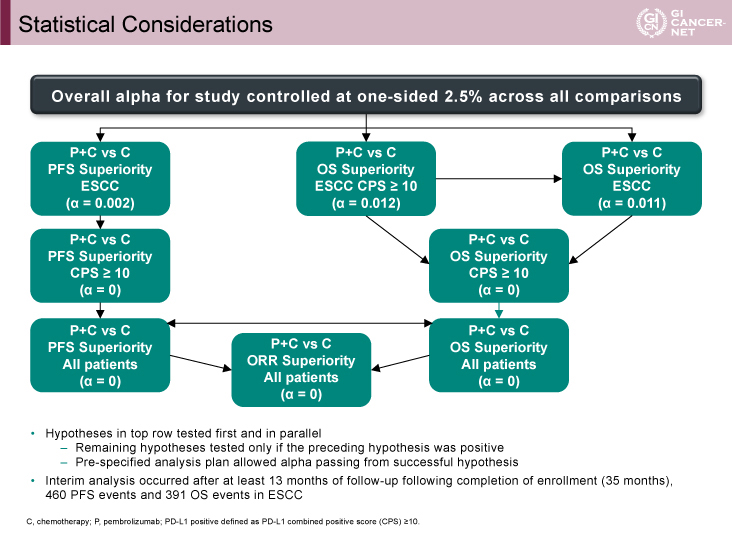
主要評価項目はESCC群、ESCCかつCPS≧10群、CPS≧10群、そして全登録患者でのOSおよびESCC群、CPS≧10群、全登録患者でのPFS(RECIST v1.1研究者評価)であり、主体のα=0.025はアルファパッシングが可能となっていた(図2)。上段の仮説が最初に検定され、並行して検定される。残りの仮説は、先行仮説が証明された場合にのみ検定された。あらかじめ決められた分析計画により、成功した仮説からのアルファパッシングが可能であった。
副次評価項目は、ORRであった。
図1 Study Design(発表者の許可を得て掲載)
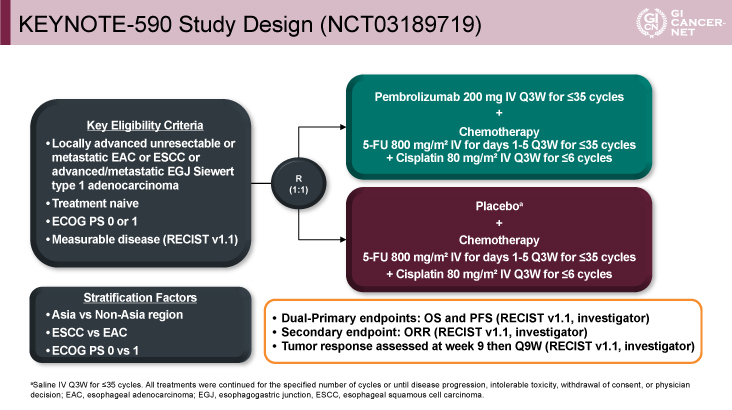
図2 Statistical Considerations(発表者の許可を得て掲載)
Pembrolizumab+FP療法はFP療法群に対してOS/PFSともに統計学的に有意な改善を認めた
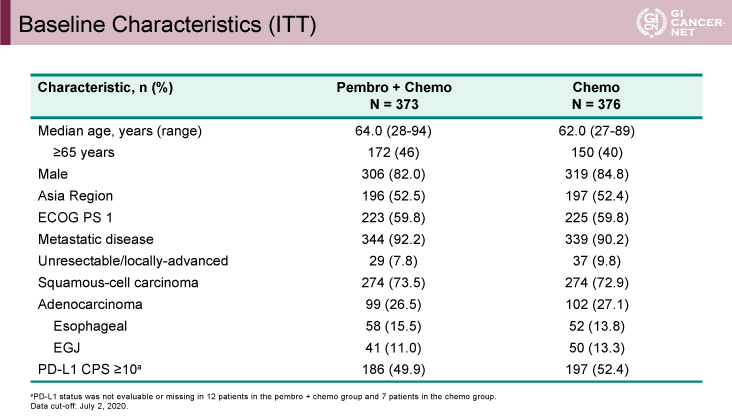
症例登録は2017年7月25日から2019年6月3日まで行われ、P+C群373例、C群376例の計749例が登録された。中間解析は、登録完了後13ヵ月以上の追跡調査後(35ヵ月後)の2020年7月に行われ、中間解析時の追跡期間中央値(無作為化からデータカットオフまたは死亡まで)は10.8ヵ月であった。ESCCで460件のPFSイベント、391件のOSイベントが発生した。患者背景はP+C群(373例)、C群(376例)それぞれで、年齢中央値(範囲)64.0歳(28-94歳)vs. 62.0歳(27-89歳)、ECOG PS 1は59.8% vs. 59.8%、扁平上皮癌は73.5% vs. 72.9%、腺癌は26.5% vs. 27.1%、食道胃接合部腺癌は11.0% vs. 13.3%、PD-L1 CPS≧10は49.9% vs. 52.4%であった(表1)。
表1 Baseline Characteristics(ITT)(発表者の許可を得て掲載)
OSはEvent発生率がESCCかつPD-L1 CPS≧10でP+C群66% vs. C群85%(HR=0.57、95% CI: 0.43-0.75、p<0.0001)(図3)、ESCCでP+C群69% vs. C群81%(HR=0.72、95% CI: 0.60-0.88、p=0.0006)(図3)、PD-L1 CPS≧10でP+C群67% vs. C群84%(HR=0.62、95% CI: 0.49-0.78、p<0.0001)(図4)でそれぞれ統計学的に有意な改善を認めた。全ての対象に対してもEvent発生率がP+C群70% vs. C群82%(HR=0.73、95% CI: 0.62-0.86、p<0.0001)(図4)と統計学的に有意な改善を認めた。
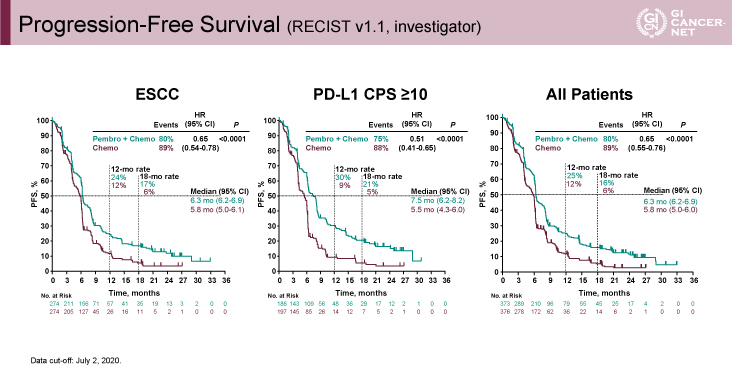
PFS(RECIST v1.1研究者評価)はEvent発生率で、ESCCでP+C群80% vs. C群89%(HR=0.65、95% CI: 0.54-0.78、p<0.0001)(図5)、PD-L1 CPS≧10でP+C群75% vs. C群88%(HR=0.51、95% CI: 0.41-0.65、p<0.0001)(図5)となっており、ともに統計学的に有意な改善を認めた。全ての対象においてもP+C群80% vs. C群89%(HR=0.65、95% CI: 0.55-0.76、p<0.0001)(図5)と統計学的に有意な改善を認めていた。
主要評価項目であるOSとPFSのサブ解析においては、P+C群においてほぼすべての項目で良好な傾向を認めた。腺癌においてもOSでHR=0.74、95% CI: 0.54-1.02、PFSでHR=0.63、95% CI: 0.46-0.87で良好な傾向であった。またPD-L1 CPS<10においてもOSでHR=0.86、95% CI: 0.68-1.10、PFSでHR=0.80、95% CI: 0.64-1.01と概ね良好な傾向であった。
副次評価項目である奏効率はP+C群45.0% vs. C群29.3%(群間差:15.7%、p<0.0001、層別Miettinen and Nurminen法)と統計学的に有意な差を示していた。奏効持続期間(DOR)は中央値(範囲)がP+C群で8.3ヵ月(1.2-31.0)、C群で6.0ヵ月(1.5-25.0)であった。
治療関連有害事象としては、Grade 3以上がP+C群71.9% vs. C群67.6%であり、両群に差はなかった。免疫関連有害事象および輸注反応はP+C群25.7% vs. C群11.6%であり、既報通りであった。治療関連死においてもP+C群2.4% vs. C群1.4%で両群に差はなかった。
図3 Overall Survival(発表者の許可を得て掲載)
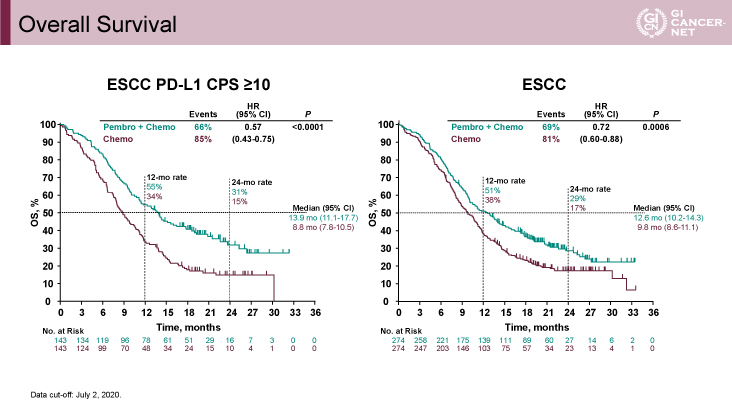
図4 Overall Survival(発表者の許可を得て掲載)
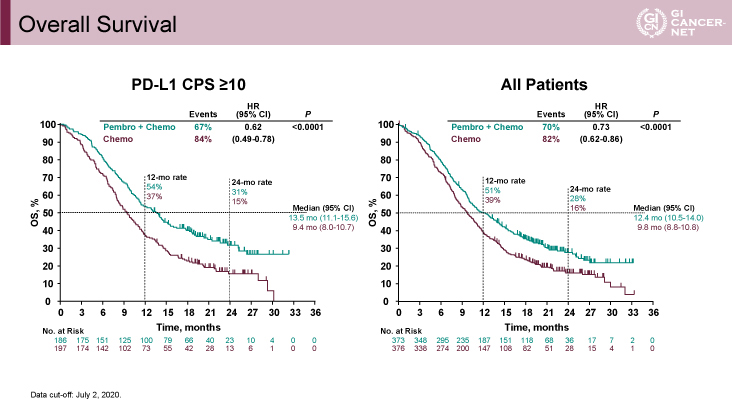
図5 Progression-Free Survival(RECIST v1.1, investigator)(発表者の許可を得て掲載)
まとめ
本試験では、P+C群はP単独群に比べてOSとPFS、ORRともに統計学的に有意な改善を認めていた。OS、PFSともにESCC CPS≧10、ESCCの対象のみならず、全ての対象に対して有意な改善を認めていた。両群間の治療関連有害事象においては既報通りであり、新たな有害事象の報告はなかった。
以上より、食道胃接合部腺癌を含む局所進行・転移を有する食道癌に対しては、Pembrolizumabと化学療法併用療法を第一選択治療に考慮すべきである。
(レポート:国立がん研究センター中央病院 頭頸部内科 廣瀬 俊晴)
References
- 1) Kato K, et al.: Lancet Oncol. 20(11): 1506-1517, 2019 [PubMed]
- 2) Shitara K, et al.: JAMA Oncol. Sep 3, 2020 [Online ahead of print]
- 3) Shah MA, et al.: JAMA Oncol. 5(4): 546-550, 2019 [PubMed]
- 4) Kato K, et al.: J Clin Oncol. 37(15_suppl): 4032-4032, 2019 [JCO]
- 5) Shah MA, et al.: J Clin Oncol. 37(15_suppl): 4010-4010, 2019 [JCO]
関連サイト
- ・ATTRACTION-3試験 [ClinicalTrials.gov][論文紹介]
- ・KEYNOTE-181試験 [ClinicalTrials.gov][学会レポート]
- ・KEYNOTE-590試験 [ClinicalTrials.gov]
- ・KEYNOTE-062試験 [ClinicalTrials.gov][学会レポート]
- ・CheckMate 648試験 [ClinicalTrials.gov]
- ・KEYNOTE-180試験 [ClinicalTrials.gov]

加藤 健 先生
国立がん研究センター中央病院 頭頸部内科 科長