RAS/BRAF野生型の切除不能進行再発大腸癌の一次治療においてmFOLFOXIRI+Panitumumab療法とmFOLFOX6+Panitumumab療法を比較した無作為化第III相試験(TRIPLETE試験)
Modified FOLFOXIRI plus panitumumab (mFOLFOXIRI/PAN) versus mFOLFOX6/PAN as initial treatment of patients with unresectable RAS and BRAF wild-type metastatic colorectal cancer (mCRC): Results of the phase III randomized TRIPLETE study by GONO
Chiara Cremolini, et al.
監修コメント
RAS野生型・左側原発大腸癌に対する一次治療としてdoubletレジメンと抗EGFR抗体薬の併用療法が標準治療のひとつであることが本学会において再確認された(abstract LBA1)。このdoubletレジメンよりさらに強力な治療はあるだろうか? そのひとつの候補となっているのがtripletレジメンと抗EGFR抗体薬の併用療法である。FOLFOXIRI療法とFOLFOXIRI+Panitumumab療法の有効性を検証した無作為化第II相のVOLFI試験では、FOLFOXIRI+Panitumumab療法の奏効率の高さが示され、今後期待されるレジメンとなった1)。本邦ではFOLFOXIRI+CetuximabとFOLFOXIRI+Bevacizumabを比較したDEEPER試験が行われ、抗EGFR抗体薬併用治療のDpRが有意に高いことが示された(ASCO 2021 abstract 3501)。
この度、イタリアのオンコロジーグループGONOにて、FOLFOX+Panitumumab療法とFOLFOXIRI+Panitumumab療法を比較検証する第III相試験が行われ、その結果が報告された。Primary endpointの奏効率はmetせず、さらにDpRも両群で有意差は認めなかった。さらに、PFSの解析でも両群に差は認めず、FOLFOX+Panitumumab療法のbackbone chemotherapyにIrinotecanを加える意義はないと結論づけられている。本試験のディスカッションポイントは、腫瘍縮小判定が施設外の中央判定になっていない設定、これまでのdoublet+抗EGFR抗体薬治療の結果と比較してDpR値が小さいことである。FOLFOXIRI+Panitumumab療法群はdose intensityがFOLFOX群よりも悪いことも示されており、毒性により強度が下がり治療効果がうまく出ていない可能性も示唆される。本邦で行われたDEEPER試験の生存解析結果はこれから発表される予定であり、今回のTRIPLETE試験のOSとDEEPER試験の生存結果に今後注目していきたい。
(聖マリアンナ医科大学 臨床腫瘍学講座 主任教授 砂川 優)
RAS/BRAF野生型大腸癌に対し、抗EGFR抗体薬併用下において殺細胞性抗癌剤を強化(tripletレジメン)する意義はあるか?
RAS/BRAF野生型の切除不能進行再発大腸癌(mCRC)に対して、doubletレジメン(FOLFOX療法またはFOLFIRI療法)と抗EGFR抗体薬の併用療法は標準治療の一つとなっている2)。一方、tripletレジメン(FOLFOXIRI療法)と抗EGFR抗体薬の併用療法は無作為化第II相試験であるVOLFI試験において、RAS野生型のmCRC患者に対してFOLFOXIRI単独療法よりも高い奏効割合(ORR:87% vs. 61%)を示した1)。今回、RAS/BRAF野生型のmCRCの初回治療において、抗EGFR抗体薬(Panitumumab)併用下で、tripletレジメンはdoubletレジメンよりも高い抗腫瘍効果を示すかどうかを検証するため、無作為化第III相試験であるTRIPLETE試験がイタリアのGONOグループによって実施された。
FOLFOXIRIレジメンはmodifiedされた用量で計画された
TRIPLETE試験の対象は、RAS/BRAF野生型のmCRCの初回治療例であり、患者は標準治療群であるmFOLFOX6+Panitumumab群(doublet+Pan群)と試験治療群であるmFOLFOXIRI+Panitumumab群(triplet+Pan群)に1:1で無作為に割り付けられた(図1)。層別化因子として、ECOG PS(0-1 vs. 2)、原発巣部位(右側vs.左側)、転移巣部位(肝限局vs.肝限局以外)が用いられた。FOLFOXIRIレジメンは、抗EGFR抗体薬との併用でgrade 3以上の消化器毒性の頻度が高くなることから、TRIBE試験で用いられた原法よりもIrinotecan(165→150mg/m2)と5-FU(3,200→2,400mg/m2)の用量を減量した投与スケジュールで計画された3,4)。両群とも導入療法として最大12サイクルまで投与し、その後はPDになるまで5-FU/LV+Panitumumab療法で維持された。主要評価項目は、RECIST 1.1によるORRで、triplet+Pan群の優越性を検証するデザインとなっていた。副次評価項目は、early tumor shrinkage、deepness of response、無増悪生存期間(PFS)、R0切除割合、全生存期間(今回未発表)などであった。
図1 TRIPLETE trial(発表者の許可を得て掲載)
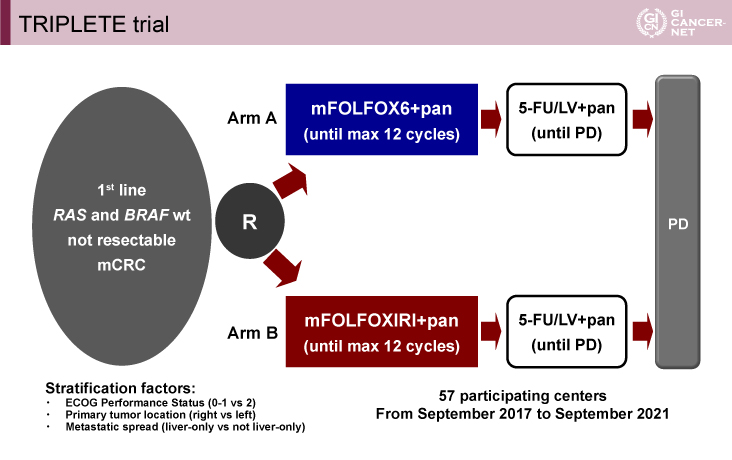
主要評価項目におけるmFOLFOXIRI+Panitumumab療法の優越性は示されず
435例の患者が登録され、217例がdoublet+Pan群に、218例がtriplet+Pan群に割り付けられた。両群の患者背景(doublet+Pan群/triplet+Pan群)は、ECOG PS 0が80%/84%、同時性転移が88%/87%、肝限局転移が37%/39%、左側大腸癌が88%/88%、ミスマッチ修復機能欠損が1%/3%であった。
主要評価項目のORRは、doublet+Pan群が76%に対し、triplet+Pan群が73%であり、triplet+Pan群の優越性が示されなかった(オッズ比[95%信頼区間]=0.87[0.56-1.34]、p=0.526)(表1)。
表1 Response and Resection Rate(発表者の許可を得て掲載)
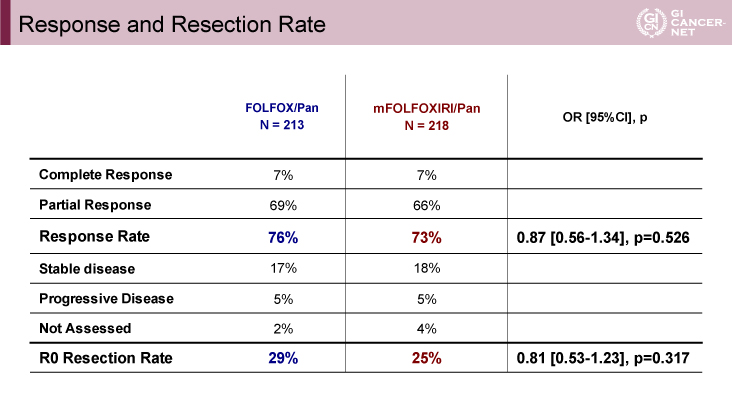
副次評価項目においてもmFOLFOXIRI+Panitumumab療法の優越性は認めず
R0切除割合はdoublet+Pan群で29%、triplet+Pan群で25%であった(オッズ比[95%信頼区間]=0.81[0.53-1.23]、p=0.317)。Deepness of response(中央値:-47% vs. -48%、p=0.845)とearly tumor shrinkage(58% vs. 57%、オッズ比[95%信頼区間]=0.97[0.66-1.42]、p=0.878)も、両群で差を認めなかった(図2)。
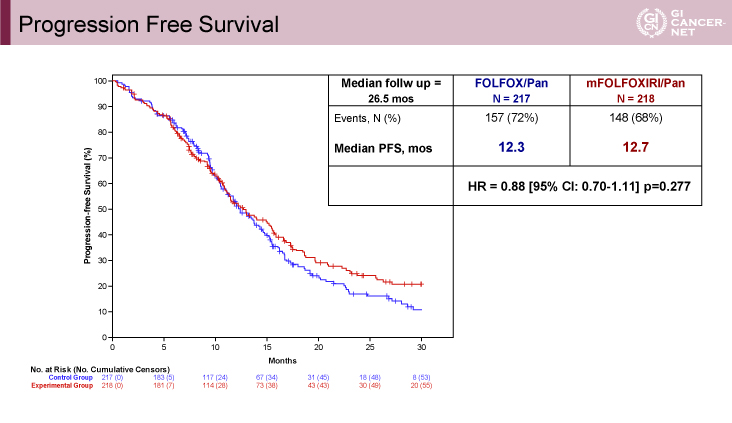
PFS中央値はdoublet+Pan群が12.3ヵ月に対し、triplet+Pan群が12.7ヵ月であり、両群で差を認めなかった(ハザード比[95%信頼区間]=0.88[0.70-1.11]、p=0.277)(図3)。
図2 Deepness of Response and Early Tumor Shrinkage(発表者の許可を得て掲載)
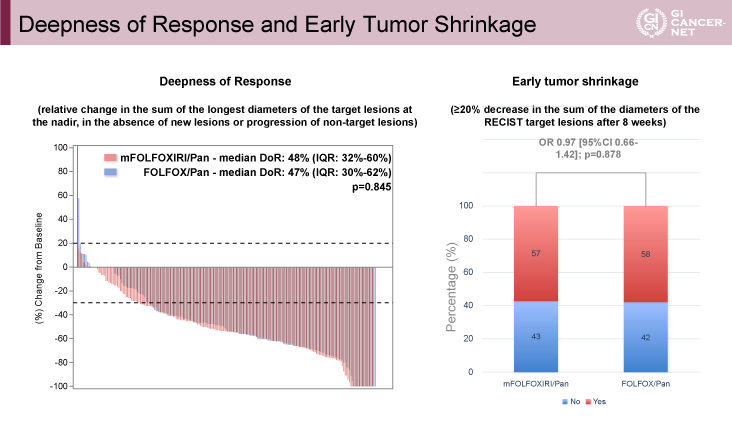
図3 Progression Free Survival(発表者の許可を得て掲載)
サブグループ解析では、ORRにおいて性別および原発巣部位が治療群との有意な交互作用を示したが、doublet+Pan群に対してtriplet+Pan群の効果が有意に高いサブグループは同定されなかった。安全性に関しては、triplet+Pan群のほうがgrade 3/4の下痢の頻度が多かった(23% vs. 7%)。
まとめ
Panitumumab併用下で、mFOLFOXIRI療法はmFOLFOX6療法よりも高い抗腫瘍効果を示すことができなかった。したがって、RAS/BRAF野生型のmCRCの初回治療として、mFOLFOXIRI+Panitumumab療法を推奨すべきではない。
(レポート:聖マリアンナ医科大学 臨床腫瘍学講座 講師 新井 裕之)
References
1) Modest DP, et al.: J Clin Oncol. 37(35): 3401-3411, 2019[PubMed]
2) Yoshino T, et al.: Ann Oncol. 29(1): 44-70, 2018[PubMed]
3) Fornaro L, et al.: Ann Oncol. 24(8): 2062-2067, 2013[PubMed]
4) Cremolini C, et al.: JAMA Oncol. 4(4): 529-536, 2018[PubMed]
関連サイト
・TRIPLETE試験[ClinicalTrials.gov]
・VOLFI試験[ClinicalTrials.gov][学会レポート(ESMO 2018)][学会レポート(ESMO 2017)]
・DEEPER試験[ClinicalTrials.gov][学会レポート]
・TRIBE試験[ClinicalTrials.gov][学会レポート][論文紹介(2018)][論文紹介(2015)]
・MACBETH試験[ClinicalTrials.gov]
砂川 優先生
聖マリアンナ医科大学 臨床腫瘍学講座 主任教授