前治療歴のない切除不能進行・再発胃癌および食道胃接合部癌に対するNivolumab+化学療法併用vs.化学療法を比較した多施設共同無作為化第II/III相試験:ATTRACTION-4試験(ONO-4538-37)
Nivolumab plus Chemotherapy versus Chemotherapy Alone in Patients with Previously Untreated Advanced or Recurrent Gastric/Gastroesophageal Junction (G/GEJ) Cancer: ATTRACTION-4 (ONO-4538-37) Study
Narikazu Boku, et al.
監修コメント
切除不能進行・再発胃癌に対する免疫チェックポイント阻害剤の開発は、“難しい”というのがここ数年の印象であろう。ATTRACTION-2試験では、いわゆるsalvage-lineでのNivolumabがプラセボとの比較で有効性を示し、胃癌もここから免疫チェックポイント阻害剤のポジティブな結果が次々と報告されると期待されていた中で、KEYNOTE-061試験では二次治療においてPembrolizumabがPaclitaxelに対し優越性を示せず、さらにKEYNOTE-062試験では、一次治療においても化学療法との併用において、いずれも想定された優越性を示せず、ネガティブな結果で終わった。バイオマーカーによるエンリッチを行うなどの施策を講じての結果だけに、胃癌に対する免疫チェックポイント阻害剤の開発は、ATTRACTION-4およびCheckMate 649試験の結果がネガティブであれば、もう終了してしまうのではないか、そもそも胃癌にはフィットしない薬剤なのではないか、という危惧があるなかでの今回の発表であった。また、今回は、KEYNOTE-062試験がCisplatin併用化学療法、かつ、アジアからの登録が25%の中で、ATTRACTION-4はOxaliplatin併用療法、かつ、経口摂取可能患者のみ、100%アジアからの患者が登録されているため、結果の違いについても興味がもたれていた。
奏効割合57.5%、PFS 10ヵ月超えという結果は、いままでに経験したことのない数字であり、SOX/CapeOx+Nivolumabという治療法のパワーを示したと考えられる。このHR=0.68という差が、OSでは0.90となってしまったのは残念であったが、両群のOSは17ヵ月を超えており、胃癌の治療もここまで来たかという印象である。胃癌の患者としては比較的状態の良い集団が登録されていることにより、化学療法群の1/4の患者に後治療として免疫チェックポイント阻害剤が入っており、後治療がしっかりと入っていたことなどが影響していると思われたが、バイオマーカーも含め、今後の詳細な解析が望まれている。
すでにPFSの結果にて、胃癌初回化学療法例に対する化学療法+Nivolumabは2020年5月に承認申請が行われ、今回の生存期間のデータも含め現在審査中である。OSの差がネガティブであったことはマイナスであるが、PFSの差が大きいこと、OSの結果が良好なこと、そして、CheckMate 649試験でのOSの延長など、ポジティブな要素もあり、経過を見守りたいと思う。
(コメント・監修:国立がん研究センター中央病院 頭頸部内科 科長 加藤 健)
進行・再発胃癌および食道胃接合部癌に対する一次治療の開発
切除不能進行・再発胃癌および食道胃接合部癌に対して、ATTRACTION-2試験1)においてNivolumabは三次治療以降における有意な生存期間の延長効果を示した。
ATTRACTION-4試験は、HER2陰性の切除不能進行・再発胃癌および食道胃接合部癌を対象に、Nivolumab+化学療法を一次治療として投与する無作為化多施設共同第II/III相試験である。ATTRACTION-4の第II相パート2)では、Nivolumab+化学療法で有望な結果が得られている。
主要評価項目はPFSおよびOSの2項目
本ATTRACTION-4の第III相パートでは、切除不能進行・再発胃癌および食道胃接合部癌に対する一次治療として、Nivolumab+化学療法の化学療法に対する優越性が検証された。
登録患者を、国、ECOG PS、腫瘍細胞のPD-L1発現および病期を割付調整因子として、Nivolumab(360 mg/bodyを3週毎)+化学療法群(SOX療法またはCapeOX療法)とプラセボ+化学療法群に1:1に割り付けた(図1)。
主要評価項目は中央判定の無増悪生存期間(PFS)と全生存期間(OS)の2つが設定された。副次評価項目は、治験責任医師判定のPFS、全奏効割合(ORR)、効果持続期間(DOR)、病勢コントロール割合(DCR)、初回奏効までの期間(TTR)、最良総合効果(BOR)および安全性であった。
本試験は主要評価項目が2つであったために、全体のα=0.05がPFSの検定に0.04、OSの検定に0.01と割り付けられ、PFSの帰無仮説が棄却された場合α=0.04がOSの検定に引き継がれる設定となった(図2)。
図1 Phase 3 part of ATTRACTION-4: Study Design(発表者の許可を得て掲載)
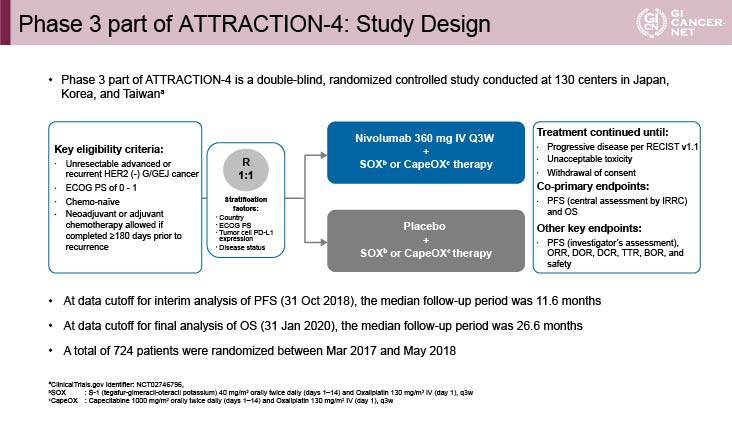
図2 Statistical Considerations(発表者の許可を得て掲載)

Nivolumab+化学療法群は、化学療法群に対して、OSの統計学的な優越性を示さなかったが、PFSの有意な改善を認めた
日本、韓国および台湾の130施設より724例の患者が登録され、Nivolumab+化学療法群362例、化学療法群362例が割り付けられた。患者背景に関しては両群間で差は認められなかった(表1)。
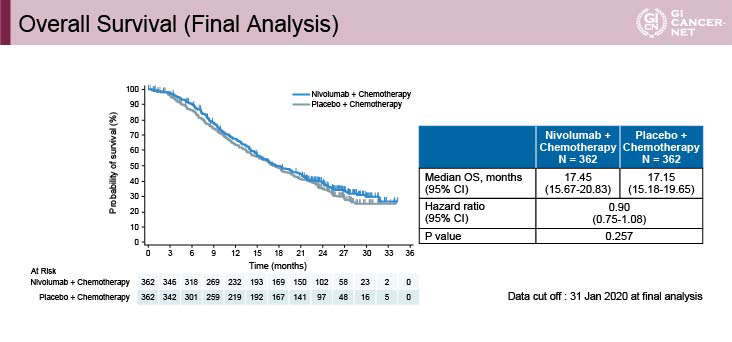
主要評価項目の一つである中央判定のPFSは、Nivolumab+化学療法群10.45ヵ月vs.化学療法群8.34ヵ月(HR=0.68、98.51% CI: 0.51-0.90、p=0.0007)であり、Nivolumab+化学療法群で有意な延長を認めた(図3)。しかしもう一方の主要評価項目であるOS中央値は、17.45ヵ月vs. 17.15ヵ月と有意差は認められなかった(HR=0.90、95% CI: 0.75-1.08、p=0.257)(図4)。
副次評価項目であるBORはComplete Responseが19.3% vs. 13.3%、ORRは57.5% vs. 47.8%(p=0.0088)と、Nivolumab+化学療法群で高い傾向にあった。また、TTRはいずれの群も1.4ヵ月で差がなかったが、DORは12.91ヵ月vs. 8.67ヵ月と、Nivolumab+化学療法群で延長傾向が認められた。
治療関連有害事象の発現は、Nivolumab+化学療法群ではGrade 3-4 69.4%、Grade 5 2.2%、化学療法群ではGrade 3-4 63.1%、Grade 5 1.7%と、Nivolumab上乗せによる有害事象の差は限られていた。
表1 Baseline Characteristics(発表者の許可を得て掲載)
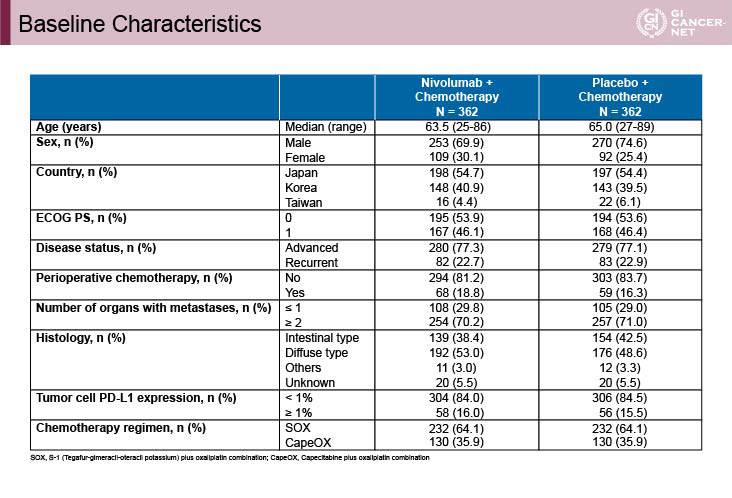
図3 Progression-Free Survival (Interim Analysis)(発表者の許可を得て掲載)
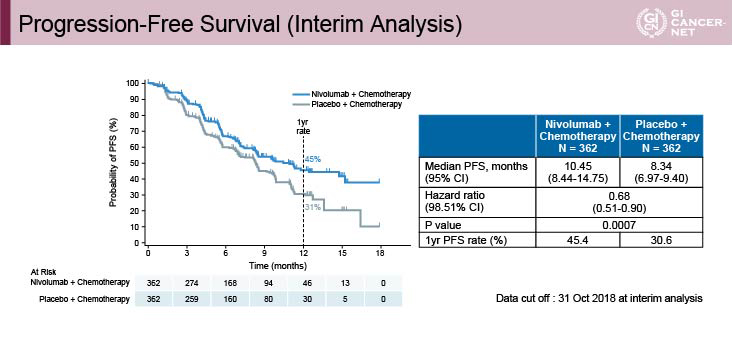
図4 Overall Survival (Final Analysis)(発表者の許可を得て掲載)
まとめ
切除不能進行・再発胃癌および食道胃接合部癌に対する一次治療において、Nivolumab+化学療法はOSの延長を示せなかったものの、PFSの著明な改善が得られ、また忍容性も保たれていた。
Nivolumab+化学療法は、切除不能進行・再発胃癌および食道胃接合部癌に対する新たな一次治療として考慮される。
(レポート:国立がん研究センター中央病院 消化管内科 三國 隼人)
References
- 1) Kang YK, et al.: Lancet. 390(10111): 2461-2471, 2017 [PubMed]
- 2) Boku N, et al.: Ann Oncol. 30(2): 250-258, 2019 [PubMed]
関連サイト
- ・ATTRACTION-2試験 [ClinicalTrials.gov][論文紹介][ケースカンファレンス][学会レポート][レジメン講座]
- ・KEYNOTE-061試験 [ClinicalTrials.gov][論文紹介][学会レポート]
- ・KEYNOTE-062試験 [ClinicalTrials.gov][学会レポート]
- ・ATTRACTION-4試験 [ClinicalTrials.gov]
- ・CheckMate 649試験 [ClinicalTrials.gov]

加藤 健 先生
国立がん研究センター中央病院 頭頸部内科 科長