食道癌
局所進行食道癌に対する術前補助療法としての2つの化学療法レジメンと化学放射線療法レジメンを比較した無作為化対照第III相試験:JCOG1109(NExT)
A randomized controlled phase III trial comparing two chemotherapy regimen and chemoradiotherapy regimen as neoadjuvant treatment for locally advanced esophageal cancer, JCOG1109 NExT study
Ken Kato, et al.
Expert’s view
切除可能な局所進行食道癌は、本邦における食道癌のうち約半数を占める対象であるが、その腫瘍学的特性や解剖学的特性から、治療に難渋する癌種の一つである。この対象に対して、欧米では、食道切除術に術前化学放射線療法を加えることで予後の改善を図った(CROSS試験)。一方、本邦では頸部・胸部・腹部の3領域リンパ節郭清を伴う食道切除術を基軸にして、日本臨床腫瘍研究グループ(JCOG)を中心に、当初は術後Cisplatin+5-FU(CF)療法(JCOG9204試験)、その後は術前CF療法(JCOG9907試験)の開発を行い、予後の改善を図った。しかし、術前CF療法と手術を組み合わせた集学的治療の5年生存割合が55%にとどまっていたことから、さらなる強度の高い周術期治療の開発が望まれていた。
そのような中、本邦で複数の強度を高めた治療開発が行われ、一つは欧米の標準治療である放射線を上乗せした術前CF+放射線(CF-RT)療法であり、第II相試験において、病理学的完全奏効割合(pCR)が42%、治療完遂割合も93.5%と良好な結果が報告された。もう一つは頭頸部癌で開発されていた、Docetaxelを上乗せしたDocetaxel+CF(DCF)療法であった。こちらも安全性試験でpCRが17%、治療完遂割合も90.5%と良好な結果が報告され、懸念された発熱性好中球減少症は予防的抗生剤内服の効果から2.4%にとどまった。このように、有望な周術期治療が2つ開発されていたことから、3群の大規模な第III相試験である、JCOG1109試験(NExT)が実施され、本学会でその結果が報告された。
本試験には601例の切除可能な食道扁平上皮癌が登録され、患者背景はPSや臨床病期など、3群間でwell-balancedであった。主要評価項目である全生存期間(OS)に関しては、DCF療法がCF療法に対する優越性を証明した一方、CF-RT療法はCF療法に対する優越性を証明できなかった。pCRに関しては、CF療法で2.2%、DCF療法で18.6%、CF-RT療法で36.7%と、前段階の第II相試験と同様の結果が得られたが、長期成績と比例しない結果となった。以前に欧州で行われた術前化学療法と術前化学放射線療法を比較したNeoRes試験において、pCRに関しては術前化学放射線療法がより良好な結果であったが、OSに関しては差を認めなかったと報告されており、今回第III相試験で再現性のある結果が示されたと考える。特に注目すべきは7~8年経過した時点でCF-RT群ではOSイベントが発生しており、同群のみ死亡例の約30%が他病死となっていることも鑑みると、放射線の晩期障害の可能性も否定し得ず、さらなる詳細な検討が求められる。
術前治療中の有害事象に関しては、事前に想定されたようにDCF療法群ではgrade 3以上の好中球減少が85.2%、発熱性好中球減少症が16.3%と血球減少がCF群やCF-RT群と比較して多い傾向にあった。以前は胃癌のV325試験のように、DCF療法の有効性は証明できても有害事象のために標準治療となり得なかったこともあった。しかし現在では支持療法の開発も進められており、予防的抗生剤の内服や、G-CSF製剤の予防的投与、J-FORCE試験に基づくOlanzapineを上乗せした4剤併用の制吐療法など、支持療法のデータも蓄積されている。これらの支持療法に加えて、適切な減量や休薬を行うことで、術前DCF療法は効果を減弱することなく、実臨床においても十分運用可能と考える。
NExT試験において、3年生存割合72%と非常に良好な治療効果を示したDCF療法であるが、強度の高い3剤併用療法を行っても治療効果が得られず、早期再発や治療中の増悪を来す症例が存在することは事実である。そのため、同対象においてさらなる治療開発が求められており、CheckMate-577試験のように術後Nivolumabの上乗せも開発の選択肢と考える。しかし、この試験は術前化学放射線療法例のみの結果であり、新しい標準治療であるDCF療法後の術後Nivolumab療法のみで、上記のような予後不良な対象の予後改善につながるかは不明である。そのような中、術前DCF療法にNivolumabを上乗せした治療を検討したJCOG1804E試験(FRONTiER)の短期的な結果も本学会で報告され、pCRが33%と非常に有望な結果が報告されている。また、本邦では術前5-FU+Leucovorin+Oxaliplatin+Docetaxel(FLOT)療法や術後S-1療法の開発も進められ、NExT試験の“NEXT”は既に始まっており、今後も動向に目が離せない領域である。
最後に、約10年の長期間にわたる研究者主導の臨床試験を高い質を維持しながら実施し、術前CF療法から術前DCF療法へと、“practice change”をなし得た研究者の方々に敬意を表したい。
(コメント・監修:国立がん研究センター中央病院 頭頸部・食道内科 医員 山本 駿)
切除可能な局所進行食道扁平上皮癌に対する新たな術前治療の開発
本邦では切除可能局所進行食道癌においては、JCOG9907試験1)の結果から、術前のCisplatin+5-FU(CF)による化学療法が標準治療となっている。一方欧米においてはCROSS試験2)やCALBG-9781試験3)などの結果から、術前の化学放射線療法が標準治療となっている。2つの術前治療に関しては、本邦と海外のリンパ節廓清の範囲や組織型の相違から、純粋な比較は難しくなっている。またCF療法にDocetaxelを加えた、DCF療法が他癌種や単群II相試験で導入化学療法や術前化学療法として有望な可能性を示した4,5)。JCOG1109試験は、切除可能な局所進行扁平上皮食道癌における、術前CF療法に対する術前DCF療法と術前CF+RT療法の優越性を検証した、国内無作為化比較第III相試験であり、本報告はその初回報告である。
術前CF療法に対する、術前DCF療法と術前CF+RT療法の優越性を検証
本試験の主な適格基準は、①切除可能な扁平上皮食道癌、②Eastern Cooperative Oncology Group Performance Status(ECOG PS)が0-1、③cStage IB、II、III(nonT4)(UICC-TNM7th)、④年齢が20~75歳であった(図1)。試験治療群はDCF療法[Docetaxel:70mg/m2(day 1)、Cisplatin:70mg/m2(day 1)と5-FU:750mg/m2(day 1-5)を3週おきに3回投与]とCF+RT療法[Cisplatin:75mg/m2(day 1)と5-FU:1,000mg/m2(day 1-4)を4週おきに2回投与し、1.8Gy×23fr(41.4Gy)の放射線治療を併用する]で、対照群はCF療法[Cisplatin:80mg/m2(day 1)と5-FU:800mg/m2(day 1-5)を3週おきに2回投与]であった。標準治療である術前CF療法の3年生存割合が63%と仮定し、術前DCF療法もしくは術前CF+RT療法の3年生存割合が73%と推定すると、有意水準片側5%、検出力70%で必要症例数は3群合わせて483例となった。途中症例登録ペースが予想を超えたため検出力を80%とし、各群200例が予定症例数となった。601例が各群へ1:1:1[199例(CF群)、202例(DCF群)、200例(CF+RT群)]で無作為に割り付けられ、調整因子は施設とT因子(cT1-2 vs. T3)であった。主要評価項目は全生存期間(OS)、副次評価項目は無増悪生存期間(PFS)、根治切除割合、術前療法における奏効割合(RR)、病理学的完全奏効割合(pCR)、術前治療中の有害事象、周術期合併症、晩期毒性、重篤な有害事象(SAE)であった。
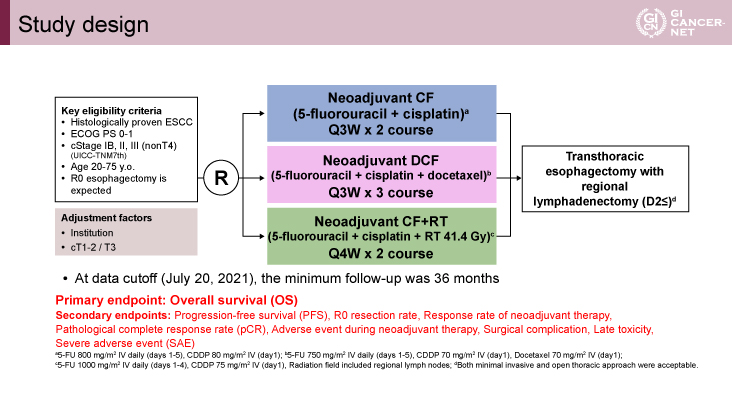
発表者の許可を得て掲載(approved by Ken Kato)
OSにおいて、術前CF療法に対する術前DCF療法の優越性が示された
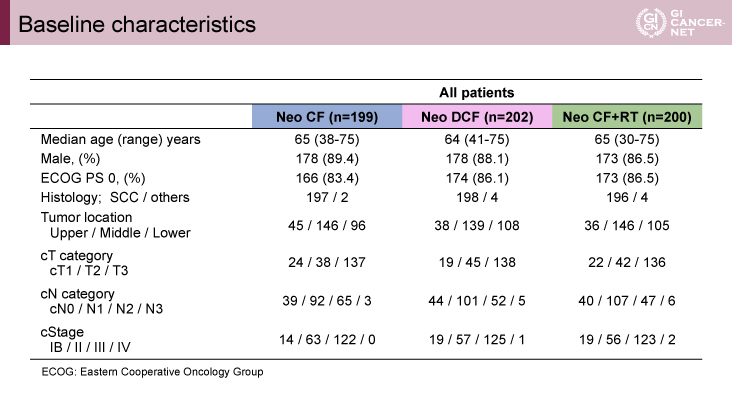
患者背景は3群間で差は認めず、年齢の中央値は約65歳、80%以上がECOG PS 0であった。またcNやcStageに関しても明らかな差はみられなかった(表1)。
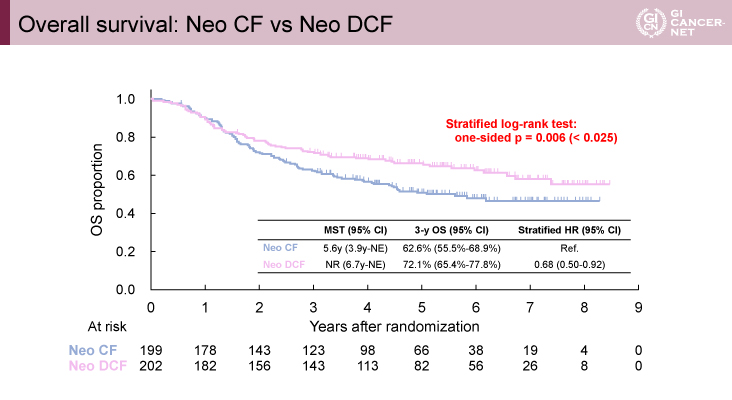
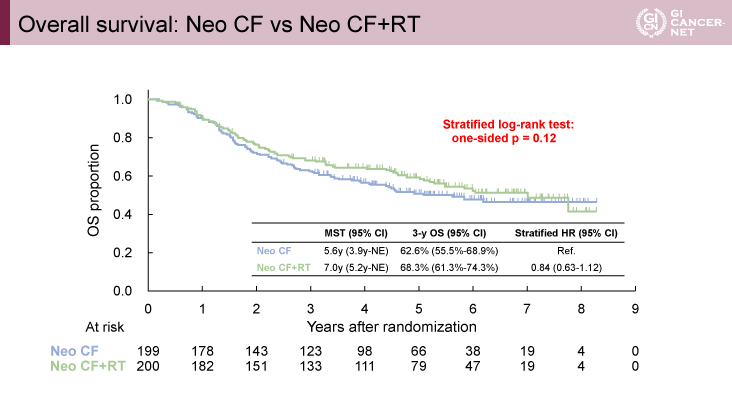
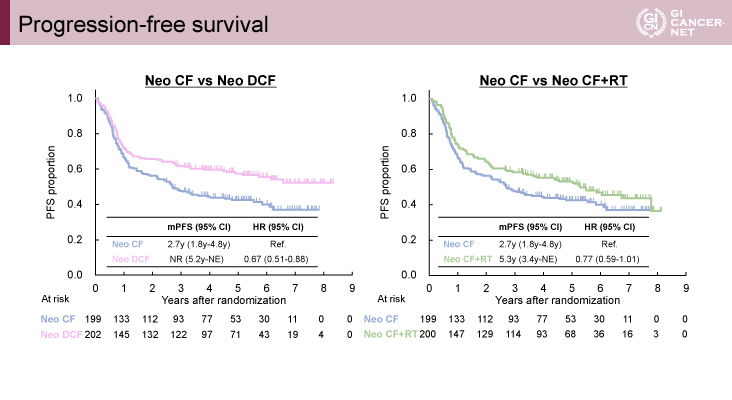
主要評価項目であるOSの中央値は、DCF群とCF群の比較では、DCF群で未到達、CF群で5.6年とDCF群で有意に良好であった[ハザード比(HR)=0.68(95% CI: 0.50-0.92)、p=0.006](図2)。またCF+RT群とCF群の比較では、CF+RT群が7.0年、CF群が5.6年と有意差は認めなかった[HR=0.82(95% CI: 0.61-1.10、p=0.092)](図3)。副次評価項目であるPFSに関しては、DCF群とCF群の比較では、DCF群で未到達、CF群で2.7年とDCF群で有意に良好であった[HR=0.68(95% CI: 0.51-0.90)、p=0.006](図4)。またCF+RT群とCF群の比較では、CF+RT群が5.5年、CF群が2.7年と有意差は認めなかった[HR=0.76(95% CI: 0.58-1.00、p=0.050)](図4)。また3年OSに関しては、CF群が62.6%、DCF群が72.1%、CF+RT群が68.3%となった。
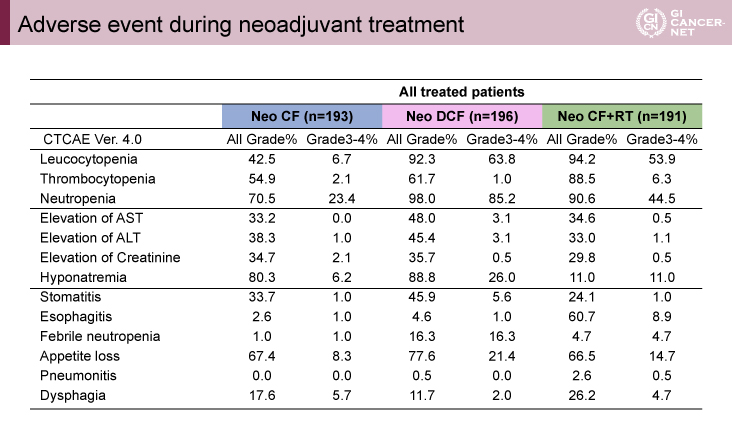
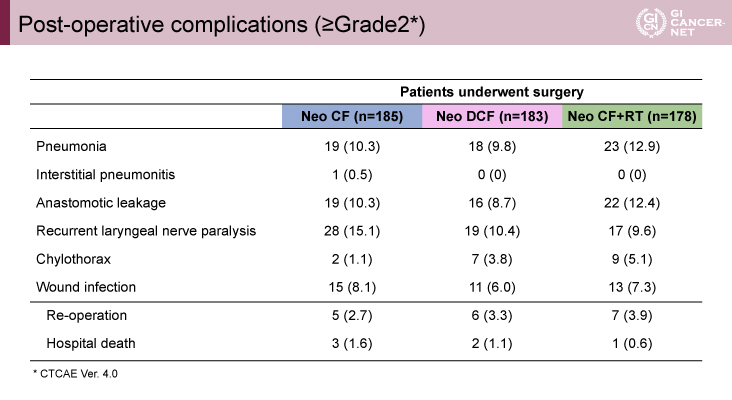
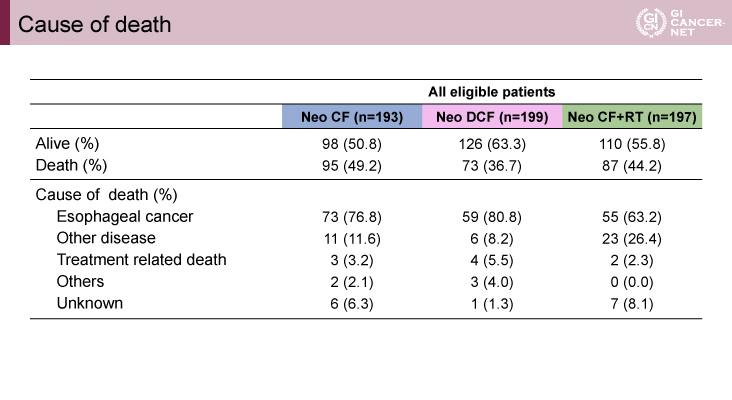
術前治療に関連した有害事象は、G3以上の好中球減少がCF群/DCF群/CF+RT群で23.4%/85.2%/44.5%、G3以上の発熱性好中球減少症はCF群/DCF群/CF+RT群で1.0%/16.3%/4.7%と、DCF群でやや多い傾向にあった(表2)。また術後合併症に関しては、肺炎がCF群/DCF群/CF+RT群で10.3%/9.8%/12.9%、吻合部リークがCF群/DCF群/CF+RT群で10.3%/8.7%/12.4%、反回神経麻痺がCF群/DCF群/CF+RT群で15.1%/10.4%/9.6%と、いずれも大きな違いはみられなかった(表3)。死因に関しては、治療関連死はCF群/DCF群/CF+RT群で3.2%/5.5%/2.3%といずれも大きな違いはみられなかったが、他病死がCF群/DCF群/CF+RT群で11.6%/8.2%/26.4%とCF+RT群でやや多くみられた(表4)。
発表者の許可を得て掲載(approved by Ken Kato)
発表者の許可を得て掲載(approved by Ken Kato)
発表者の許可を得て掲載(approved by Ken Kato)
発表者の許可を得て掲載(approved by Ken Kato)
発表者の許可を得て掲載(approved by Ken Kato)
発表者の許可を得て掲載(approved by Ken Kato)
発表者の許可を得て掲載(approved by Ken Kato)
まとめ
切除可能な局所進行食道扁平上皮癌に対して、術前CF療法に対する術前DCF療法のOSの延長が示された。一方で術前CF療法に対する術前CF+RT療法のOSの延長は示せなかった。また毒性に関しても対応可能な毒性であり、術前のDCF療法が切除可能な食道扁平上皮癌に対する、新たな標準治療と考えられた。
(レポート:国立がん研究センター中央病院 頭頸部・食道内科 池田 剛)
References
- 1) Ando N, et al.: Ann Surg Oncol. 19(1): 68-74, 2012 [PubMed]
- 2) van Hagen P, et al.: N Engl J Med. 366(22): 2074-2084, 2012 [PubMed]
- 3) Tepper J, et al.: J Clin Oncol. 26(7): 1086-1092, 2008 [PubMed]
- 4) Vermorken JB, et al.: N Engl J Med. 357(17): 1695-1704, 2007 [PubMed]
- 5) Hara H, et al.: Cancer Sci. 104(11): 1455-1460, 2013 [PubMed]
関連サイト
- ・CROSS試験 [論文紹介]
- ・JCOG9204試験 [PubMed]
- ・JCOG9907試験 [学会レポート]
- ・NeoRes試験 [ClinicalTrials.gov]
- ・V325試験 [論文紹介]
- ・J-FORCE試験 [学会レポート]
- ・CheckMate-577試験 [学会レポート] [PubMed]
- ・JCOG1804E(FRONTiER)試験 [ClinicalTrials.gov] [PubMed]









山本 駿先生
国立がん研究センター中央病院 頭頸部・食道内科 医員