2018年1月18日~20日に米国サンフランシスコにて開催された2018年 消化器癌シンポジウム(2018 Gastrointestinal Cancers Symposium)より、大腸癌や胃癌、肝細胞癌などの注目演題のレポートをお届けします。演題レポートの冒頭には“Expert's view”として、臨床研究の第一線で活躍する監修ドクターのコメントを掲載しています。
胆道癌
進行胆道癌を対象としたGemcitabine+Cisplatin併用療法(GC療法)とGemcitabine+S-1併用療法(GS療法)の第III相比較試験(JCOG1113)
Randomized phase III study of gemcitabine plus S-1 combination therapy versus gemcitabine plus cisplatin combination therapy in advanced biliary tract cancer (JCOG1113)
Chigusa Morizane, et al.
Expert’s view

上野 誠先生
神奈川県立がんセンター 消化器内科 医長
胆道癌は地理的局在により欧米で患者数が少なく、開発がなかなか進行していない難治性癌の一つである。2010年英国よりGemcitabine+Cisplatin(GC)療法が進行胆道癌の標準治療として確立したのち、新たな標準治療は登場しなかった。その間、欧米では、GC療法に上皮成長因子(EGFR)阻害剤や血管内皮増殖因子(VEGF)を併用する開発が行われ、本邦においては、薬事承認されているS-1を用いた開発が行われてきた。今回、本邦から、S-1関連の開発の一翼である、JCOG肝胆膵グループのGemcitabine+S-1(GS)療法のGC療法に対する非劣性を検証する第III相試験(JCOG1113)が、国立がん研究センター中央病院・森実千種先生より報告された。本試験では、GS療法の非劣性が検証され、さらにgrade 2以上の事前に設定した消化器毒性もGS療法がやや軽度であった。今後、両群の治療成績が大きくは離れていないことから、進行胆道癌の標準治療としてGC療法がGS療法に完全に置き換わることはないと思われるが、二つの治療選択枝が確立したことは、非常に大きな意義があったと考えられる。GS療法は、大量補液を必要としないことから、心機能低下例や外来治療室での長時間点滴が難しい施設など、さまざまな状況で恩恵となり得る。
(コメント・監修:神奈川県立がんセンター 消化器内科 医長 上野 誠)
進行胆道癌に対するGC療法とGS療法
進行胆道癌に対する標準治療はGemcitabine+Cisplatin療法(GC療法)である。JCOG0805において進行胆道癌に対するGemcitabine+S-1療法(GS療法)はS-1単独療法に比べて生存期間が良好な傾向を示し1)、GCと同等程度の治療効果があることが期待された。有害事象プロファイルはGS療法のほうが良好な可能性があり、また、GC療法で必要となる約4時間の補液はGS療法においては不要である。これらを背景として進行胆道癌に対するGC療法に対するGS療法の非劣性を検証する試験を計画した。
GC療法に対するGS療法の非劣性を検証する第III相試験
切除不能もしくは再発胆道癌(肝内胆管癌、肝外胆管癌、胆?癌、乳頭部癌)を有する化学療法未施行の患者を対象とした。患者は無作為化されGC療法(GEM 1,000mg/m2 d1,8+CDDP 25mg/m2 d1,8、3週毎)もしくはGS療法(GEM 1,000mg/m2 d1,8+S-1 60, 80, 100mg/body d1-14、3週毎)に割り付けられた。CDDPの投与回数は最大で16回(400mg/m2)とした。
主要評価項目は全生存期間(OS)であり有意水準は片側5%、検出力80%、ハザード比(HR)の非劣性マージンは1.155と設定した。有害事象の比較に関しては、臨床的に重要なgrade 2以上の有害事象(倦怠感、食欲不振、悪心・嘔吐、口内炎、下痢)を事前に定義した。
GC療法に対するGS療法の非劣性が示された
日本国内の33施設から354人の患者が登録されGC療法群に175人、GS療法群に179人が割り付けられた。有効性の解析は登録された全患者を対象とした(ITT解析)。
患者背景はGC療法/GS療法でそれぞれ、年齢中央値:67歳/67歳、PS 0:74%/69%、胆?癌:39%/39%、切除歴あり:21%/22%、遠隔転移:61%/60%であった。
主要評価項目であるOSの中央値はGC療法群で13.4ヵ月、GS療法群で15.1ヵ月であった(図1)。
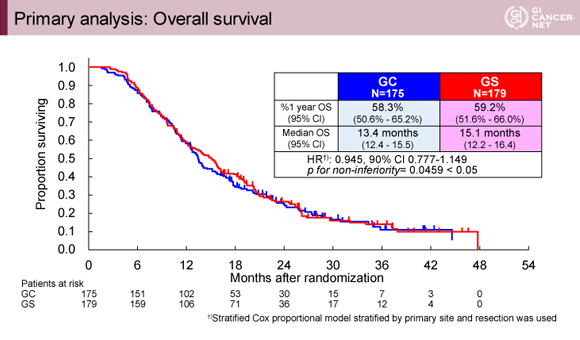
発表者の許可を得て掲載(approved by Chigusa Morizane)
OSのHRは0.945[90%信頼区間(CI):0.777-1.149]であり信頼区間の上限が事前に定めた1.155を下回りGCに対するGS療法の非劣性が示された(非劣性に関するp値0.0459)。サブグループ解析では局所進行例においてGS療法群のOSが良好な傾向があった。
無増悪生存期間(PFS)の中央値はGC療法群で5.8ヵ月、GS療法群で6.8ヵ月であり(図2)、HRは0.864(95% CI: 0.697-1.070)とGS療法群で良好な傾向にあった。
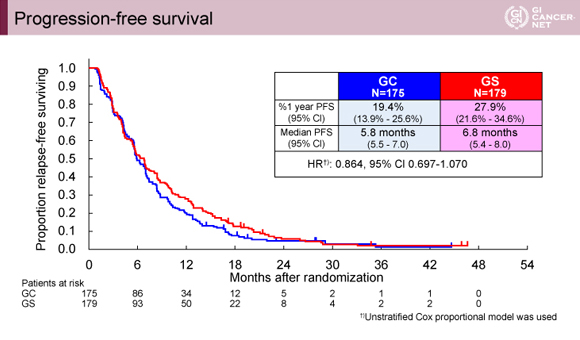
発表者の許可を得て掲載(approved by Chigusa Morizane)
奏効割合はGC療法群で32.4%、GS療法群で29.8%であった。二次化学療法を受けた患者の割合はGC療法群で84%、GS療法群で81%であり、GC療法群の44%が二次化学療法でS-1療法を受け、GS療法群の56%が二次化学療法でGC療法を受けていた。
有害事象に関してはGC療法群/GS療法群においてそれぞれ、grade 3以上の貧血が24%/6.2%、血小板減少が16.4%/7.3%、全gradeの倦怠感が50.9%/44.1%、悪心が36.8%/31.6%、口内炎が12.9%/28.8%、下痢が13.5%/20.9%、皮疹が9.4%/23.7%、であった。事前に設定した臨床的に重要なgrade 2以上の有害事象(倦怠感、食欲不振、悪心・嘔吐、口内炎、下痢)の出現割合はGC療法群で35.1%、GS療法群で29.9%でありGS療法群において少ない傾向があった。治療関連死はGC療法群で3例(1.8%)、GS療法群で0例(0%)であった。
まとめ
進行胆道癌においてGC療法に対するGS療法のOSに関する非劣性が示された。GS療法は進行胆道癌に対する一次化学療法の新たなオプションと考えられる。
(レポート:国立がん研究センター東病院 肝胆膵内科 医員 高橋 秀明)
Reference
- 1) Morizane C, et al.: Cancer Sci. 104(9): 1211-1216, 2013[PubMed]

監修・レポーター
監修
谷口 浩也先生
愛知県がんセンター中央病院 薬物療法部 医長
レポーター
賀川 義規先生
関西ろうさい病院 下部消化器外科 副部長
#745
監修
山﨑 健太郎先生
静岡県立静岡がんセンター 消化器内科 医長
レポーター
山本 祥之先生
筑波大学附属病院 消化器内科 病院講師
#557
監修
上野 誠先生
神奈川県立がんセンター 消化器内科 医長
レポーター
高橋 秀明先生
国立がん研究センター東病院 肝胆膵内科 医員
#207