大腸癌
FOxTROT試験:RAS/BRAF野生型局所進行結腸癌(LACC)における術前Panitumumabの有効性に対するERBB2(HER2)とERBB3(HER3)の予測効果
FOxTROT: predictive effects of ERBB2 (HER2) and ERBB3 (HER3) on neoadjuvant panitumumab benefit in RAS/BRAF wild-type locally advanced colon cancer (LACC)
Jordan Wesley Appleyard, et al.
Expert’s view
抗EGFR抗体薬はRAS/BRAF野生型大腸癌においてその有用性が確立されているものの、さらなる治療効果予測バイオマーカーが求められている。一方、局所進行大腸癌においては、術後補助療法としての抗EGFR抗体薬の有効性は示されておらず1)、また切除可能肝転移に対する術前治療においては、抗EGFR抗体薬の併用がむしろ予後を悪化させる可能性も報告されている2)。大腸癌の進行度によって抗EGFR抗体薬の意義が異なる理由は明らかになっていないが、再発をきたす癌細胞はEGFR依存性が低く上皮間葉転換(EMT)が強いなど生物学的特性が異なるクローンである可能性などが想定されている。
そうした中、本試験でHER3やAREG/EREGなどのバイオマーカーによって対象集団を限れば、周術期における抗EGFR抗体薬の有効性が期待できる集団を選別できる可能性が示唆された点は興味深い。また、既報のPICCOLO試験と同様に、HER3高発現およびAREG/EREG高発現というpositive biomarkerが再現された点も意義深い。進行度によらず抗EGFR抗体薬のバイオマーカーは同様であるのかもしれない。
一方、本発表では従来の再発リスクや患者背景に関する群間差が十分に示されておらず、症例数も限られた探索的な解析にとどまっている点は、本研究の大きな限界である。大腸癌における個別化医療は、切除不能例から切除可能例の周術期治療へとその適用範囲を着実に拡大しつつある。今後の治療開発の過程において、本発表の意義が改めて認識される機会が訪れるとすれば、それは大腸癌治療の進展を示す一つの証左ともいえるであろう。
(コメント・監修:愛知県がんセンター 薬物療法部 医長 谷口 浩也)
背景
FOxTROT試験はT3-4、N0-2、M0の局所進行結腸癌(locally advanced colon cancer: LACC)を対象とした術前治療(neoadjuvant chemotherapy: NAC)の意義を検証した第III相試験である。主解析では、RAS野生型患者に対するPanitumumabの有用性は示されなかった3)。HER2は大腸癌患者の予後不良因子とされ、mCRC一次治療では抗EGFR抗体の効果予測因子とはならないことが報告されている4)。
一方、HER3やEGFRリガンドAREG/EREGについては、mCRC二次治療でHER3やAREG/EREG mRNA高発現の患者でPanitumumabの上乗せ効果が高いことが示されていた5)。今回Post hoc解析としてERBB2(HER2)とERBB3(HER3)に着目したバイオマーカー解析結果を報告する。
方法
FOxTROT試験は、6週NAC~手術~18週の術後治療(adjuvant chemotherapy: AC)を行う試験治療群と、手術~24週ACを行う標準治療群に2:1で割り付けられた。NACに割り付けられた患者でKRAS codon 12、13、61が野生型の場合は、Panitumumab併用群と非併用群へ1:1にランダムに割り付けられ、NACにPanitumumabを追加する意義を検討する第II相試験に組み込まれた。Extended RAS(KRAS codon 12、13、59、61、117、146およびNRAS codon 12、13、59、61)およびBRAF codon 600の遺伝子解析とRNA-seqが行われた。RAS/BRAF野生型に絞った集団において、ERBB2(HER2)とERBB3(HER3)の遺伝子発現と、無病生存期間(disease free survival: DFS)および全生存期間(overall survival: OS)の相関が検討された(図1)。
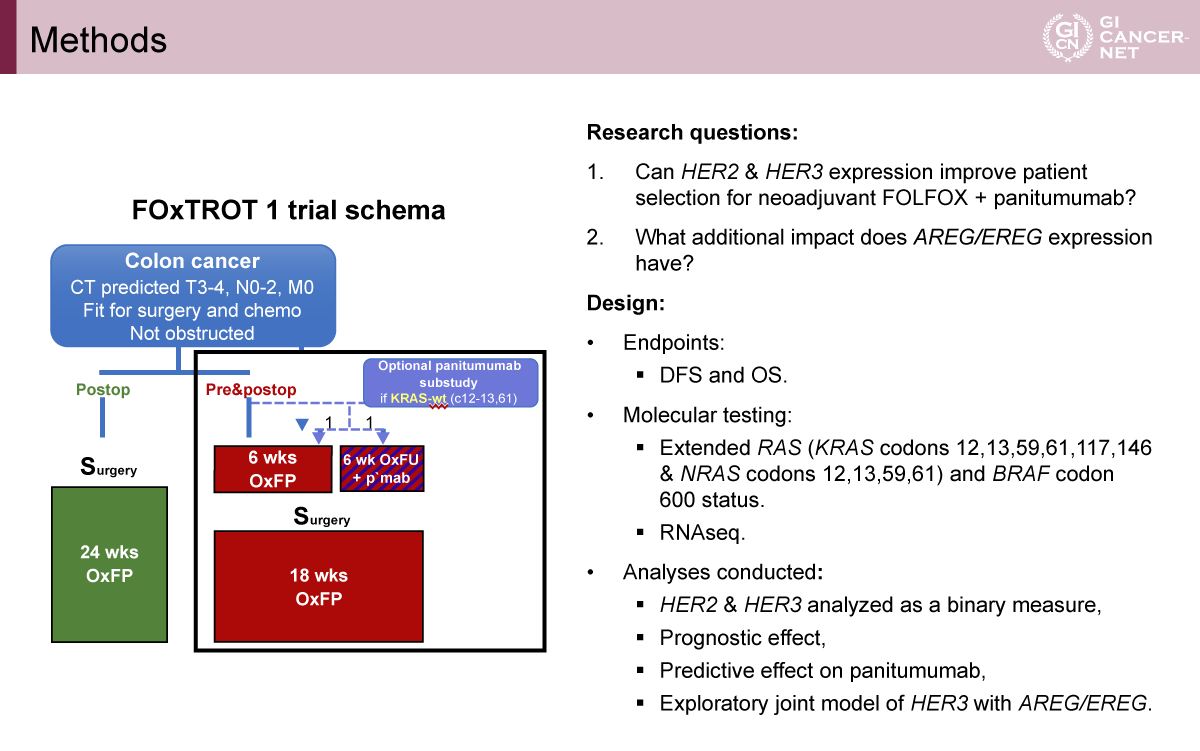
発表者の許可を得て掲載(approved by Jordan Wesley Appleyard)
結果
KRAS野生型と判定され、Panitumumab追加のサブ研究へランダム化された279例のうち、RASおよびBRAF野生型と判定されたのは169例(60.6%)であった。このうちmRNAのデータを利用できるのは157例であり、FOLFOX+Panitumumab群は85例、FOLFOX群は72例であった。
HER2高発現(50th percentile)は79例、HER2低発現は78例、HER3高発現(40th percentile)は88例、HER3低発現は69例にグループ分けされた。また、HER3とAREG/EREG(66th percentile)の共同評価が行われ、少なくとも一方が高発現の群が125例、いずれも低発現の群が32例に分けられた。フォローアップ期間の中央値は49カ月であった。
HER2高発現はFOLFOX群内ではDFS不良因子であった(HR=1.53、95% CI: 1.02-2.31、p=0.04)。一方、FOLFOX+Panitumumab群とFOLFOX群の比較では、HER2高発現群でDFSは51.7カ月 vs. 40.5カ月(HR=0.45、95% CI: 0.17-1.19)、OSは55.6カ月 vs. 46.7カ月(HR=0.40、95% CI: 0.12-1.38)であり、HER2低発現群でDFSは41.9カ月 vs. 37.3カ月(HR=0.60、95% CI: 0.23-1.59)、OSは51.6カ月 vs. 38.4カ月(HR=0.24、95% CI: 0.05-1.18)であった。HER2のmRNA発現はPanitumumabの効果と相関しなかった。
HER3は全体集団においてはDFSとOSいずれにおいても予後因子とならなかった。一方、HER3高発現群では、FOLFOX+Panitumumab群とFOLFOX群を比較すると、DFSは51.2カ月 vs. 40.3カ月(HR=0.37、95% CI: 0.14-0.97、p=0.04)、OSは57.6カ月 vs. 46.2カ月(HR=0.16、95% CI: 0.04-0.75、p=0.02)と有意に良好であった。HER3低発現群ではDFSは38.5カ月 vs. 36.7カ月(HR=0.80、95% CI: 0.29-2.22)、OSは50.4カ月 vs. 39.0カ月(HR=0.71、95% CI: 0.18-2.84)であり、有意差は認めなかった(図2)。
さらに、HER3に加えてAREG/EREGの高発現も共同評価すると、DFSは51.6カ月 vs. 39.7カ月(HR=0.38、95% CI: 0.17-0.82、p=0.01)、OSは57.0カ月 vs. 46.4カ月(HR=0.22、95% CI: 0.07-0.67、p=0.008)とPanitumumab上乗せの効果が高い患者選択が改善された(図3)。
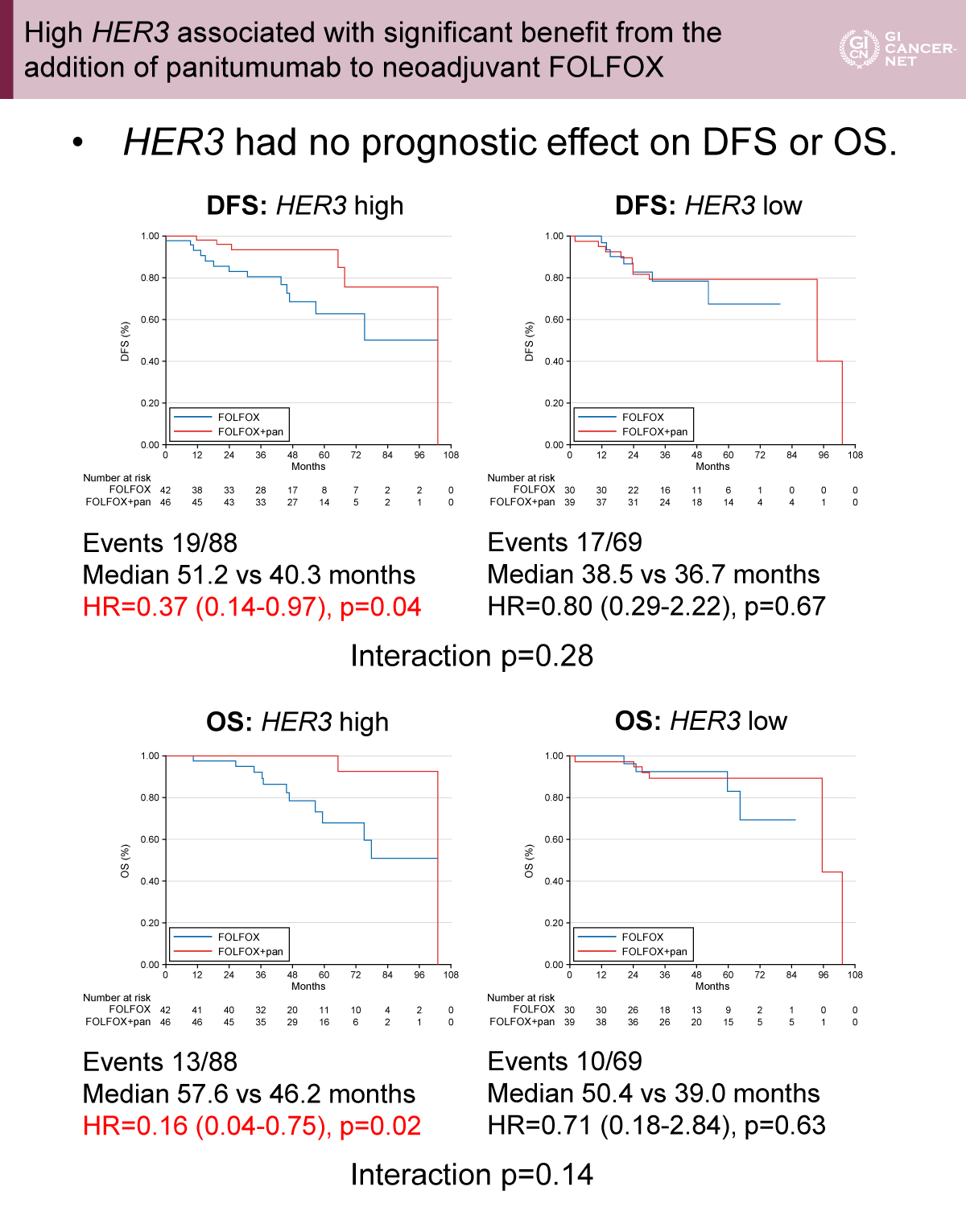
発表者の許可を得て掲載(approved by Jordan Wesley Appleyard)
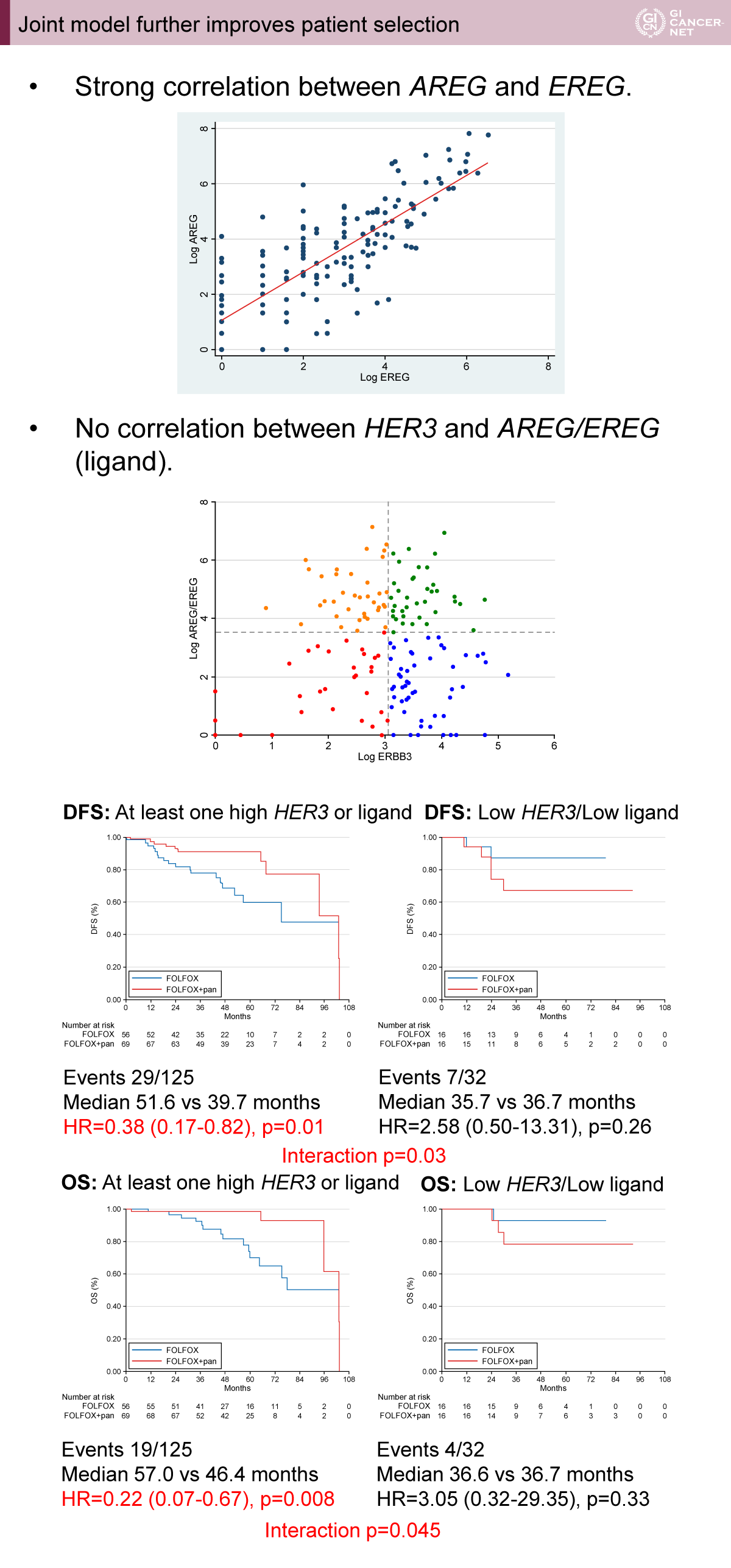
発表者の許可を得て掲載(approved by Jordan Wesley Appleyard)
結論
LACCにおけるバイオマーカー選択集団に対して、抗EGFR抗体を用いた分子標的治療により予後改善を目指す個別化医療の有用性が示唆された。
(レポート:愛知県がんセンター ゲノム医療センター 梅垣 翔)
References
- 1) Alberts SR, et al.: JAMA. 307(13): 1383-1393, 2012[PubMed]
- 2) Bridgewater JA, et al.: Lancet Oncol. 21(3): 398-411, 2020[PubMed]
- 3) Morton D, et al.: J Clin Oncol. 41(8): 1541-1552, 2023[PubMed]
- 4) Germani MM, et al.: J Clin Oncol. 43(29): 3184-3197, 2025[PubMed]
- 5) Seligmann JF, et al.: JAMA Oncol. 4(4): 564-568, 2018[PubMed]
関連サイト
- ・FOxTROT試験[ClinicalTrials.gov][ASCO 2019学会レポート]
- ・PICCOLO試験[ClinicalTrials.gov][ASCO 2011学会レポート]










谷口 浩也先生
愛知県がんセンター 薬物療法部 医長