胆道癌
FGFR2融合/再構成陽性胆道癌に対する高選択的FGFR2阻害薬Lirafugratinibの有効性と安全性に関する第I/II相試験
Efficacy and safety of lirafugratinib in patients with FGFRi-naïve cholangiocarcinoma harboring FGFR2 fusions/rearrangements
Antoine Hollebecque, et al.
Expert’s view
近年、切除不能または再発の胆道癌に対する薬物療法は大きく2つの要因により治療成績の向上が認められている。
1つは一次薬物療法において、GemcitabineおよびCisplatin併用療法にそれぞれS-1、Durvalumab、Pembrolizumabの上乗せが検証されたことで、3剤併用療法が標準治療として確立したことである。
そしてもう1つが二次薬物療法において、遺伝子変異に基づく個別化医療が進んでおり、次々と新たな薬剤が開発されている点である。FGFR2融合遺伝子または再構成陽性の胆道癌は胆道癌の5~10%程度に認められ、本邦ではPemigatinib、Futibatinib、Tasurgratinibが承認、使用されている。
本発表ではLirafugratinibが従来のFGFR2阻害薬とは異なる安全性プロファイルをもつことが示唆される結果が示された。また、良好な有効性の結果に加えて、本学会ではほかに、FGFR阻害薬の治療歴がある患者に対するLirafugratinibの治療成績も報告されており、また、耐性機序に関する基礎的検討も進められていることから、これらの薬剤の使い分けが今後、議論になると考えられる。
本サイトでは、FGFR2阻害薬のほかにIDH1陽性胆道癌に対するIvosidenib、HER2陽性胆道癌に対するTrastuzumab Deruxtecanの治療成績を取り上げてきたが、これらの薬剤は間もなく日常診療で使用可能になる見込みである。胆道癌の薬物療法が益々発展していくことが期待される。
(コメント・監修:金沢医科大学 腫瘍内科 准教授 寺島 健志)
背景
FGFR2融合/再構成は胆道癌における代表的なドライバー遺伝子異常であり、既存のFGFR阻害薬は臨床的有効性を示してきた。一方、多くのFGFR阻害薬はFGFR1やFGFR3など他アイソフォームも阻害するため、高リン血症や皮膚・爪障害などのオフターゲット毒性が課題とされてきた。Lirafugratinibは、FGFR2に対して高い選択性を有する新規阻害薬であり、より良好な安全性プロファイルと有効性の両立が期待されている。
試験デザイン
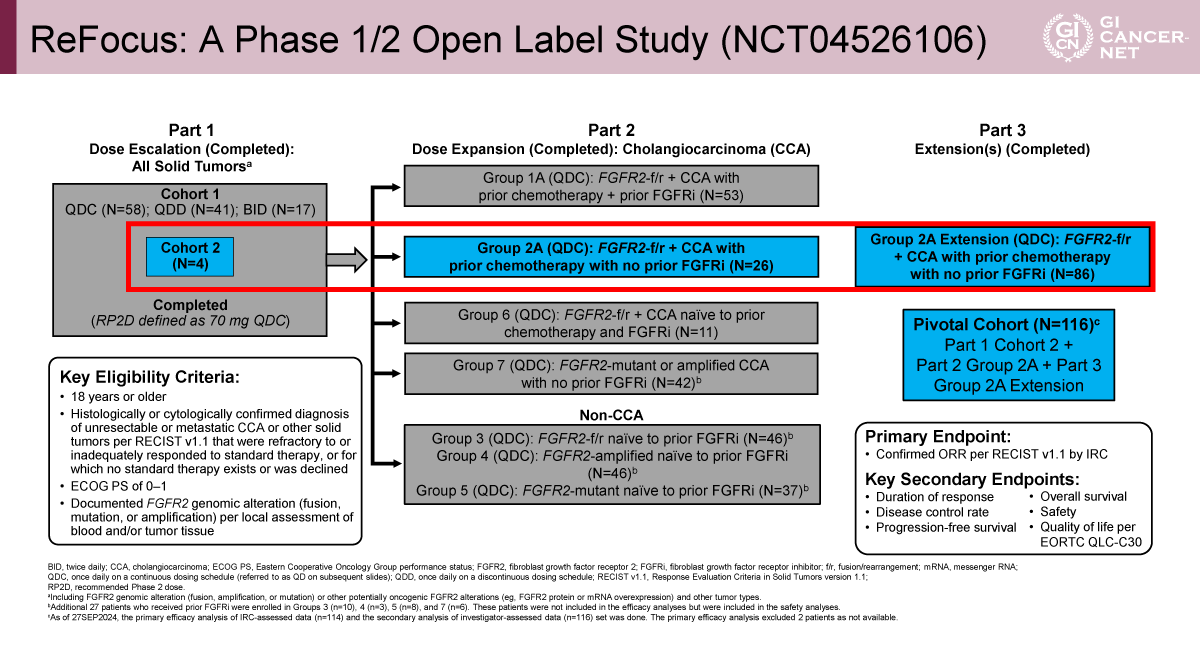
主な適格規準は、18歳以上、病理組織学的に診断された切除不能または遠隔転移胆道癌、化学療法既治療、FGFR阻害薬未治療(FGFRi-naïve)、ECOG PSは0-1、FGFR2融合/再構成陽性であった(図1)。
主要評価項目は、独立画像判定委員会(IRC)による奏効割合(ORR)で、推奨第II相用量(RP2D)は70mg QD(連日投与)で、解析対象は114例(主要有効性解析)であった。
発表者の許可を得て掲載(approved by Antoine Hollebecque)
患者背景
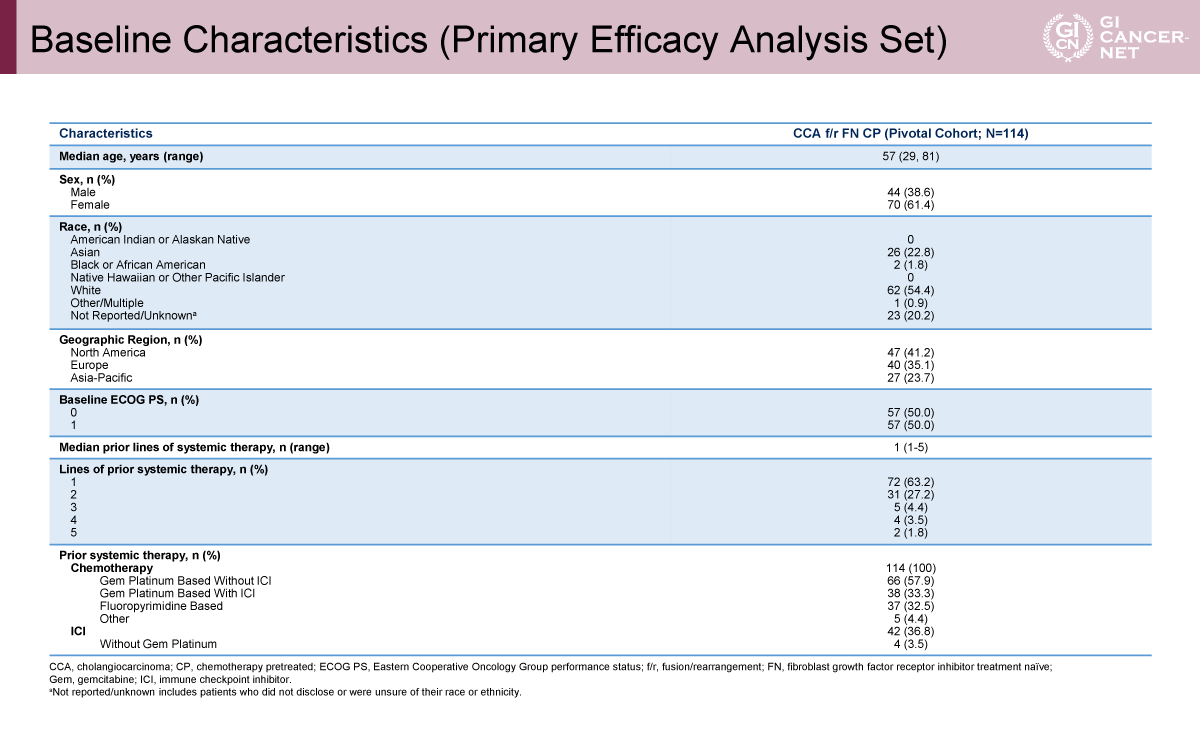
主要有効性解析集団には114例が含まれ、年齢中央値は57歳であった。女性は61.4%を占め、人種別では白人が54.4%、アジア系が22.8%であった。ECOG PSは0および1がそれぞれ50%であった。既治療ライン数は、1ラインが63.2%、2ラインが27.2%、3ライン以上が9.7%であった。前治療としては、90%以上の患者がGemcitabine系レジメンを含む治療歴を有しており、免疫チェックポイント阻害薬を含む治療歴を有する患者も3分の1強に認められた(表1)。
発表者の許可を得て掲載(approved by Antoine Hollebecque)
有効性
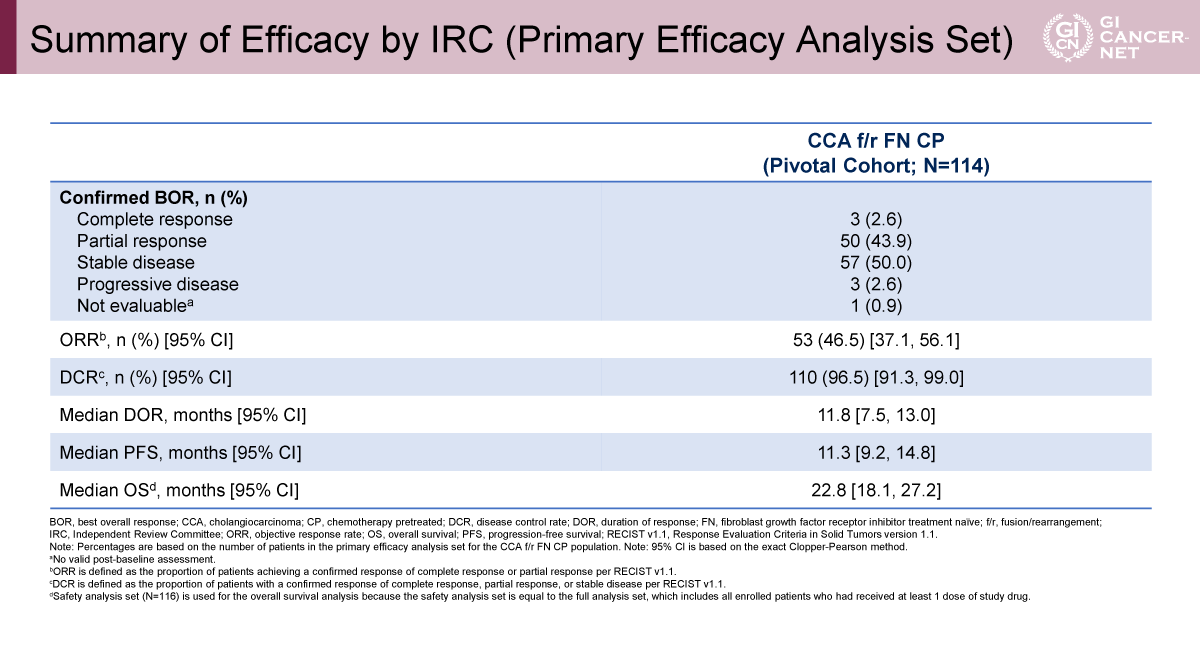
IRC評価による主要有効性解析で、Lirafugratinibは以下のように高い腫瘍縮小効果を示した(表2)。
- ORR:46.5%(95% CI: 37.1-56.1)
- DCR:96.5%(95% CI: 91.3-99.0)
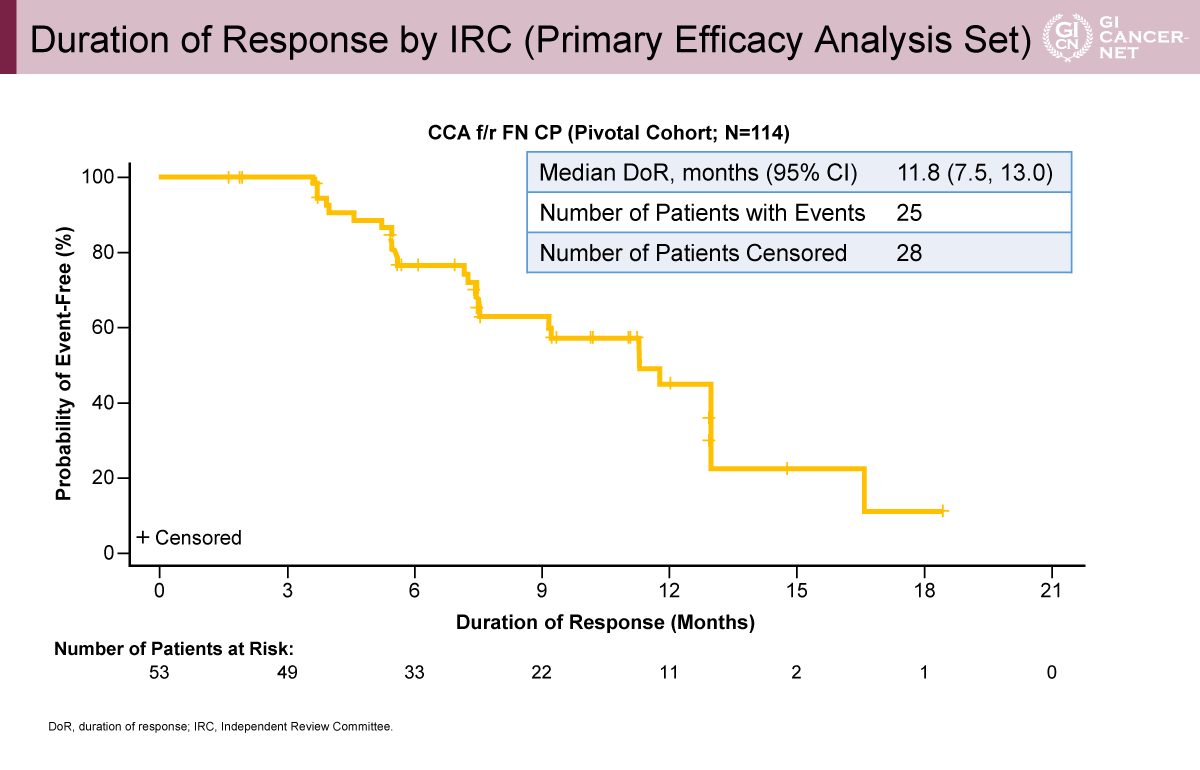
- DoR中央値:11.8カ月(95% CI: 7.5-13.0)
- PFS中央値:11.3カ月(95% CI: 9.2-14.8)
- OS中央値:22.8カ月(95% CI: 18.1-27.2)
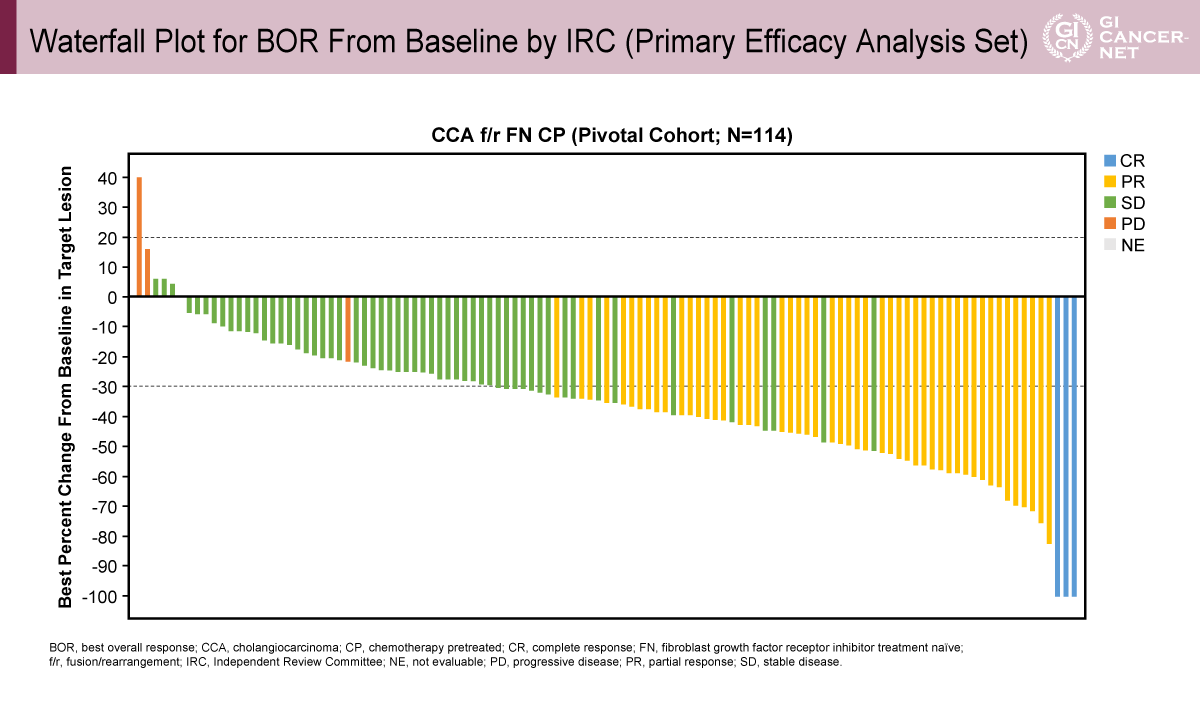
ウォーターフォールプロットでは、多くの症例で腫瘍縮小が認められ、奏効の持続も比較的良好であった(図2、図3)。
発表者の許可を得て掲載(approved by Antoine Hollebecque)
発表者の許可を得て掲載(approved by Antoine Hollebecque)
発表者の許可を得て掲載(approved by Antoine Hollebecque)
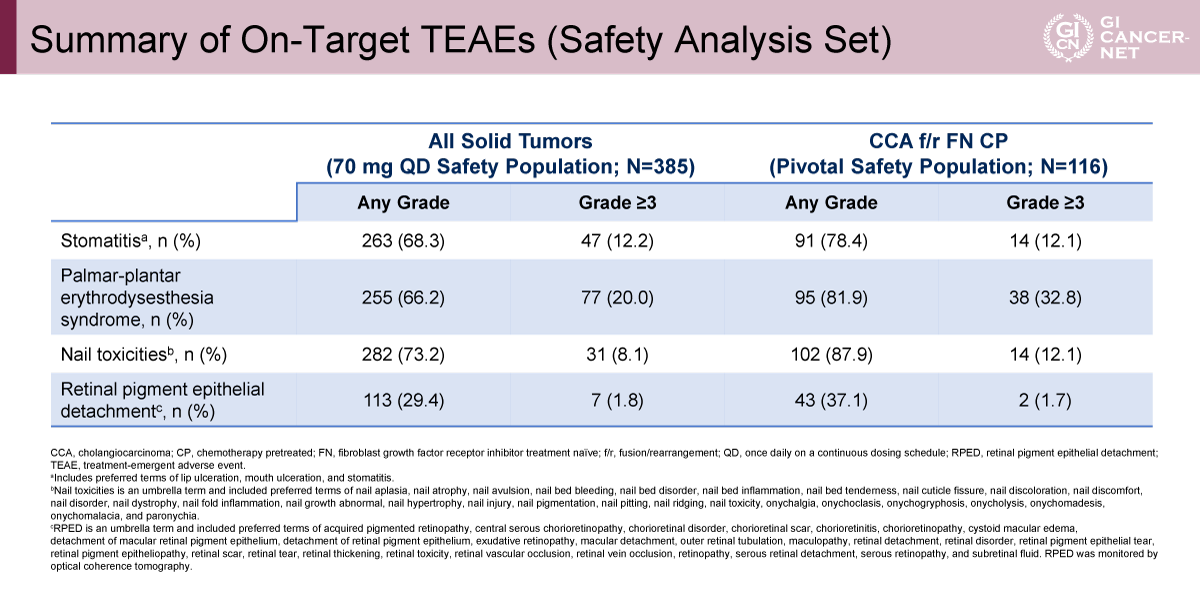
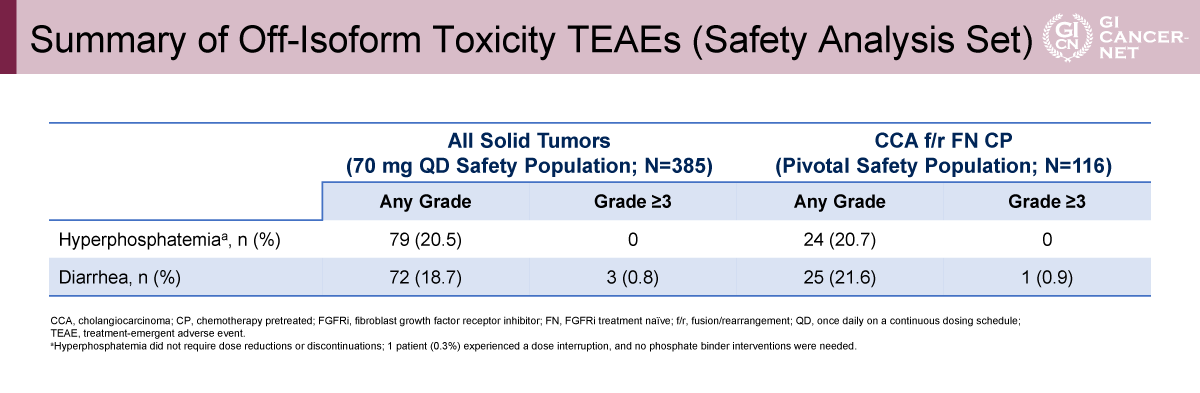
安全性
結論
本解析により、Lirafugratinibは標準治療後に増悪したFGFR2融合/再構成陽性かつFGFR阻害薬未治療の胆道癌において、良好な奏効割合、奏効持続期間、そして管理可能な安全性プロファイルを示した。
(レポート:国立がん研究センター東病院 肝胆膵内科 澁木 太郎)
関連サイト
- ・REFOCUS試験[ClinicalTrials.gov]










寺島 健志先生
金沢医科大学 腫瘍内科 准教授