胃癌
食道胃接合部癌
局所進行切除可能胃癌/食道胃接合部癌に対する周術期Toripalimab併用化学療法の第II相無作為化試験:NEOSUMMIT-01試験3年追跡結果
Perioperative PD-1 Antibody Toripalimab Combined with Chemotherapy versus Chemotherapy Alone in Locally Advanced Gastric or Gastroesophageal Junction Cancer: 3-Year Follow-Up of the Prospective, Randomized, Phase 2 NEOSUMMIT-01 Trial
Shu-Qiang Yuan, et al.
Expert’s view
2025年は、MATTERHORN試験において、胃癌の周術期化学療法FLOT療法に、PD-L1抗体であるDurvalumabを併用することで、EFSとOSの延長効果が示されたが、ベースとなる術前術後FLOT療法は、ドイツで開発され、主に欧米で用いられている治療であった。アジアにおいては、韓国ではPRODIGY試験により術前DOS療法と術後S-1療法が、中国ではRESOLVE試験により術前術後SOX療法が、それぞれ標準治療となっている。
NEOSUMMIT-01試験は、術前術後SOX療法に対してPD-1抗体であるToripalimabを併用することの有用性を探索的に検討した無作為化II相試験である。MATTERHORN試験と異なるのは、ベースライン化学療法がFLOTのような3剤併用ではなく、SOXと2剤併用であることである。そして、アジア人患者が少ないMATTERHORN試験と比べ、全員が中国からの患者であり、手術手技や、患者背景などが若干異なることである。結果としては、Toripalimabの術前術後SOX療法に対する上乗せ効果が示されたが、3年EFSは74%と、MATTERHORN試験の約65%と比較しても高い数字となっている。3年OSでも81.3%と、68.6%だったMATTERHORN試験よりも高くなっている。もちろん観察期間が不十分であり、患者背景でもCPSスコアや年齢など両群でインバランスなところが多く、それがこの試験の結果につながっていると考えられた。
腹膜播種再発が少ないことは興味深かったが、CPSスコア別のHRなど、みたいデータの一部しか発表されていないため、今後の発表に注目したい。本邦の胃癌の周術期治療はMATTERHORN試験のいわゆるD-FLOT療法が標準治療のひとつとなるが、高齢者など、3剤併用でのダメージが大きいと思われる集団では、周術期に2剤を用いたりすることもある。また日本では手術先行であとから術後化学療法を行うことが標準治療である。現在JCOG1509試験として、術前SOX療法の有用性を検証しているが、結果が出るのは数年後と思われる。周術期SOX+ICI療法は、D-FLOTが不耐の患者にとって選択肢になりうるが、今回の発表はrPIIであるが、同じPD-1抗体であるSerplulimabを胃癌周術期SOX療法に併用したASTRUM-006試験がポジティブな結果を出している。この試験はCPS>5のみに対象者を絞り、術後がSerplulimab単剤となっているが、それでもポジティブな結果がプレスリリースで報告されている。
胃癌周術期化学療法も本格的にICIの時代に入ってきているが、本試験だけでなく、他の試験の結果も待ちたいと思う。
(コメント・監修:国立がん研究センター中央病院 消化管内科/頭頸部・食道内科 科長 加藤 健)
背景
胃癌および食道胃接合部(GEJ)癌において、周術期化学療法は切除可能局所進行例に対する標準治療として確立している1,2)。一方、進行/再発例ではPD-1/PD-L1阻害薬を含む免疫療法が治療成績を改善しており3,4)、免疫療法を周術期治療へ導入する戦略が注目されている。
NEOSUMMIT-01試験は、切除可能な局所進行胃癌/GEJ癌に対して、周術期化学療法に PD-1抗体Toripalimabを追加することの有効性を検証する目的で実施された。これまでに、腫瘍縮小グレード(TRG):0/1割合(44.4% vs. 20.4%、p=0.009)および病理学的完全奏効(pCR)割合(22.2% vs. 7.4%、p=0.030)の有意な改善が報告されている5)。本レポートでは、追跡期間を延長した3年追跡結果および再発様式に関する解析結果を概説する。
NEOSUMMIT-01の試験デザイン
本試験はオープンラベル無作為化第II相試験として実施された。対象は、治療歴のない切除可能な局所進行胃癌またはGEJ癌(cT3-4a N+ M0)で、18歳から75歳、ECOGパフォーマンスステータス0あるいは1の患者であった。過去に胃癌に対して化学療法、放射線療法、免疫療法あるいは手術歴を有する患者、5年以内に他の悪性疾患を有する患者、治療薬に対するアレルギー歴を有する患者は除外された。患者は1:1に無作為化され、それぞれ下記の通りに実施された(図1)。
- 化学療法群:術前3コース+術後5コースのSOXまたはXELOX療法
- Toripalimab+化学療法群:同化学療法にToripalimabを併用し、術前3コース後に手術を施行、さらに術後5コースの併用療法後に最大6カ月間のToripalimab単剤療法
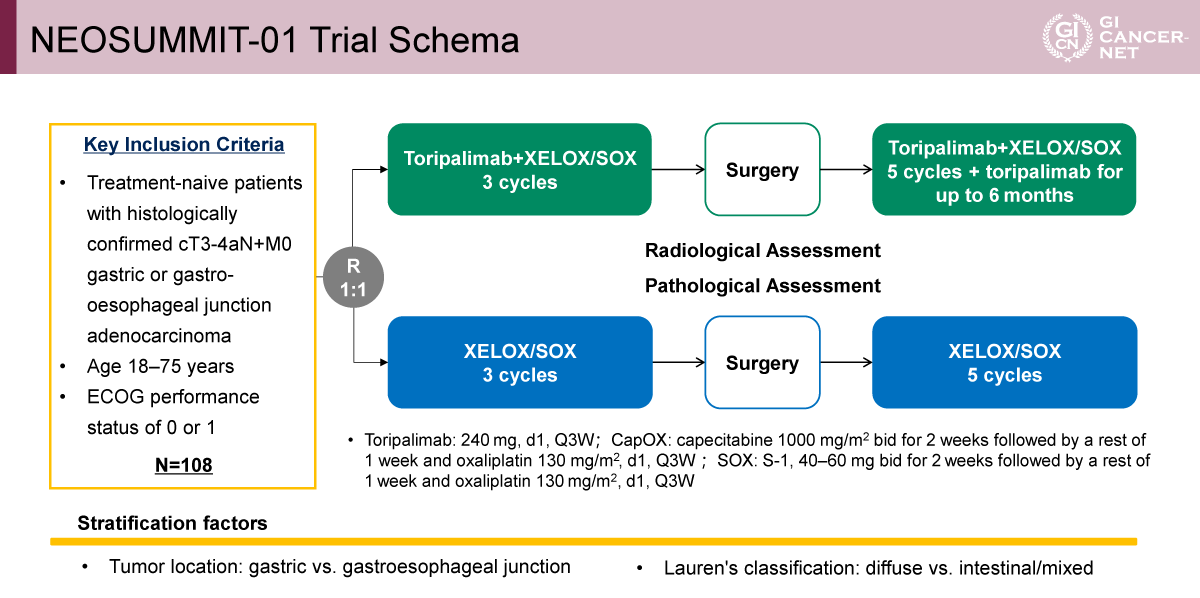
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
治療効果は画像評価および病理学的評価により判定され、腫瘍原発部位(胃 vs. GEJ)およびLauren分類(びまん型 vs. 腸型/混合型)で層別化が行われた。
主要評価項目はTRG 0/1割合とされ、副次評価項目としてpCR割合、R0切除割合、無イベント生存期間(EFS)、全生存期間(OS)、無再発生存割合、奏効割合、病勢制御割合、および安全性が設定された。本解析ではITT集団を主解析とし、pMMR集団およびPer-protocol集団における解析も実施された。
Toripalimab併用療法群と化学療法単剤群はバランス良く割り付けられた
2019年10月から2022年6月までに108例が登録された。臨床データカットオフ(2025年8月)時点での追跡期間中央値は43.2カ月(IQR: 36.6-53.7カ月)であった。ITT解析では、周術期Toripalimab+化学療法群および化学療法単独群にそれぞれ54例ずつ無作為割付された。Toripalimab併用群では全例が術前治療術後治療を受け、51例が手術を受け、32例が術後に少なくとも5コースのToripalimab併用化学療法を完遂した(図2)。
登録された108例の患者背景は、Toripalimab併用群(n=54)と化学療法単独群(n=54)で概ね均衡していた。全体集団において、年齢中央値は60歳(範囲26-74)、男性/女性は64.8%/35.2%、ECOG PS 0/1は66.7%/33.3%、原発部位:胃/GEJは65.7%/34.3%、T因子:cT3/cT4aは35.2%/64.8%、N因子:cN1/cN2/cN3は42.6%/40.7%/16.7%、Lauren分類:腸型/混合型は35.2%/64.8%、印鑑細胞癌:あり/なしは23.1%/76.9%、治療レジメン:SOX/XELOXは53.7%/46.2%、PD-L1発現:CPS<5/CPS≧5/不明は65.7%/15.7%/18.5%、MMRステータス:pMMR/dMMR/不明は86.1%/5.6%/8.3%であった(表1)。

発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
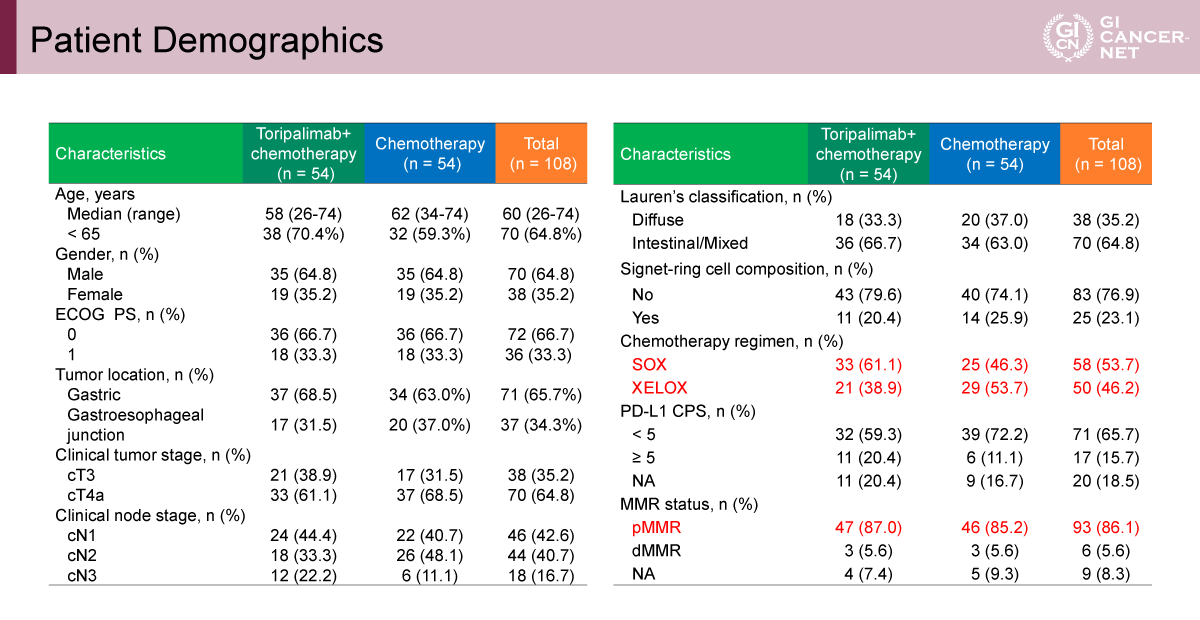
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
Toripalimabの併用により3年EFS/OSの改善を認めた
周術期Toripalimab+化学療法は、化学療法単独と比較してEFSを有意に改善した。3年EFSは、Toripalimab+化学療法群74.7%(95% CI: 63.6-87.7%)、化学療法単独群56.2%(95% CI: 43.3-73.0%)であり、Toripalimab併用により有意な改善が認められた(HR=0.51、95% CI: 0.27-0.98、p=0.044)。追跡期間中、Toripalimab併用群ではEFS中央値は未到達であったのに対して化学療法単独群では38.2カ月(95% CI: 27.2-NE)であった(図3)。
周術期Toripalimab+化学療法は、化学療法単独と比較してOSを有意に改善した。3年OSはToripalimab併用群81.3%(95% CI: 71.4-92.4%)、化学療法単独群72.2%(95% CI: 61.2-85.2%)であり、Toripalimab併用群で有意に良好であった(HR=0.45、95% CI: 0.21-0.95、p=0.036)。追跡期間中はEFSおよびOS中央値はいずれも併用群では未到達であった(図4)。
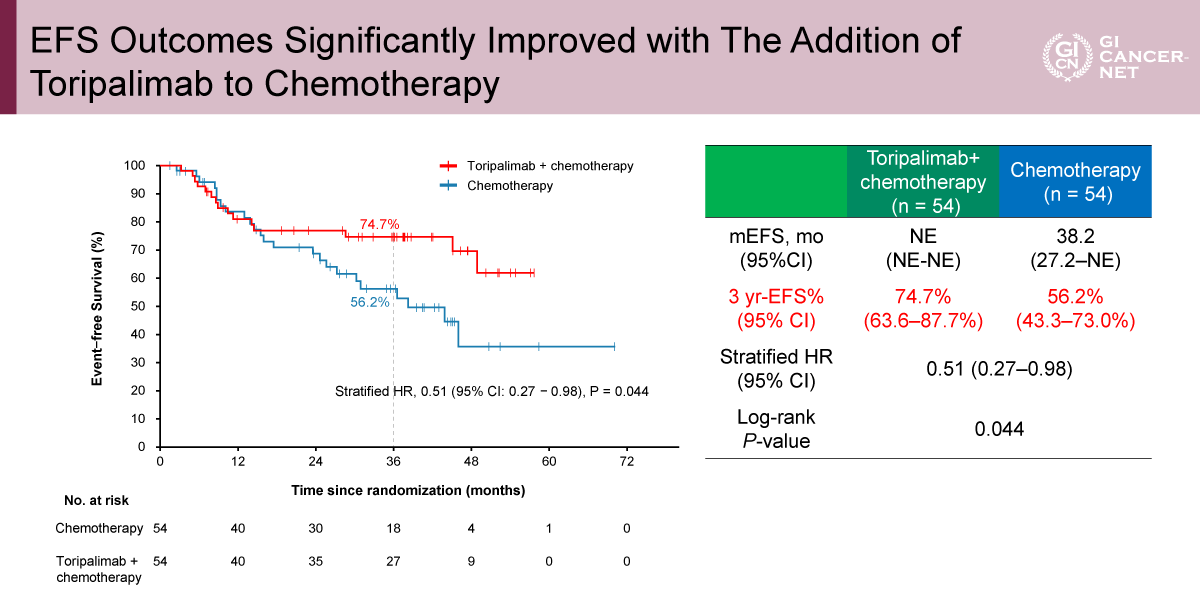
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
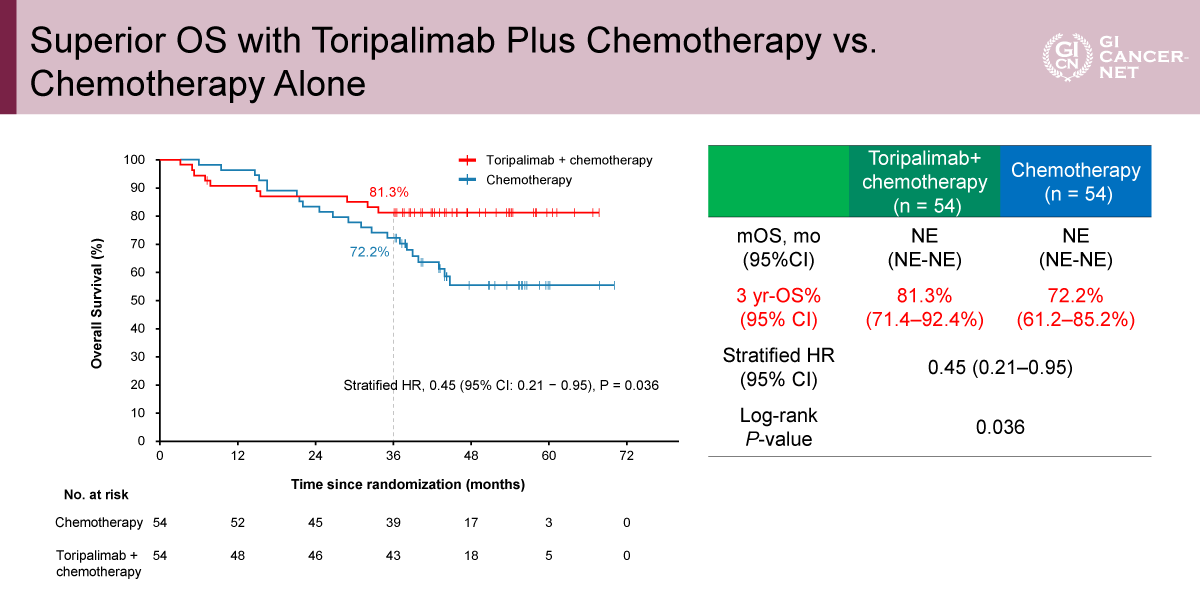
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
サブグループ解析においてもToripalimab上乗せによるベネフィットが示された
pMMR集団に限定した解析においても、周術期Toripalimab+化学療法は化学療法単独と比較して、一貫した生存期間延長を示した。3年EFSは75.5% vs. 53.4%(HR=0.47、p=0.035)、3年OSは80.6% vs. 71.7%(HR=0.43、p=0.036)であり、OSにおいて有意な改善が認められた(図5)。
Per-protocol集団においても、周術期Toripalimab+化学療法は化学療法単独と比較して、一貫してEFSおよびOSの改善を示した。3年EFSは77.8% vs. 58.7%(HR=0.49、p=0.043)、3年OSは84.3% vs. 75.0%(HR=0.40、p=0.028)であった。これらの結果は、本試験の主要解析結果の頑強性を支持するものであった(図6)。
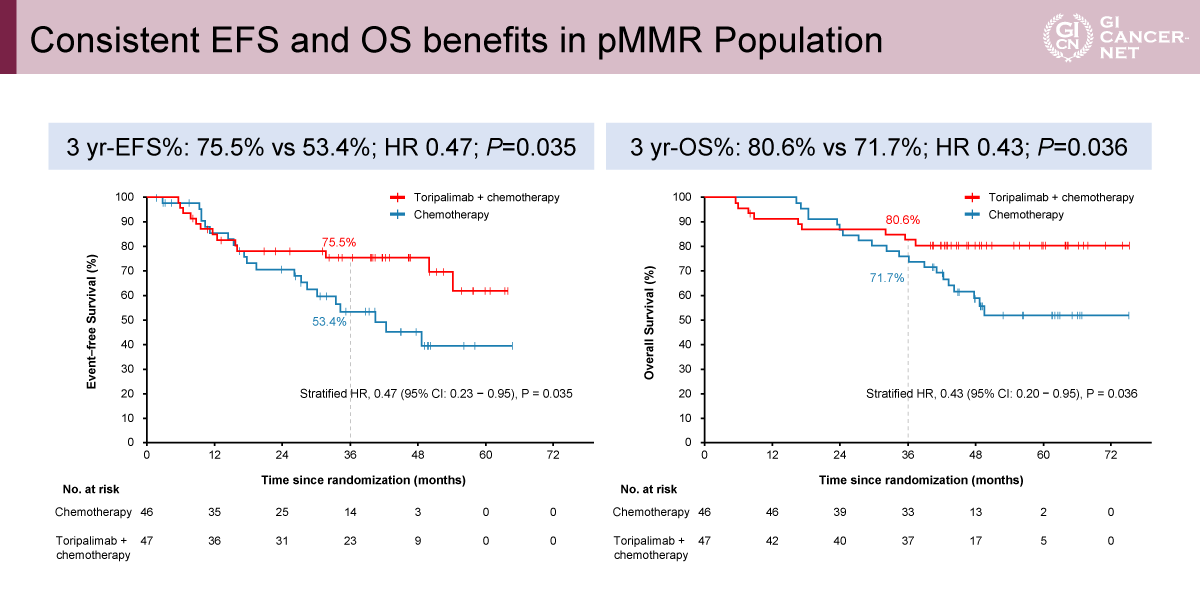
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
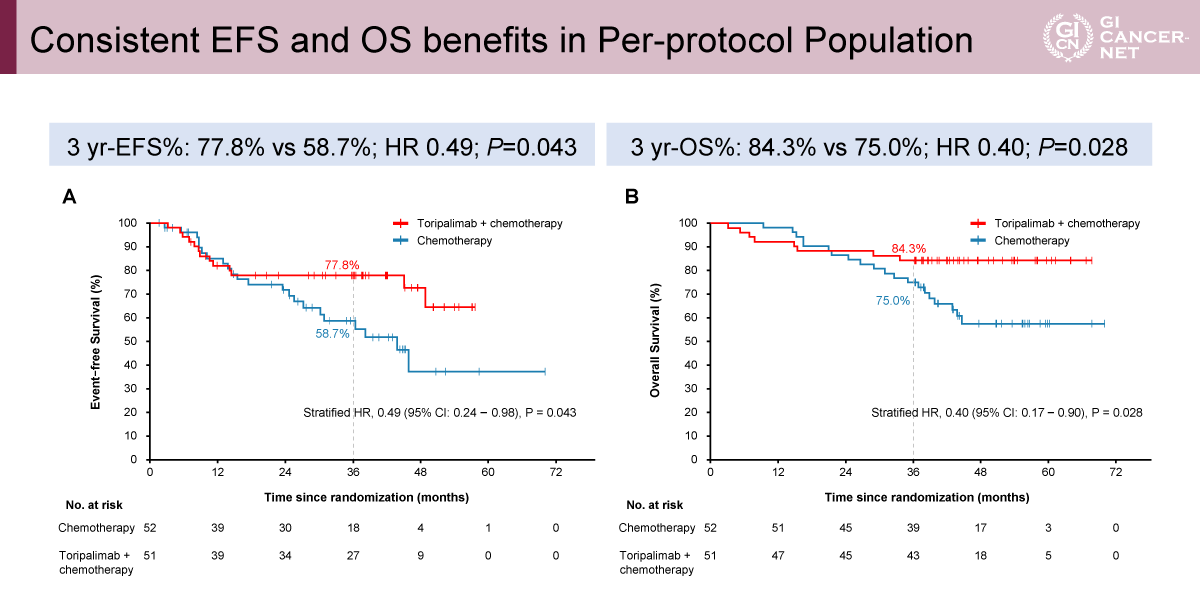
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
再発様式の解析ではToripalimab併用療法に腹膜転移の抑制効果示す
初回再発部位の解析では、周術期Toripalimab+化学療法は化学療法単独と比較して、全再発割合が有意に低下していた(18.5% vs. 38.9%、差:−20.4%、p=0.019)。特に腹膜転移は、Toripalimab併用群13.0%、化学療法単独群29.6%と有意に抑制されていた(差:−16.6%、p=0.034)。一方、血行性転移、リンパ節再発、局所再発については、両群間で有意差は認められなかった(表2)。
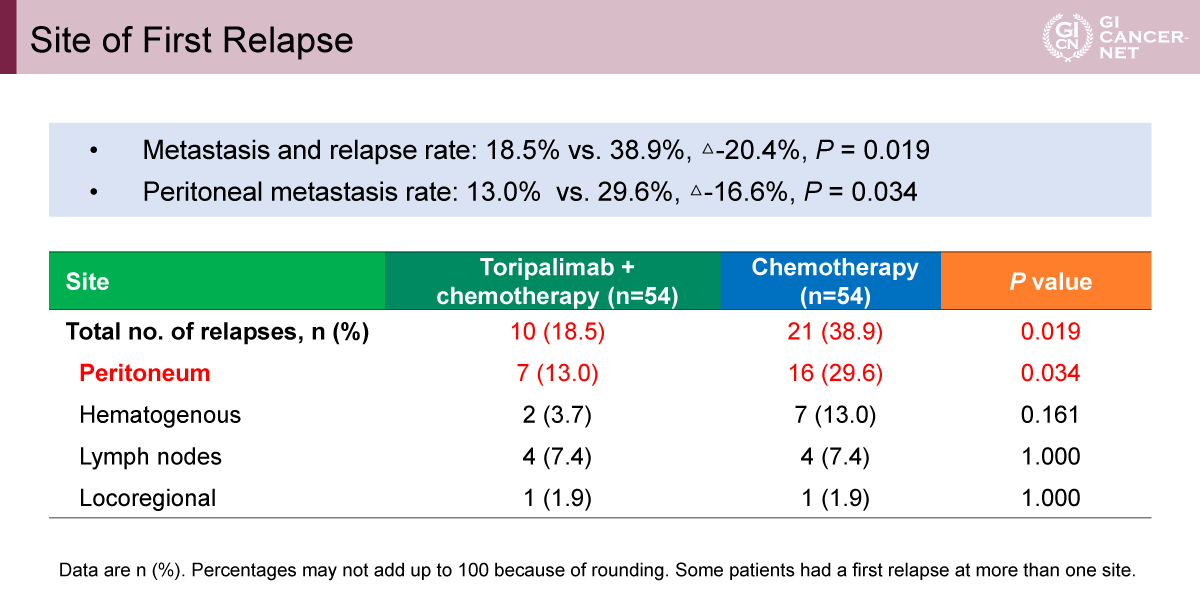
発表者の許可を得て掲載(approved by Shu-Qiang Yuan)
考察
NEOSUMMIT-01試験は第II相試験ではあるものの、3年という比較的長期の追跡において、EFSおよびOSの両方で一貫した改善を示した点が注目される。既報の病理学的奏効割合の改善と合わせると、Toripalimabの周術期導入が腫瘍免疫環境を改善し、長期予後に寄与している可能性が考えられる。
さらに、本試験では腹膜再発の有意な抑制が確認された。腹膜転移は局所進行胃癌における主要な再発様式であり、治癒切除後の予後を規定する重要な因子であることから、周術期免疫療法が微小残存病変や腹膜播種形成過程に介入している可能性が示唆される。また、本治療効果はpMMR集団およびPer-protocol解析においても一貫して認められており、結果の再現性および頑強性が支持された点は重要である。一方、症例数が限られていること、オープンラベル試験であることから、今後は第III相試験による検証が求められる。
結論
局所進行切除可能胃癌/GEJ癌において、周術期Toripalimab併用化学療法は、化学療法単独と比較して3年EFSおよびOSを有意に改善し、再発割合、特に腹膜再発を有意に低下させた。これらの生存利益はpMMR集団およびPer-protocol解析においても維持されており、本治療戦略は周術期治療において新たに有望な選択肢となる可能性が示唆された。
(レポート:国立がん研究センター中央病院 消化管内科 亀石 眞)
References
- 1) Al-Batran SE, et al.: Lancet. 393(10184): 1948-1957, 2019[PubMed]
- 2) Costa M, et al.: Cancers. 16(23): 4036, 2024[MDPI]
- 3) Janjigian YY, et al.: J Clin Oncol. 42(17): 2012-2020, 2024[PubMed]
- 4) Lowery MA, et al.: Eur J Cancer. 231: 115807, 2025[PubMed]
- 5) Yuan SQ, et al.: Nat Med. 30(2): 552-559, 2024[PubMed]
関連サイト
- ・NEOSUMMIT-01試験[ClinicalTrials.gov]
- ・MATTERHORN試験[ClinicalTrials.gov][ASCO 2025学会レポート][論文紹介][ESMO 2025学会レポート]
- ・PRODIGY試験[ClinicalTrials.gov][論文紹介][論文紹介][ESMO 2019学会レポート]
- ・RESOLVE試験[ClinicalTrials.gov][論文紹介]
- ・JCOG1509試験[JRCT]
- ・ASTRUM-006試験[Press Release]










加藤 健先生
国立がん研究センター中央病院 消化管内科/頭頸部・食道内科 科長