大腸癌
大腸癌患者を対象としたALTAIR無作為化試験の適格性に与える術後ctDNA動態の影響:臨床試験の登録に対する影響
Impact of Postoperative ctDNA Dynamics on Eligibility for ALTAIR Randomized Trial in Patients with Colorectal Cancer: Implications for Clinical Trial Enrollment
Hideaki Bando, et al.
Expert’s view
ctDNAを用いたMRD検査は、再発リスクの層別化という段階を超え、ctDNAステータスに基づく治療介入という次のステージに進んでいる。MRD陰性例における術後補助療法のde-escalationに関する報告が蓄積されつつある一方で1,2)、ALTAIR試験はctDNA陽性例に対する早期治療介入の有用性を検証した第III相試験であったが、残念ながら結果はnegativeであった。しかしながら、癌種は異なるものの、術後ctDNA陽性の高リスク筋層浸潤膀胱癌に対してAtezolizumabがOSを延長したとの報告もなされており3)、ctDNA陽性例を対象とした治療開発は今後も多様な癌種において加速していくだろう。そのような流れの中で、ctDNA陽性例をいかに効率よく同定し、いかなる臨床試験デザインによって検証すべきかは、極めて重要かつ本質的・実用的な課題である。
本報告では、術後MRD陰性例や術後補助化学療法でctDNAが陰性化した患者においても、サーベイランス中にctDNAが陽性化するケースが存在すること、さらに早期再発により試験登録に至らない症例ではctDNA量が高値である傾向が示された。これらは、今後のMRD陽性例を対象としたTreatment on Molecular Recurrence(TOMR)試験を設計する上で、極めて重要な基盤データである。また、本研究により、当初の想定を大きく上回る規模での患者スクリーニングが必要であることが明らかとなった。このことは、本領域での治療開発の成否が、スクリーニング体制の整備、患者紹介ネットワークの構築、さらにはDCTの積極的活用に依存することを示唆しており、引き続き“日本向き”であることが実感できる。一方で、「TOMR試験は本当に必要なのか」「ctDNA陽性を臨床上の再発とみなし切除不能例に準じた治療薬を早期に導入することで構わないのではないか」という根源的な問いも、常に我々の前に突き付けられている。少なくともctDNA陽性例において、molecular responseやDFS延長のみをもって治療価値を論ずることには本質的な限界がある。真に目指すべきゴールは、再発そのものを減らし、最終的にOSを改善することである。その達成に直結する治療戦略、そしてそれに特化した治療薬が開発されることを夢見ている。
(コメント・監修:愛知県がんセンター 薬物療法部 医長 谷口 浩也)
背景
大腸癌術後に体内にわずかに残存した癌(molecular residual disease: MRD)を検出できるctDNA検査が開発され、術後ctDNA陽性は大腸癌術後再発リスクの上昇と強く相関することが明らかになってきており4,5)、ctDNA陽性例を対象とする治療強化試験も進行中である5,6)。CIRCULATE-Japanでは、ctDNAの経時的変化を追う前向き観察コホート研究GALAXY試験と、標準的な術後補助療法(adjuvant chemotherapy: ACT)を行った後にctDNA陽性となった患者を対象にFTD/TPIとプラセボを比較する第III相試験(ALTAIR試験)が行われている。今回の報告では、ALTAIR試験の適格性や登録に与える影響が検討された。
方法
Stage II〜IVの切除可能大腸癌患者に対して、術後にSignatera™を用いてctDNAを経時的に(術後1、3、6、9、12、18、24カ月)測定した。ALTAIR試験のctDNAに基づく適格基準はACT後にctDNA陽性かつMRD検出から3カ月以内にCT画像上の臨床的再発がない症例とされた。ALTAIR参加施設に登録された患者における術後ctDNAの推移を解析し、適格基準を満たす割合を算出した。患者登録に関する要因を正確に評価するため、ALTAIR試験に参加していない施設の患者は本解析から除外した。これは参加施設への患者紹介自体が登録率に影響を与える交絡因子となり得るためである。MRD陽性は術後2〜10週のうちにctDNA陽性と定義した。
結果
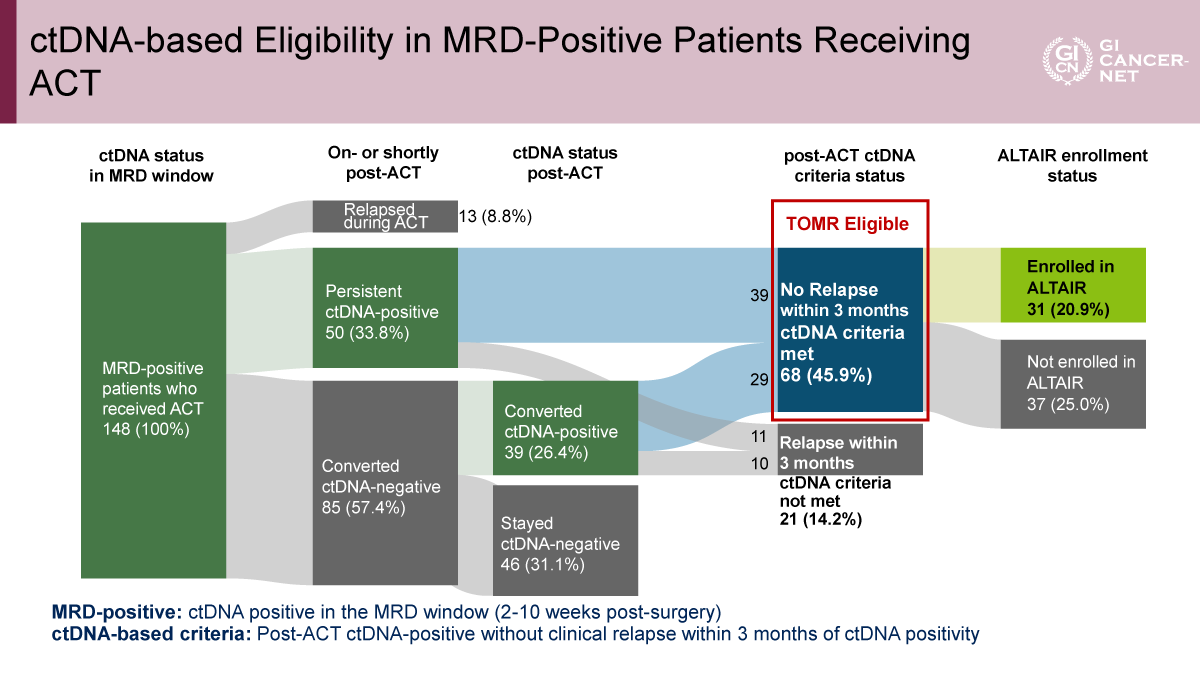
ALTAIR参加施設におけるGALAXY試験への登録は2,016例で、そのうち術後MRD陽性例は290例(14.4%)であった。MRD陽性のうちACT施行例は148例であった。そのうち、補助療法においてもctDNA陽性のままであった患者39例と、いったんctDNAが陰性となったが再びctDNA陽性となった29例の計68例(45.9%)がALTAIR試験の候補となり、このうち31例がALTAIR試験に登録された(図1)。
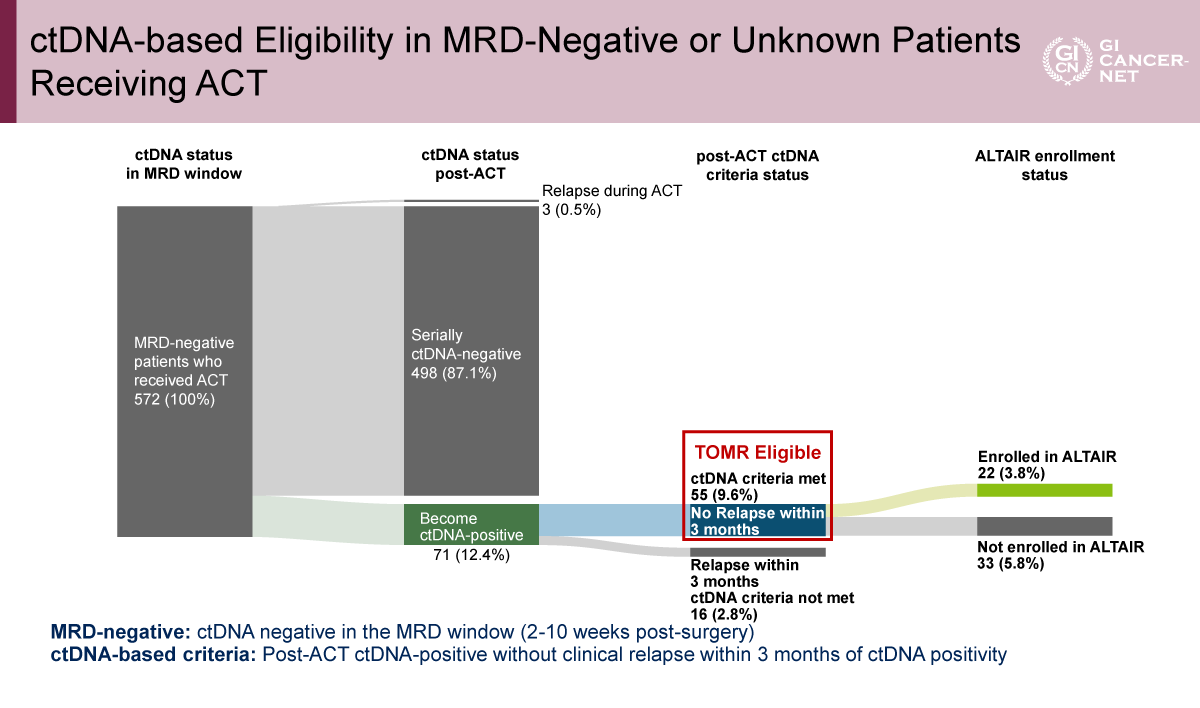
一方、術後MRD陰性(or unknown)は1,726例のうちACT施行例では572例であり、ACT後にctDNA陽性化したのは71例、ALTAIR試験の候補となったのは55例(9.6%)、うち22例がALTAIR試験に登録された(図2)。
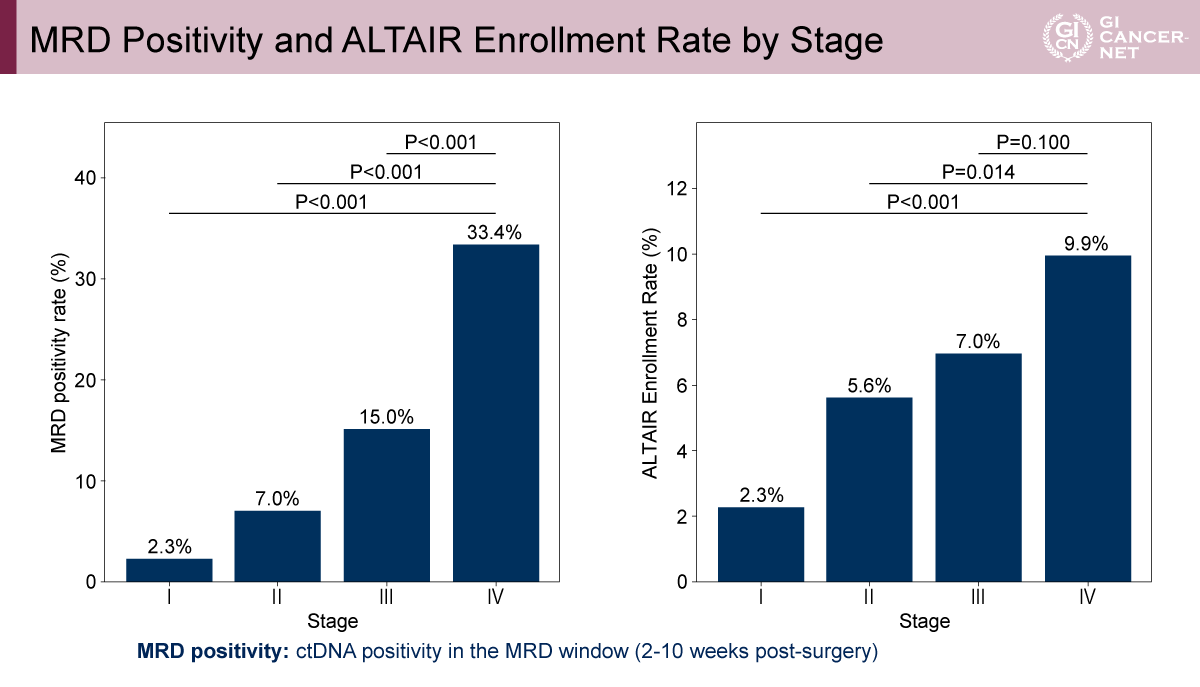
Stage別の解析ではstage IIで15.5%(15/97)、stage IIIで14.3%(71/498)、stage IVで30.7%(35/114)であった。Stage別(stage I/II/III/IV)のMRD陽性率は順に2.3%/7.0%/15.0%/33.4%であり、ALTAIR試験への登録率は2.3%/5.6%/7.0%/9.9%であった(図3)。
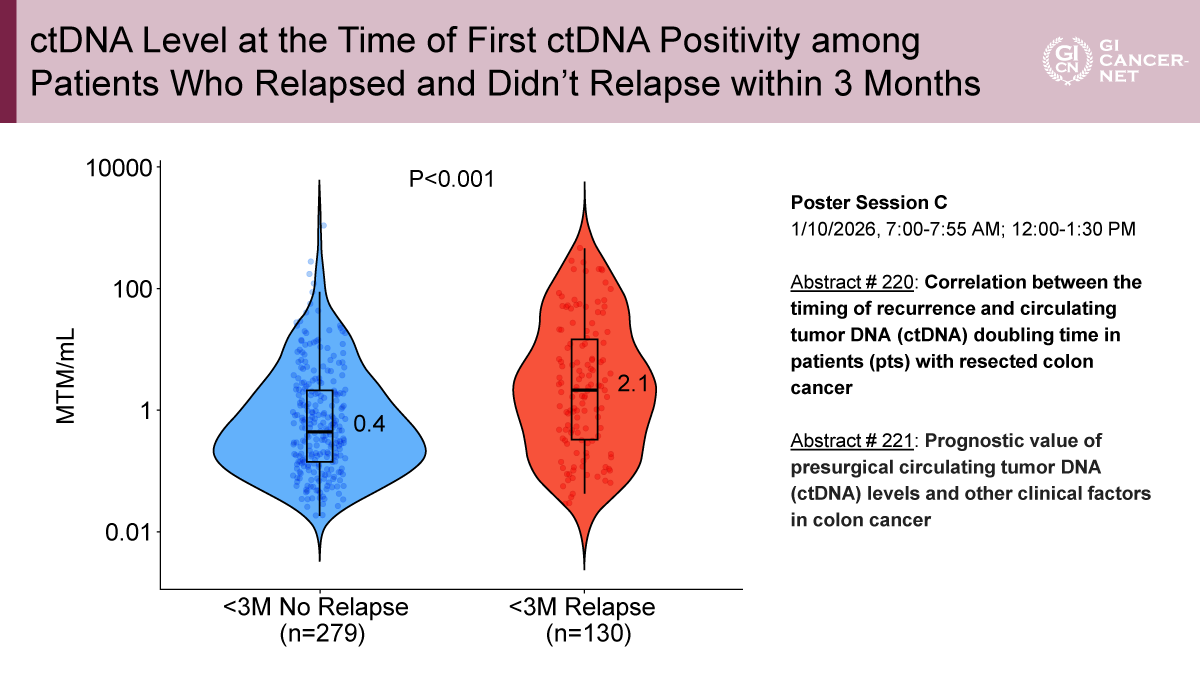
また、ctDNA量はctDNA陽性化から3カ月以内の臨床的な再発なし群で中央値0.4 MTM/mL、再発あり群で中央値2.1 MTM/mLであり、臨床的な再発が認められた群のほうが有意に高かった(p<0.001)(図4)。
発表者の許可を得て掲載(approved by Yoshiaki Nakamura)
発表者の許可を得て掲載(approved by Yoshiaki Nakamura)
発表者の許可を得て掲載(approved by Yoshiaki Nakamura)
発表者の許可を得て掲載(approved by Yoshiaki Nakamura)
結語
ALTAIR試験参加施設では、GALAXY試験の登録症例の6.5%(131/2016)がALTAIR試験に登録された。ACT後にctDNA陽性となった患者では77.5%(55/71)が適格性を満たしていた。病期stageが高いほど適格基準を満たす割合が高く、登録率が増えることが明らかになった。ctDNA高値は3カ月以内の早期再発を示唆する所見となりうる。MRD陽性例を対象とする臨床試験の適格症例を確実に拾い上げるには、ACT中からサーベイランス中にctDNAを連続的に測定し、その動的変化を捉えることが重要と考えられる。
(レポート:愛知県がんセンター ゲノム医療センター 梅垣 翔)
References
- 1) Tie J, et al.: Nat Med. 31(12): 4291-4300, 2025[PubMed]
- 2) Tie J, et al.: N Engl J Med. 386(24): 2261-2272, 2022[PubMed]
- 3) Powles T, et al.: N Engl J Med. 393(24): 2395-2408, 2025[PubMed]
- 4) Tie J, et al.: Sci Transl Med. 8(346): 346ra92, 2016[PubMed]
- 5) Kotani D, et al.: Nat Med. 29(1): 127-134, 2023[PubMed]
- 6) Cha Y, et al.: BMC Cancer. 25(1): 1373, 2025[PubMed]
関連サイト
- ・ALTAIR試験[ClinicalTrials.gov]
- ・GALAXY試験[ClinicalTrials.gov][ASCO GI 2022学会レポート][CIRCULATE-Japan]










谷口 浩也先生
愛知県がんセンター 薬物療法部 医長