膵癌
DDR(DNA damage repair)遺伝子異常を有する遠隔転移膵癌に対するDurvalumab+Olaparib併用療法の第II相試験
Phase II study of durvalumab plus olaparib in patients with metastatic pancreatic cancer and DNA damage repair genes alterations
Teresa Macarulla, et al.
Expert’s view
胆道癌とは対照的に、切除不能または再発の進行膵癌に対する薬物療法は、殺細胞性抗癌剤がその中心を担っており、分子標的薬として、臓器横断的に使用可能な薬剤を除いては唯一、生殖細胞系列のBRCA1またはBRCA2遺伝子変異陽性例の白金製剤治療後の維持療法としてOlaparibが承認されている。最近の膵癌のトピックスの大部分をKRAS阻害薬の開発が占める中で、今回、Pembrolizumabを上乗せした併用療法の有効性および安全性が検討された。
有効性に関して、対象患者など、同様のデザインで行われたPOLO試験1)におけるOlaparib単剤のPFS中央値が7.4カ月、OS中央値が18.9カ月、奏効割合が20%であったことを考慮すると、Pembrolizumabの上乗せ効果については、対象患者の絞り込みなどを含めて慎重な判断が必要である。
OlaparibとPembrolizumabの併用療法は既に、乳癌、卵巣癌などでの開発が先行し、臓器横断的な臨床試験成績も報告されている。ただし、免疫チェックポイント阻害薬がさまざまな癌種の標準治療に組み入れられる中で膵癌は免疫療法が奏効しない数少ない癌種の1つである。また、乳癌や卵巣癌と比較するとOlaparib単剤の治療成績も膵癌では芳しくない。一部のフラクションであるものの、予後不良な膵癌患者の希望となり得るのか、さらなる検討が求められる。
(コメント・監修:金沢医科大学 腫瘍内科 准教授 寺島 健志)
背景
転移性膵癌の予後は不良だが、BRCA1、BRCA2、PALB2などのDNA損傷修復(DDR)遺伝子異常を有する症例では、プラチナ製剤およびPARP阻害薬に対する感受性が高いことが知られている。近年、PARP阻害と免疫チェックポイント阻害の併用が抗腫瘍免疫を増強する可能性が示唆されており、本試験ではその有効性および安全性が検討された。
試験デザイン
本試験は、DDR遺伝子異常を有する転移性膵癌患者を対象としたopen label、single arm、多施設共同の第II相試験である。プラチナ製剤を含む一次または二次治療後に病勢進行を認めていない患者を対象に、Durvalumab+Olaparib併用療法の有効性および安全性が評価された。
- 登録期間:2022年12月〜2024年10月
- 加施設:14施設
- 登録患者数:40例
患者背景
年齢中央値は57歳(IQR: 50-65)であり、女性は52.5%を占めていた。原発巣は膵頭部が35.9%と最も多く、膵体部および膵尾部はいずれも28.2%であった。病期はstage IVが大半(87.2%)を占めていた。ECOG PSは0が53.8%、1が46.2%であった。転移部位としては肝転移が85.0%と最も多く、肺転移は22.5%、腹膜転移は15.0%に認められた。DDR遺伝子異常の内訳は、BRCA2変異が80%と多数を占め、BRCA1変異およびPALB2変異はいずれも10.0%であった。既治療ライン数は1ラインが80.0%、2ラインが20.0%であった。一次治療としてはOxaliplatinが70.0%、Cisplatinが20.0%で使用されていた(表1)。
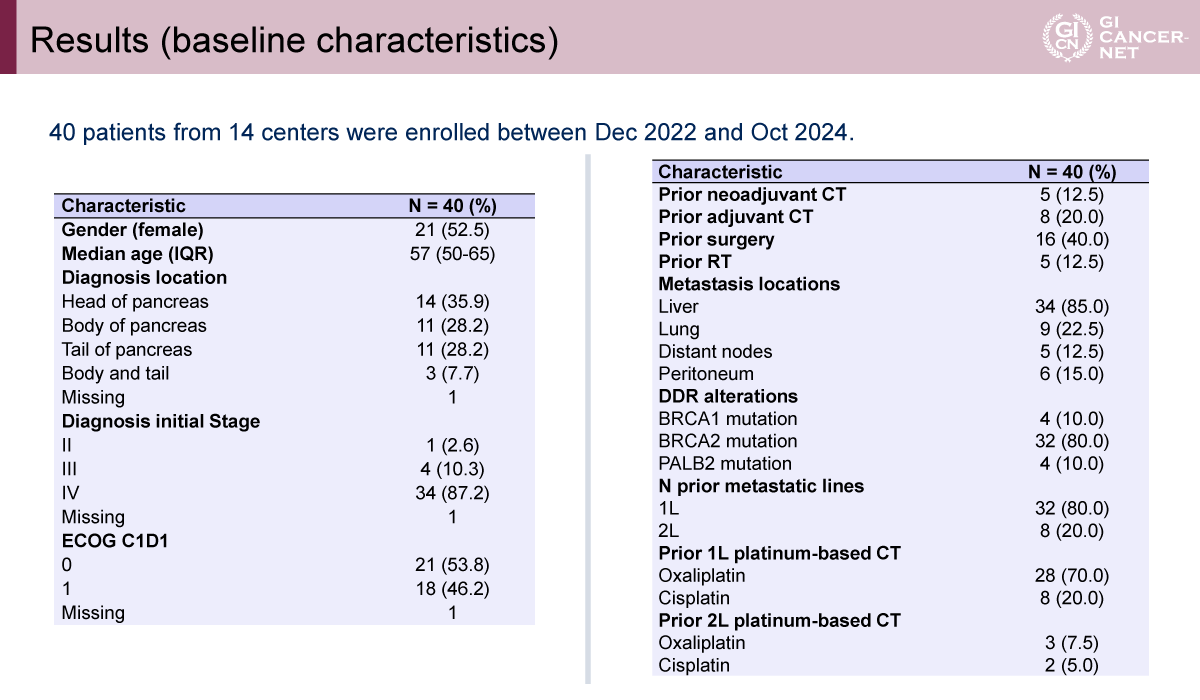
発表者の許可を得て掲載(approved by Teresa Macarulla)
有効性
奏効割合において、併用療法は良好な抗腫瘍効果を示した。解析時点で13例が治療継続中であった。
- 奏効割合:35.0%
- 完全奏効(CR):2例
- 部分奏効(PR):12例
- 病勢制御割合(DCR):77.5%
- 奏効持続期間(DoR)中央値:14.5カ月(95% CI: 14.5-NA)
Swimmer plotでは、奏効の持続が比較的長期間に及ぶ症例が確認された(図1)。
無増悪生存期間(PFS)および全生存期間(OS)はいずれも、DDR遺伝子異常を有する集団において臨床的に意義のある成績を示した(図2、図3)。サブグループ解析では、特定のDDR遺伝子背景における治療効果の差異が示唆された。
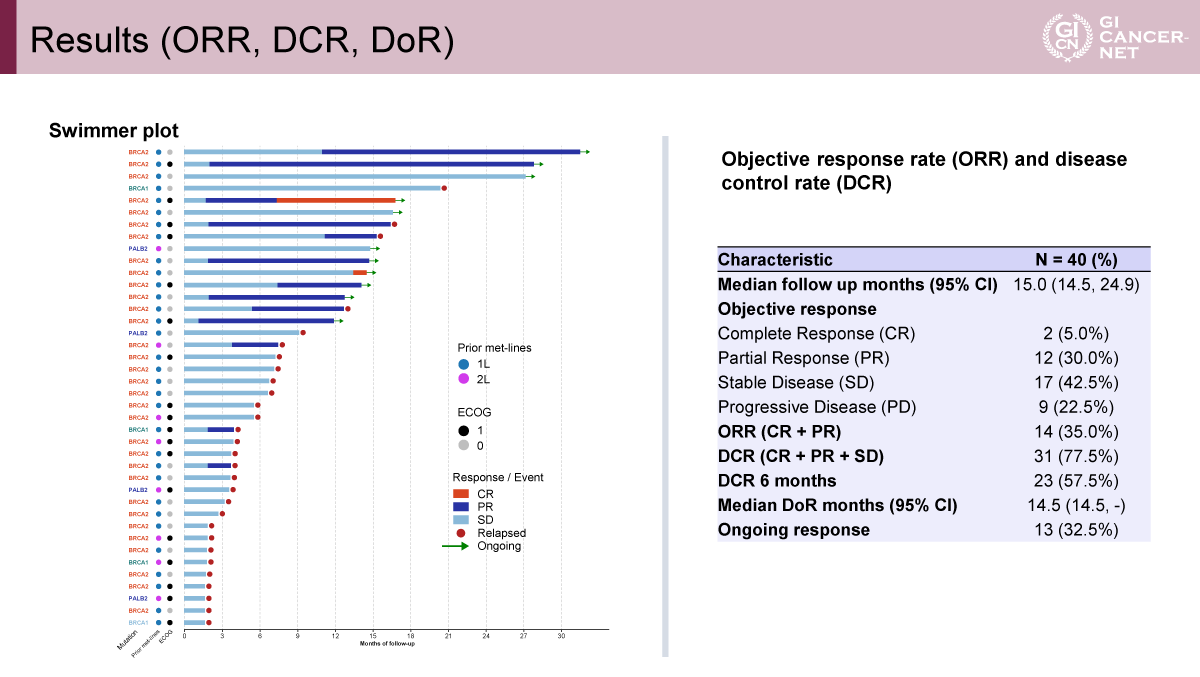
発表者の許可を得て掲載(approved by Teresa Macarulla)
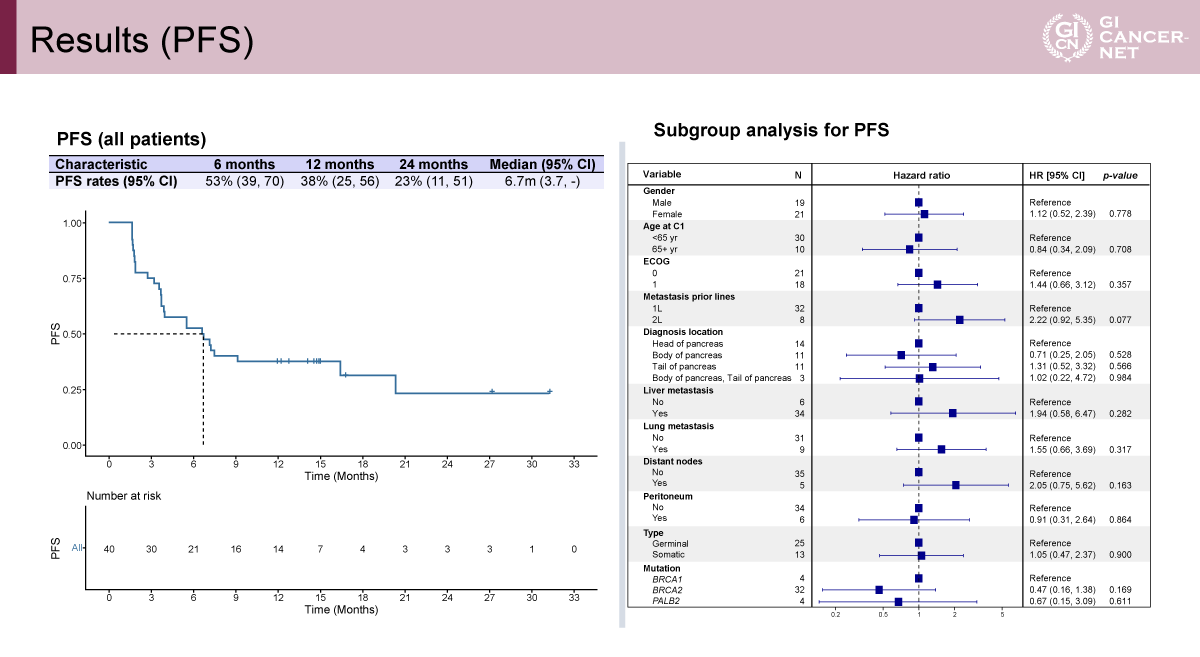
発表者の許可を得て掲載(approved by Teresa Macarulla)
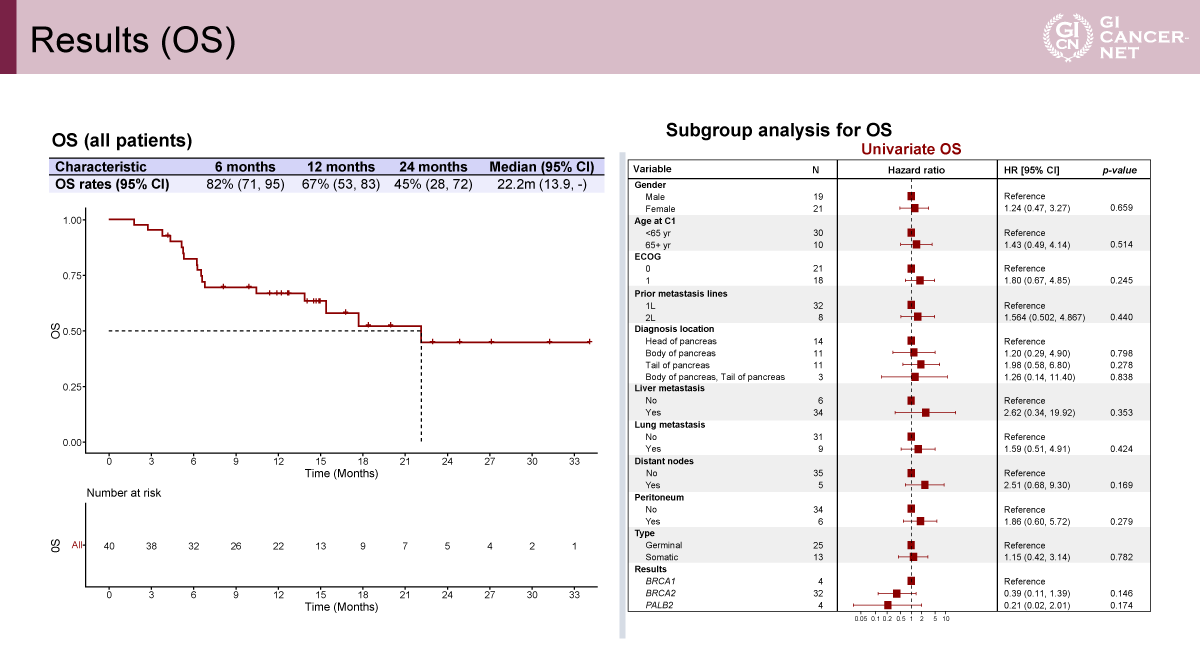
発表者の許可を得て掲載(approved by Teresa Macarulla)
安全性
本併用療法の安全性プロファイルは、既知の各薬剤の毒性と概ね一致しており、全体として管理可能であった。Grade≧3の主な有害事象は貧血(10%)、腹痛(5%)であり、新たな副作用プロファイルは認められなかった(図4)。
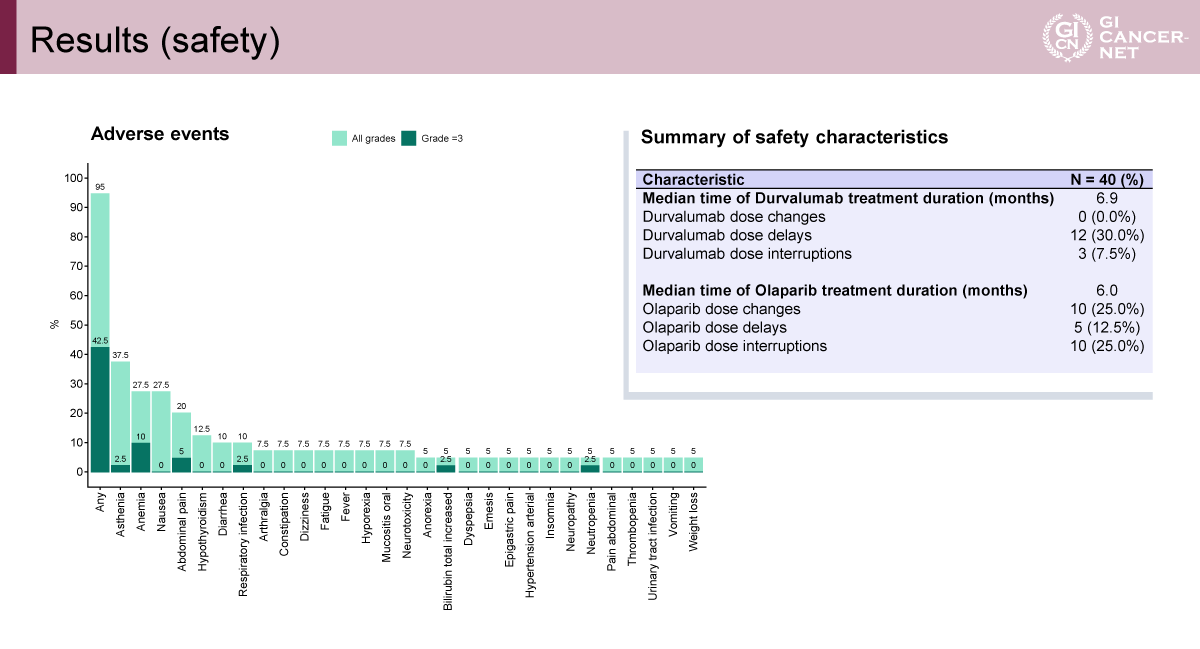
発表者の許可を得て掲載(approved by Teresa Macarulla)
結論
DDR遺伝子異常を有する転移性膵癌患者において、プラチナ製剤治療後のDurvalumab+Olaparib併用療法は、良好かつ持続的な抗腫瘍効果を示し、管理可能な安全性プロファイルを示した。遺伝子異常に基づく治療戦略として、本併用療法は有望な選択肢となる可能性が示唆された。
(レポート:国立がん研究センター東病院 肝胆膵内科 澁木 太郎)
Reference
- 1) Golan T, et al.: N Engl J Med. 381(4): 317-327, 2019[PubMed]
関連サイト
- ・NCT05659914[ClinicalTrials.gov]










寺島 健志先生
金沢医科大学 腫瘍内科 准教授