大腸癌
COMMIT試験:dMMRまたはMSI-H切除不能進行再発大腸癌の1次治療におけるAtezolizumab単剤とmFOLFOX6+Bevacizumab+Atezolizumabを比較する無作為化第III相試験(NRG-GI004/SWOG-S1610)
NRG-GI004/SWOG-S1610: COlorectal cancer dMMR Immuno-Therapy (COMMIT) study -A randomized phase III study of atezolizumab monotherapy versus mFOLFOX6/bevacizumab/atezo in the first-line treatment of patients with dMMR or MSI-H metastatic colorectal cancer-
Caio Max Sao Pedro Rocha Lima, et al.
Expert’s view
本試験は、MSI-High/dMMRを有する切除不能進行再発大腸癌を対象とした複合免疫療法の開発試験であり、大腸癌の標準治療の一つであるchemo+Bevacizumabと併用したレジメンが検証された。CheckMate 8HW試験の結果に基づき、現在のMSI-High/dMMR大腸癌の標準1次治療はNivolumab+Ipilimumab併用療法である。本試験の対照群はAtezolizumabの免疫チェックポイント阻害薬の単剤療法であり、Nivolumab・Pembrolizumabとも違い抗PD-L1抗体薬である点も違いがある。
他の試験と直接比較することはできないものの、KEYNOTE-177試験のPembrolizumab群のPFSと比較して、本試験のPFSが短いようにみえることが気になるが、MSI/MMRの診断の質が良くないことが影響していると議論されていた。となれば、それぞれの群でnon-MSI-High症例が一定数含まれている可能性があり、Atezolizumab単剤療法群のPFSは悪くなる一方で、chemo+Bevacizumab併用群では標準治療が担保されている形となる。さらに、immatureなデータであるものの、OSの結果において2群が重なっている点も気になるところである。
MSI-High/dMMRを有する切除不能進行再発大腸癌の1次複合免疫療法については、Nivolumab+Ipilimumab併用療法を主軸に質の高い臨床試験で比較することが求められるであろう。
(コメント・監修:聖マリアンナ医科大学 臨床腫瘍学講座 主任教授 砂川 優)
免疫チェックポイント阻害薬への化学療法と抗VEGF抗体薬の併用療法を検証する
ミスマッチ修復欠損(dMMR)または高頻度マイクロサテライト不安定性(MSI-H)を有する切除不能進行再発大腸癌(mCRC)は、全mCRCの約5%を占める。2020年に報告されたKEYNOTE-177試験の結果を受け、Pembrolizumabは1次治療の標準治療となった。しかし、約半数の患者が12カ月以内に病勢進行を来しており、免疫療法単独では十分な効果が得られない患者が一定数存在することが課題であった1)。
その後、CheckMate 8HW試験では、1次治療においてNivolumabとIpilimumab(Nivo+Ipi)の免疫チェックポイント阻害薬併用療法が標準化学療法と比較して無増悪生存期間(PFS)を有意に改善した2)。現在、本邦においてもNivo+IpiはdMMR/MSI-H mCRCの1次治療の標準治療の一つとして承認されている。
一方、本試験は免疫チェックポイント阻害薬に化学療法と分子標的薬を組み合わせる複合免疫療法を検証するものである。前臨床研究では、OxaliplatinとPD-L1阻害薬の併用が腫瘍増殖抑制と生存延長をもたらし、化学療法が腫瘍微小環境を免疫応答に有利な状態へ変化させ得ることが示唆されている3,4)。さらにASCO 2025でATOMIC試験の結果が報告され、stage IIIのdMMR/MSI-H結腸癌においてFOLFOXにAtezolizumab(Atezo)を上乗せすることで無病生存期間が有意に改善し、化学療法併用の有効性が臨床的にも支持されている。加えて、抗VEGF療法を組み合わせることで腫瘍血管の正常化や免疫細胞の腫瘍内浸潤が促進され、免疫療法の効果が一層高まる可能性が示唆されている5)。
COMMIT試験は、PD-L1阻害薬であるAtezoにmFOLFOX6+Bevacizumab(FFX/Bev)を併用することで、免疫チェックポイント阻害薬単剤療法を上回る治療効果が得られるかを検証することを目的として計画された。
試験デザイン:Atezolizumab単剤 vs. FOLFOX+Bevacizumab+Atezolizumab併用
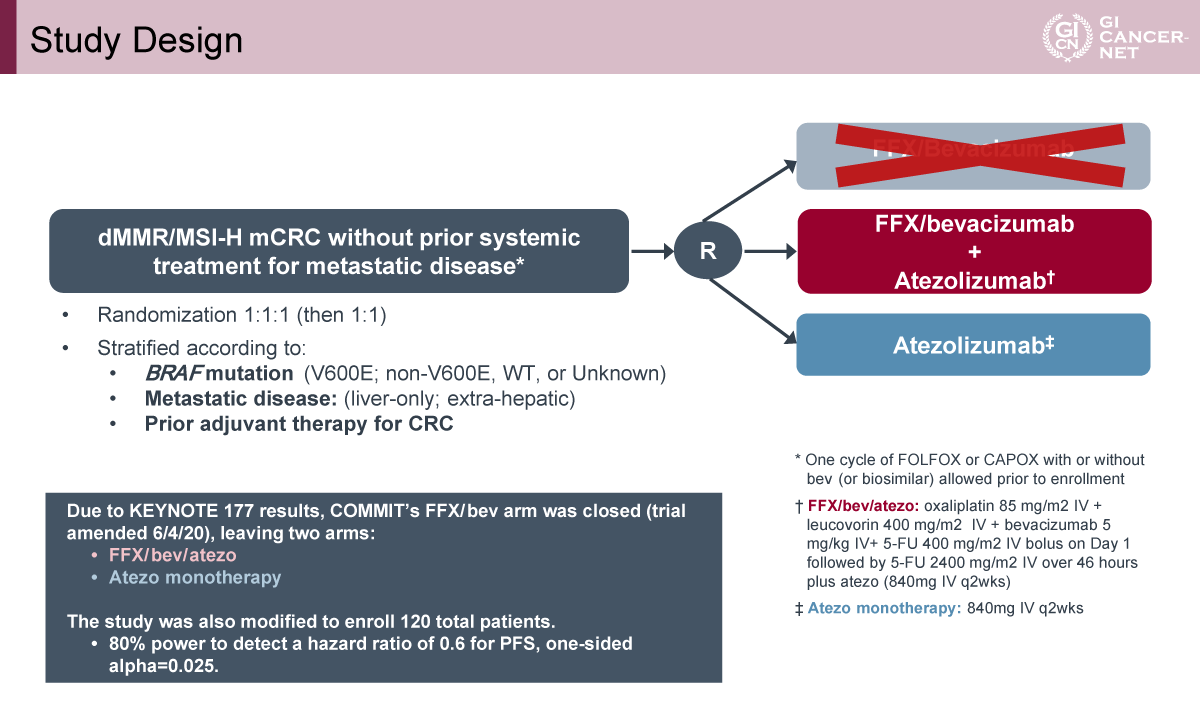
本試験(COMMIT:NRG-GI004/SWOG-S1610)は、dMMRまたはMSI-Hを有するmCRCを対象とした米国における多施設共同・非盲検・第III相無作為化比較試験である。1次治療として、Atezo単剤と、mFOLFOX6+Bevacizumab+Atezolizumab(FFX/Bev/Atezo)併用の有効性および安全性を比較検討した。登録時にBRAF V600E変異の有無、転移様式(肝限局か否か)、術後補助療法の既往などで層別化の上、無作為に割り付けた。
試験開始当初は、FFX/Bev単独、FFX/Bev/Atezo、Atezo単剤の3群比較(1:1:1)であったが、KEYNOTE-177試験の結果を受けて化学療法単独群は登録中止となり、以降はFFX/Bev/Atezo群とAtezo単剤群の2群比較に改訂された(図1)。
主要評価項目はPFSとし、副次評価項目として奏効率(ORR)、病勢制御率(DCR)、全生存期間(OS)、および安全性を設定した。統計設定では、PFSにおいてハザード比(HR)0.6(片側α=0.025、検出力80%)が検出されることを設定し、目標登録数は120例とした。主要解析はITT集団で行い、事前に規定された中間解析に基づき、PFSの優越性が確認された場合には試験の早期終了を検討する計画とした。
発表者の許可を得て掲載(approved by Caio Max Sao Pedro Rocha Lima)
中間解析結果:化学療法+抗VEGF抗体併用によるPFSの有意な改善と早期増悪リスクの抑制
CheckMate 8HW試験の結果を受け、2025年3月31日に本試験の登録は中断された。同時期に、事前に計画された中間解析が実施された。登録期間は2017年11月から2025年3月までで、計102例が登録された。本解析では、試験当初に設定されていた化学療法群を除外し、FFX/Bev/Atezo併用群(n=41)とAtezo単剤群(n=41)の2群を統計解析対象とした。年齢、性別、ECOG PS、BRAF V600E変異、転移様式、腫瘍占拠部位(左側か右側か)などの予後に影響し得る因子に大きな偏りは認められなかった。
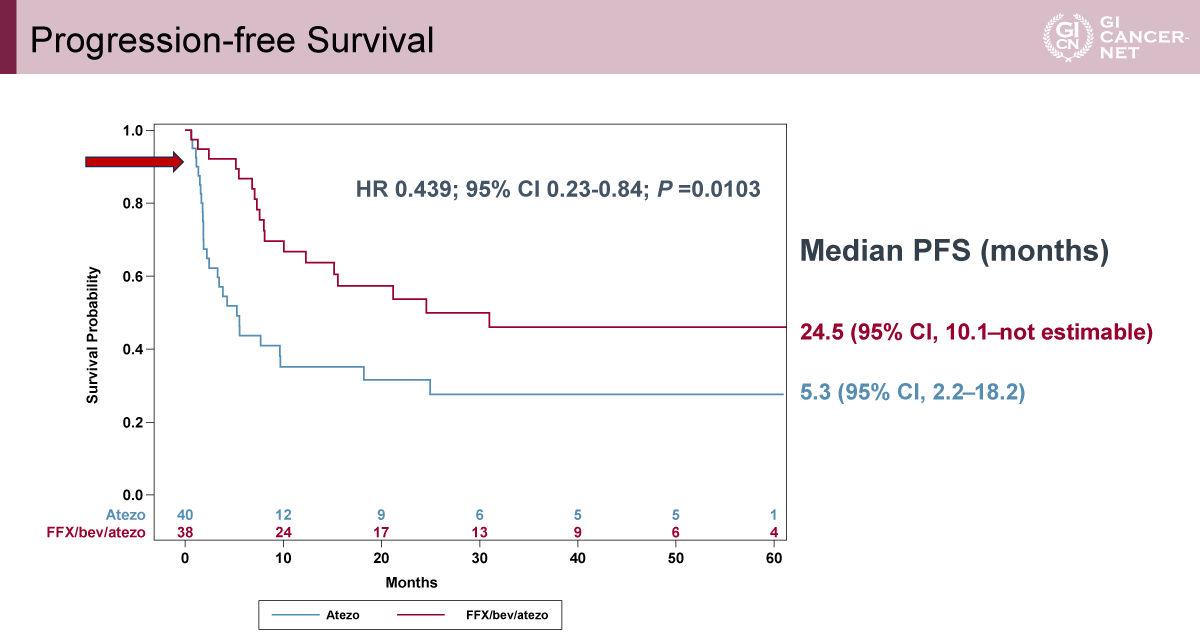
主要評価項目であるPFSの中間解析は、追跡期間中央値3.5年、PFSイベント45件、情報率65%の時点で実施された。PFSは併用群で有意に延長し(HR=0.439、95% CI: 0.23-0.84、p=0.0103)、中央値PFSは併用群24.5カ月、単剤群5.3カ月で、O’Brien-Fleming法に基づく事前規定の中間解析有意水準(p<0.0152)を満たした。さらにKaplan-Meier曲線では、単剤群で治療早期から病勢進行に至る症例が相対的に多く認められた。一方、FFX/Bev/Atezo併用群ではKaplan-Meier曲線の形状から、治療開始早期の病勢進行が相対的に少なく、化学療法およびBevacizumabの追加により早期増悪リスクが軽減される可能性が示された(図2)。
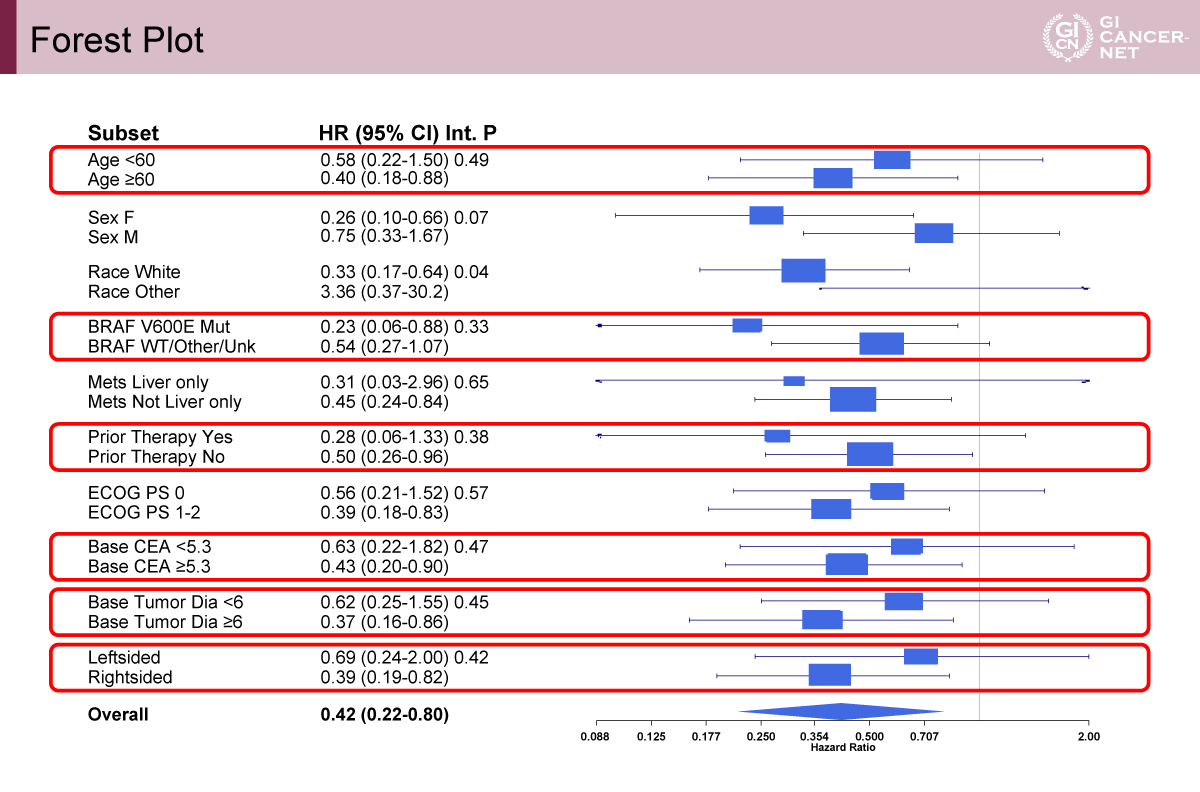
サブグループ解析では全体として一貫したPFS改善傾向が認められ、特に高齢、右側結腸、BRAF V600E変異、肝外転移、ECOG PS 1-2、腫瘍径が大きい、CEA高値といった高リスク因子を有する患者群で併用療法のPFSが良好な傾向がみられた(図3)。
奏効に関しても、ORRは併用群86.1%、単剤群46%、CRは36.1% vs. 18.9%、PDは2.8% vs. 32.4%と、腫瘍縮小効果および病勢制御の両面で併用群が優れていた。12カ月時点のDCRも、併用群64.7%、単剤群32.4%であった。
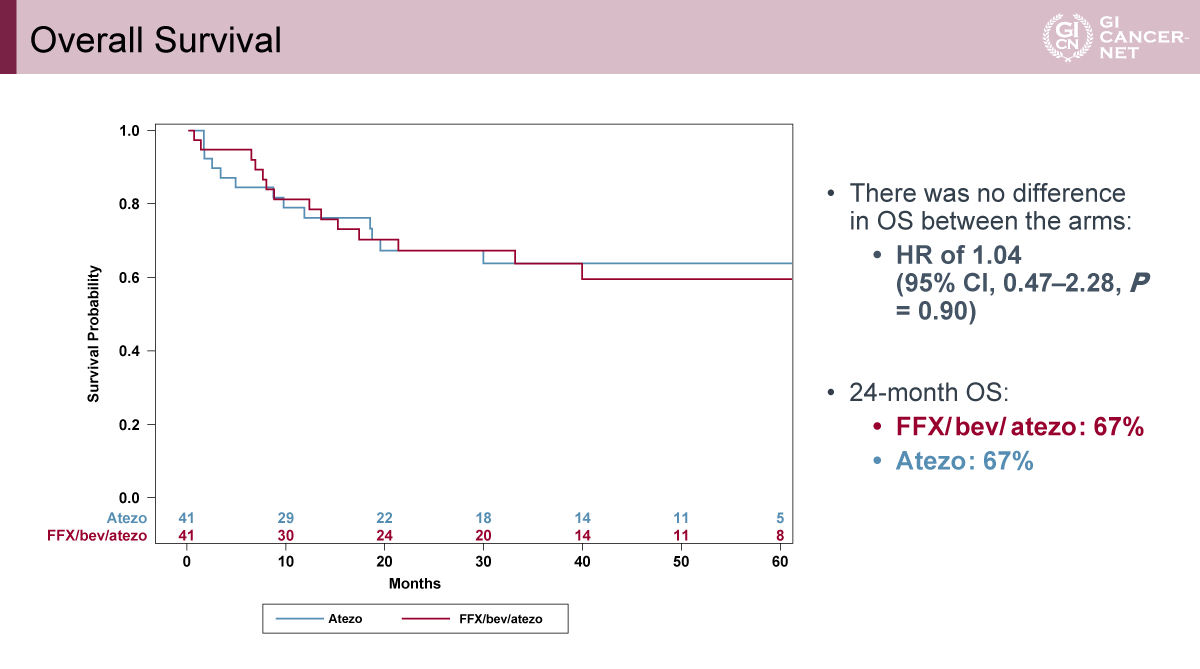
一方、OSについては現時点で有意差は認められず(HR=1.04、95% CI: 0.47-2.28、p=0.90)、24カ月OSは両群とも67%であった(図4)。
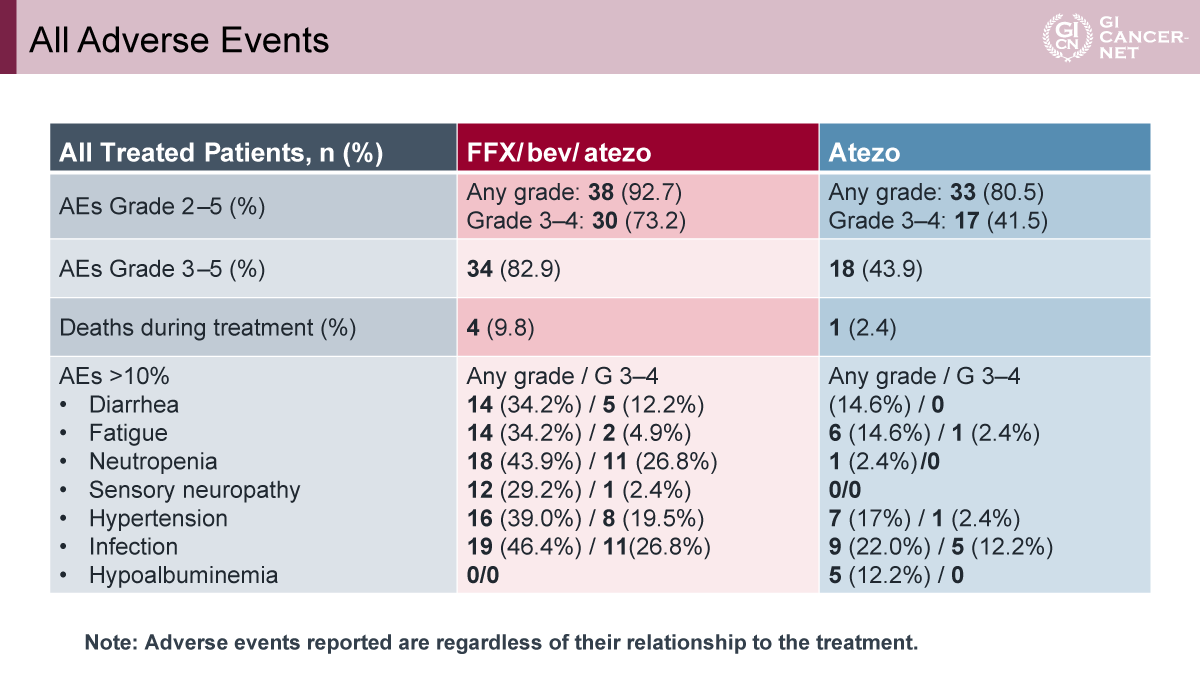
安全性では、grade 3-4の有害事象は併用群で高頻度に認められた(73.2% vs. 41.5%)(表1)。主な有害事象は、下痢、好中球減少、末梢神経障害、高血圧、感染症などで、化学療法およびBevacizumab併用に伴う既知の毒性プロファイルと一致していた。Grade 5有害事象は計5例で、単剤群では病勢進行による死亡が1例、併用群では4例(病勢進行1例、サイクル16および18投与後の突然死が各1例、サイクル12後に施行された右肝拡大切除後の肝出血が1例)であった。
発表者の許可を得て掲載(approved by Caio Max Sao Pedro Rocha Lima)
発表者の許可を得て掲載(approved by Caio Max Sao Pedro Rocha Lima)
発表者の許可を得て掲載(approved by Caio Max Sao Pedro Rocha Lima)
発表者の許可を得て掲載(approved by Caio Max Sao Pedro Rocha Lima)
まとめ:安全性の懸念とOSの最終評価は今後の課題
COMMIT試験の中間解析では、FFX/Bev/Atezo併用療法がAtezo単剤に比べてPFSを有意に延長した。Kaplan-Meier曲線の形状からは、単剤治療で課題となる治療早期の病勢進行が、化学療法および抗VEGF抗体薬の追加によって抑えられる可能性が示唆された。一方、OSの有意差は現時点では確認されておらず、grade 3-4有害事象の増加やgrade 5事象の発生を踏まえると、有効性と安全性を含めた総合的な評価が必要である。
発表後の質疑では、免疫療法単剤群のPFSがKEYNOTE-177試験やCheckMate 8HW試験と比べて短くみえる点が議論された。発表者は、その要因として本試験ではMSI/MMR判定の中央判定が行われていないことを挙げ、MSI/MMRの誤分類がAtezo単剤群のPFSを短くした可能性があると説明した。また、本試験はグローバル試験ではなく米国の施設のみで実施された試験であり、患者背景や試験運用に違いがあり、試験間でPFSを単純に比較して結論づけることは難しいとの見解を示した。
今後は、どのような患者にFFX/Bev/Atezo併用療法が最適かを同定することが重要であり、進行中のOS解析に加え、バイオマーカー解析によって、治療群間で転帰が分かれた背景の理解が深まることが期待される。
(レポート:聖マリアンナ医科大学 臨床腫瘍学講座 武田 弘幸)
References
- 1) André T, et al.: N Engl J Med. 383(23): 2207-2218, 2020[PubMed]
- 2) André T, et al.: N Engl J Med. 391(21): 2014-2026, 2024[PubMed]
- 3) Golchin S, et al.: J Cell Physiol. 234(11): 19866-19874, 2019[PubMed]
- 4) Wang W, et al.: Biochem Biophys Res Commun. 487(1): 1-7, 2017[PubMed]
- 5) Li X, et al.: Int Immunopharmacol. 149: 114212, 2025[PubMed]
関連サイト
- ・COMMIT試験[ClinicalTrials.gov]
- ・CheckMate 8HW試験[ClinicalTrials.gov][ASCO 2024学会レポート][論文紹介]
- ・KEYNOTE-177試験[ClinicalTrials.gov][論文紹介]
- ・ATOMIC試験[ClinicalTrials.gov][ASCO 2025学会レポート]










砂川 優先生
聖マリアンナ医科大学 臨床腫瘍学講座 主任教授